Международный эндокринологический журнал Том 15, №2, 2019
Вернуться к номеру
Превентивная диабетология на рубеже столетий. Профилактика сахарного диабета второго типа: достижения и перспективы
Авторы: Генделека Г.Ф. (1), Генделека А.Н. (2)
1 - Одесский национальный медицинский университет, г. Одесса, Украина
2 - Коммунальное некоммерческое предприятие «Центр первичной медико-санитарной помощи № 5» Одесского городского совета, г. Одесса, Украина
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
У статті наводяться досягнення в області профілактики цукрового діабету (ЦД) 2го типу. На даний час проведені різні дослідження з профілактики ЦД з різним дизайном, видом втручання, тривалістю спостереження і механізмом дії. Один із можливих механізмів впливу полягає в тому, щоб загальмувати темп досягнення пікової поширеності ЦД. Другий сценарій стосується більшості перевірених медикаментозних втручань, за допомогою яких вдається знизити темп конверсії порушень толерантності до глюкози в маніфестації ЦД. Третя можлива превентивна модель полягає в досягненні стійкої стабілізації толерантності до глюкози. Після виявлення передумов для розвитку ЦД 2го типу профілактичні заходи повинні проводитися протягом 10–12 років, поки бетаклітини функціонально активні.
В статье приводятся достижения в области профилактики сахарного диабета (СД) 2-го типа. В настоящее время проведены различные исследования по профилактике СД с разным дизайном, видом вмешательства, длительностью наблюдения и механизмом действия. Один из возможных механизмов влияния заключается в том, чтобы затормозить темп достижения пиковой распространенности СД. Второй сценарий касается большинства проверенных медикаментозных вмешательств, с помощью которых удается снизить темп конверсии нарушений толерантности к глюкозе в манифестации СД. Третья возможная превентивная модель заключается в достижении стойкой стабилизации толерантности к глюкозе. После выявления предпосылок для развития СД 2-го типа профилактические мероприятия должны проводиться на протяжении 10–12 лет, пока бета-клетки функционально активны.
This article presents the key achievements in the field of diabetes mellitus prevention. Currently, various researches have been conducted on the prevention of diabetes mellitus, with different designs, types of intervention, duration of followup and mechanisms of action. One of the possible mechanisms is aimed to slow down the rate of the peak prevalence of the diabetes mellitus. The second possibility is concerned the majority of medical interventions conducted, which enable to decrease the rate of impaired glucose tolerance in manifestation of diabetes mellitus. The third preventive model consists in a strong stabilization of glucose tolerance. After detection of preconditions, which result in diabetes mellitus, preventive methods should be tested for 10–12 years, while beta cells are functionally active.
цукровий діабет 2го типу; профілактика; стратегія предикції; порушення толерантності до глюкози; модифікація способу життя
сахарный диабет 2-го типа; профилактика; стратегия предикции; нарушение толерантности к глюкозе; модификация образа жизни
type 2 diabetes mellitus; prevention; prediction strategies; impaired glucose tolerance; lifestyle modification
Сахарный диабет (СД) 2–го типа — это глобальная проблема системы здравоохранения. За 50 лет, т.е. продолжительность жизни двух поколений, распространенность СД выросла в 10 раз — с 0,5–0,6 до 5–7 % и продолжает расти с угрожающей скоростью [1]. Количество больных этим тяжелым заболеванием в настоящее время в мире составляет 425 млн. К следующему столетию 25–30 % населения планеты могут страдать СД.
В отличие от СД 1–го типа диабет 2–го типа во многом является продуктом современного способа питания и современного образа жизни. Система быстрого питания и сидячий образ жизни в добавление к избыточной массе тела увеличивает риск развития СД 2–го типа.
Большинство заболеваний, которые распространены в современных цивилизованных странах (ожирение, СД 2–го типа, сердечно–сосудистые заболевания, метаболический синдром), являются результатом неспособности генов соответствовать современному образу жизни. Мы создали такие усло–вия, в которых геном уже не справляется с современным способом питания и образом жизни [2].
Эффективная профилактика СД требует глубоких знаний этиологии и патогенеза заболевания. Рассматривая проблему под этим углом, следует подчеркнуть, что до сих пор неизвестны все генетические дефекты, которые лежат в основе как СД 1–го, так и СД 2–го типа. Другой факт заключается в необходимости обнаружения условий внешней среды, выполняющих роль пускового фактора (триггера), а эти факторы различны при разных типах СД.
При СД 2–го типа выявлено генетически детерминированное ограничение способности к репликации β–клеток и первичное или адаптивное нарушение секреции инсулина.
Фенотипическая экспрессия базисного генетического дефекта происходит после постоянной перегрузки секреторной мощности инсулинопродуцирующего аппарата. Перегрузка связана с инсулинорезистентностью (ИР) органов–мишеней. Индуктором ИР служит целый ряд факторов, из них прежде всего:
— гиперкалорийное питание;
— ожирение и избыточная масса тела;
— снижение двигательной активности (гиподинамия);
— процесс постарения населения.
Изначальным дефектом в развитии СД является периферическая ИР, которая вызывает перегрузку β–клеток в течение длительного времени, что в конечном итоге приводит к истощению эндогенного резерва инсулина. Проявлением этого процесса является редукция глюкозоиндуцированной секреции, которая проявляется сначала выпадением раннего пика секреции, а затем снижением секреции инсулина. Неспособность β–клеточного аппарата адекватно отвечать на повышенные нагрузки соответствующим объемом репликации β–клеток в конечном итоге приводит к уменьшению количества последних до 40 % от нормальных показателей. Время манифестации СД 2–го типа детерминируется степенью истощения эндогенного резерва инсулина, то есть состоянием функции β–клеток и уровнем ИР [3].
Важнейшим вопросом при предупреждении СД 2–го типа является восстановление массы β–клеток. Стратегия должна заключаться в индукции регенерации их из эндогенных источников. Доказано, что масса β–клеток динамична и способна адаптивно изменяться в соответствии с различными потребностями организма в инсулине. У людей масса β–клеток увеличивается при ожирении примерно на 50 %, секреция инсулина и масса β–клеток возрастают также у беременных женщин [4].
Продолжаются дебаты о механизмах поддержания массы β–клеток и численности их популяции у взрослых. Обсуждаются два возможных пути.
С одной стороны, убедительно доказана возможность митотического деления предсуществующих β–клеток. Так, доказано, что в поджелудочной железе взрослых мышей, крыс и людей, а также у постнатальных мышей возможно образование новых β–клеток исключительно путем митотического деления существующих.
С другой стороны, тесную связь между экзокринными протоками и β–клетками считают доказательством того, что β–клетки могут возникать также из стволовых клеток эпителия протоков поджелудочной железы. Обнаружено значительное увеличение числа таких клеток у грызунов после длительной гиподинамии или лечения глюкагоноподобным пептидом 1 (ГПП–1).
Сейчас нет сомнений в том, что деление β–клеток продолжается в течение всей жизни. Однако частота репликации β–клеток островков Лангерганса у взрослых людей очень низкая, что затрудняет ее определение. Низкая при нормальных условиях скорость деления β–клеток в случае значительной потребности в инсулине возрастает. У грызунов скорость деления β–клеток увеличивается в 5–10 раз после частичной резекции поджелудочной железы, во время беременности, при хронической инфузии глюкозы и после лечения ГПП–1. Все это свидетельствует о значительной пластичности эндокринного аппарата поджелудочной железы у грызунов [5].
У людей способность к репликации β–клеток (то есть репликационный потенциал) значительно ниже, чем у грызунов, и в поджелудочной железе взрослого человека можно обнаружить очень мало делящихся β–клеток (одна клетка примерно в 50 островках из примерно 100 β–клеток на каждом поперечном срезе). В ряде недавних исследований высказано предположение, что β–клетки человека сохраняют способность к регенерации даже на очень позднем этапе жизни.
В чем заключается физиологическая цель профилактики? Какая профилактика является своевременной?
С учетом патогенеза СД 2–го типа, который характеризуется ИР и дисфункцией β–клеток, задача заключается в длительной поддержке физиологической секреции инсулина β–клетками. Исходя из этого, первичной целью является стабилизация и улучшение толерантности к глюкозе (ТГ) путем снижения ИР. С помощью этого можно сдвинуть на более поздние сроки время конверсии нарушения толерантности к глюкозе (НТГ) в явный СД 2–го типа и в результате этого поддерживать уровень глюкозы, чувствительность к инсулину и функцию β–клеток на стадии НТГ на приемлемом уровне и даже в норме.
С учетом стабилизации ТГ возникает вопрос: насколько различные интервенционные мероприятия по профилактике СД способны привести к снижению частоты развития СД 2–го типа и каких целей можно добиться с помощью первичной профилактики?
Возможные модели профилактики сахарного диабета
В настоящее время проведены различные исследования по профилактике СД с разным дизайном, видом вмешательства, длительностью наблюдения, механизмом действия и исходными гипотезами. Имеется необходимость вкратце рассмотреть различные возможные модели профилактики СД.
Один из возможных механизмов влияния интервенций может заключаться в том, чтобы затормозить темп достижения пиковой частоты распространения СД, однако в долгосрочной перспективе абсолютная частота заболевания не изменяется. Это касается, как правило, тех видов вмешательства, эффективность которых ускользает в среднесрочной перспективе (например, программа изолированного снижения массы тела). В этом случае интервенция в течение определенного времени приводит к уменьшению квоты конверсии НТГ в явный СД, следовательно, к уменьшению числа вновь заболевших в сравнении с лицами без такого вмешательства. Через определенный промежуток времени, 3–8 лет, эффективность и стойкость интервенции значительно падает и обе кривые сходятся. В конечном итоге частота манифеста СД становится одинаковой в более поздние сроки наблюдения и отсутствуют различия между опытной и контрольной группами.
Тем не менее у многих пациентов удается на время интервенции отодвинуть манифестацию диабета. Таким образом, этот вид вмешательства в состоянии эффективно затормозить конверсию НТГ в явный диабет, однако не предупредить навсегда.
Второй сценарий касается большинства проверенных медикаментозных вмешательств. В этом случае с помощью медикаментозных препаратов удается пропорционально уменьшать темп достижения пиковой частоты конверсии НТГ, что в действительности означает профилактику и предупреждение болезни. Это действие сохраняется на протяжении всего периода приема препаратов. Однако после прекращения медикаментозной интервенции (отмены препаратов) в период фазы вымывания квота конверсии в этой группе становится больше, чем прежде, и быстро достигает показателя контрольной группы.
Это вмешательство по сути соответствует лечению СД как такового с помощью антидиабетических средств и, тем не менее, не характеризуется стойким превентивным эффектом. Этот эффект прямо связан с применением лекарственных препаратов. К исследованиям с этой моделью действия относится SТOP–NIDDM [6–8].
Третья возможная превентивная модель заключается в целевом достижении стойкой стабилизации ТГ. Этот сценарий предусматривает интервенцию, с помощью которой достигается пропорциональное замедление роста частоты конверсии НТГ в явный СД. При этом интервенция приводит к таким изменениям метаболизма, которые носят стойкий характер и более продолжительны, чем сама интервенция. В фазе вымывания происходит рост частоты СД больше, чем в период вмешательства. Однако этот рост идет параллельно контрольной группе и на более низком уровне и не достигает величин, наблюдае–мых у лиц без интервенции. Эта различная частота конверсии (расстояние между двумя кривыми) соответствует действительным превентированным годам СД. Такого эффекта можно достичь только постоянной модификацией образа жизни или изменением условий жизни. Изменения такого рода вызывает медикаментозная интервенция. Такой сценарий динамики конверсии НТГ характерен для исследования TRIPOD и модификации образа жизни (МОЖ), включающих рациональное питание и увеличение двигательной активности.
Долгосрочная цель эффективной программы первичной профилактики заключается в том, чтобы путем стабилизации ТГ обеспечить наиболее низкую квоту конверсии НТГ в явный СД.
Модификация образа жизни как метод профилактики сахарного диабета второго типа
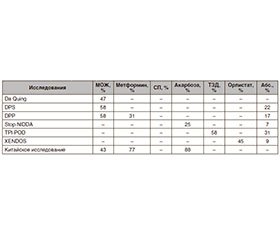
СД 2–го типа особенно хорошо поддается первичной профилактике, т.к. в значительной степени заболевание обусловлено образом жизни пациента, и поэтому соответствующее вмешательство приводит к желаемому результату. Общая задача состоит в раннем выявлении лиц с высоким риском заболевания на доклиническом этапе. Важным является установление варианта МОЖ или медикаментозной терапии, которые наиболее эффективно будут предупреждать или замедлять развитие СД. Результаты многих международных исследований дали первые ответы и с высоким уровнем доказательности подтвердили возможность эффективной профилактики СД 2–го типа с помощью МОЖ или раннего назначения медикаментозной терапии лицам с высоким риском заболевания (табл. 1).
В вышеприведенных исследованиях неоднократно было подтверждено, что МОЖ на раннем этапе заболевания снижает риск развития СД почти на 60 %, а медикаментозная терапия — на 25 %.
В китайском исследовании Da Quing DPS изу–чалось влияние МОЖ на конверсию НТГ в явный СД. В исследование было включено 577 пациентов с НТГ, которые были рандомизированы на контро–льную и опытную группы. Кумулятивная частота развития СД через 6 лет наблюдения в контрольной группе составила 67,7 %, в опытной — 41,1 %. Таким образом, с помощью интенсивной МОЖ (диетотерапия + увеличение двигательной активности) удалось снизить частоту конверсии НТГ в явный СД 2–го типа на 46 % [9–11].
В финском исследовании DPS тоже изучалось влияние МОЖ у лиц с НТГ (n = 522) на риск возникновения СД в течение трех лет. В результате исследования установлено снижение риска развития СД 2–го типа с 23 до 10,2 %, т.е. частота развития заболевания уменьшилась на 58 %. МОЖ включает индивидуальные рекомендации по рациональному питанию и увеличению двигательной активности. Пациенты опытной группы по сравнению с контрольной снизили массу тела на 4,2 кг, увеличили физическую нагрузку, а также отмечали снижение уровня АД и улучшение липидного профиля. Для предупреждения одного случая СД необходимо «лечить» 8 человек. У лиц, снизивших массу тела на 5 % от исходной, риск СД уменьшился на 70 % в сопоставлении с пациентами без снижения массы тела [12].
Снижение массы тела и увеличение двигательной активности являются важнейшими детерминантами успеха.
Цель американского исследования DPP состояла в изучении эффективности влияния МОЖ и раннего назначения метформина на частоту конверсии НТГ в явный СД 2–го типа в сравнении с плацебо–группой. Исследование длительностью 2,8 года показало, что раннее лечение метформином снижает риск развития СД на 31 %, а МОЖ — на 58 % по сравнению с плацебо–группой. Пробанды группы МОЖ снизили массу тела на 5,6 кг, метформин–группа — на 2,1 кг, а контрольная — на 0,1 кг. Частота конверсии НТГ в явный СД 2–го типа составила:
— у лиц с МОЖ — 4,8 случая на 100;
— в метформин–группе — 7,8 случая на 100;
— в плацебо–группе — 11 случаев на 100.
Также в этом исследовании установили, что при МОЖ число NNT составляет 7 случаев, при терапии метформином — 14 случаев, т.е. необходимо лечить столько людей, чтобы предупредить 1 случай СД (14,21).
В рамках превентивного исследования Stop–NIDDМ изучалась эффективность акарбозы с целью предупреждения конверсии НТГ в явный СД. Было установлено, что регулярный прием акарбозы приводит к относительному снижению риска развития заболевания на 25 %. Превентивный эффект исчезал после отмены препарата. После отмены акарбозы отмечалось уменьшение конечных точек как вторичных целей — на 49 %, а именно на столько уменьшилось число сердечно–сосудистых событий и на 34 % — артериальной гипертензии. Это является свидетельством того, что лечение НТГ приводит не только к предупреждению СД, но и снижает сердечно–сосудистый риск.
Результаты этих исследований позволяют сформировать перечень целевых показателей при МОЖ, которые необходимо достичь для предупреждения развития СД.
Они включают:
— снижение массы тела на 7 %;
— ежедневную физическую нагрузку 150 мин;
— содержание пищевых волокон — 15 г/1000 ккал рациона;
— содержание жира в пище до 30 % от суточного калоража;
— содержание насыщенных жирных кислот до 10 % от общего количества жира.
Интерес представляет ретроспективная оценка важности достижения целевых показателей для реализации превентивного потенциала МОЖ.
Достижение одного из целевых показателей не оказывает превентивного эффекта, однако с увеличением количества достигнутых показателей возрастает превентивный потенциал МОЖ. Так, у лиц, достигших 4 или 5 целевых показателей в течение периода наблюдения, удалось почти в 100 % случаев предупредить развитие СД 2–го типа.
Результаты вышеизложенных исследований свидетельствуют о принципиальной возможности первичной профилактики СД с помощью успешной модификации образа жизни, включающей рациональное питание и увеличение двигательной активности.
Второй вывод заключается в том, что назначение некоторых медикаментозных препаратов, а именно раннее назначение метформина или акарбозы лицам с НТГ предупреждает конверсию последней в явный СД.
С учетом переносимости препаратов, а также стоимости лечения в будущих программах превентивной терапии возможна медикаментозная профилактика у определенных лиц, не достигших эффекта с помощью МОЖ, что является приемлемой альтернативой.
Медикаментозная профилактика СД 2–го типа
Метформин
Уже в 2001 году рабочая китайская группа сообщила о результатах проспективного исследования метформина у китайцев с НГТ. Оно показало, что при лечении метформином конверсия НТГ в явный СД снижалась на 76,6 % в сравнении с плацебо–группой. Данные исследования свидетельствовали о высоком потенциале метформина в качестве превентивного средства.
В DPP–исследовании пациенты принимали метформин 850 мг 2 раза в сутки или плацебо.
В сопоставлении с плацебо–группой метформин уменьшил число новых случаев СД на 31 %. Прием метформина приводил к снижению массы тела на 2 кг. В то время как МОЖ требовала значительно больших затрат — было проведено 16 занятий в первые 24 недели, а в группе метформина проводился только прием препарата. Комплайенс данной группы был сравним с таковым группы плацебо по причине хорошей переносимости метформина. Хорошая переносимость метформина — достаточное преимущество данного препарата в сравнении с акарбозой. У молодых тучных людей (24–44 года) с пограничными показателями уровня глюкозы натощак (НГН) метформин, вероятно, был эффективнее МОЖ или даже равносилен по эффективности. Также у пробандов с индексом массы тела (ИМТ) ≥ 35 кг/м2 метформин был более эффективен, чем МОЖ. Имеются сведения из DPP–исследования о том, что протективный эффект метформина сохраняется длительное время после прекращения приема.
Вероятно, общий эффект метформина связан с его влиянием на массу тела, распределение жира, липидный профиль, ИР и свертывающую систему крови.
В любом случае эти данные вместе с результатами исследования UKPDS являются основанием для раннего назначения метформина в приведенных целевых группах.
Акарбоза
В исследовании STOP–NIDDМ изучалось влияние акарбозы как на манифестацию СД, так и на возможные кардиоваскулярные события. Пациенты в течение периода наблюдения принимали акарбозу в дозе 100 мг 3 раза в день или плацебо. В результате лечения акарбозой квота конверсии НТГ в явный СД снизилась на 25 % в сравнении с плацебо–группой. Также отмечается предположительное снижение массы тела. Следовательно, раннее назначение акарбозы в состоянии предупредить развитие СД 2–го типа. Важнейшим результатом этого исследования было доказательство того, что прием акарбозы снижает кардиоваскулярный риск на 49 % и количество случаев инфаркта миокарда — на 91 %.
Орлистат
В исследовании XENDOS изучалось влияние приема орлистата на манифестацию СД в сравнении с плацебо, а также с группой МОЖ. Риск развития СД 2–го типа в группе, принимавшей орлистат + МОЖ, был на 37 % ниже, чем у тех, кто только модифицировал образ жизни, что, вероятно, связано с достигнутым снижением массы тела. Потеря массы тела была максимальной на первом году наблюдения. Потенциал орлистата как превентивного препарата связан в значительной степени со снижением массы тела, в то время как влияние метформина и акарбозы связано со снижением ИР и гиперинсулинемии.
Глитазоны
В исследовании TRIPOD 235 женщин с ранним диабетом беременных получали троглитазон или плацебо. После периода наблюдения в среднем 30 месяцев частота конверсии НТГ в явный СД составила 5,4 % в плацебо–группе против 2,3 % в группе, принимавшей троглитазон (снижение относительного риска на 56 %). Особый интерес представляет сохранение превентивного эффекта в течение 8 месяцев после прекращения приема препарата. В результате этих наблюдений обсуждается вопрос о том, что глитазоны могут влиять на эволюцию НТГ.
В мультицентровом исследовании DREAM изу–чалось влияние розиглитазона и рамиприла у лиц с НТГ на риск развития СД и кардиоваскулярных событий.
Натеглинид
В 2010 году на 46–м конгрессе Европейской ассоциации изучения СД были представлены результаты масштабного исследования NAVIGATOR, в котором пытались с помощью длительного приема (в течение 5 лет) натеглинида и валсартана добиться снижения риска кардиоваскулярных событий и манифестации СД у лиц с НТГ. К сожалению, эти препараты не продемонстрировали способности предотвращать развитие кардиоваскулярных событий у лиц высокого риска. Что касается профилактики СД 2–го типа, то длительный прием натеглинида не влиял на риск развития этого заболевания, а терапия валсартаном лишь незначительно снижала его. Так, применение валсартана в течение пяти лет позволило предотвратить развитие манифестации СД 2–го типа у 38 пациентов из 1000. Следовательно, на сегодняшний день можно сделать вывод, что прием валсартана с целью профилактики СД 2–го типа является нецелесообразным.
Отдаленные результаты проспективных исследований по профилактике СД 2–го типа
В 2010 г. в Новом Орлеане (США) на одном из симпозиумов конгресса Американской диабетической ассоциации избирательно были представлены отдельные результаты проспективных исследований по профилактике СД 2–го типа.
Китайское превентивное исследование (DQDPS)
Активные интервенционные мероприятия проводились в течение 6 лет — до 1992 г. В 2006 г. участники исследования были повторно обследованы с целью документации отдельных результатов проведенных интервенций. Из 577 пациентов с НТГ остались живы 435 (74 %), а умерли 142 (25 %). СД диагностирован у 98 % пациентов, ретинопатия — у 94 %, нефропатия — у 84 %, сердечно–сосудистые заболевания — у 94 %. Однако в группе лиц с комбинированной МОЖ (диетотерапия + увеличение двигательной активности) частота развития СД 2–го типа была на 51 % ниже в сравнении с контрольной группой (р < 0,05) в период активной интервенции и на 43 % ниже в течение 20–летнего периода наблюдения. Средняя годовая квота конверсии НТГ в явный СД составила в интервенционной группе 7 %, в контрольной группе — 11 %, с кумулятивной частотой 80 % в опытной группе и 93 % в контрольной группе. В группе с интервенцией продолжительность СД в среднем была на 3,6 года меньше, чем у лиц контрольной группы. Не было достоверного различия между опытной и контрольной группой относительно сердечно–сосудистых заболеваний, кардиоваскулярной и общей смертности.
Авторы пришли к заключению, что активная интервенция (то есть МОЖ) в течение 6 лет может предотвратить развитие СД 2–го типа и этот эффект может сохраниться даже спустя 14 лет после прекращения МОЖ. Что касается вопроса о способности МОЖ дополнительно предупреждать развитие сердечно–сосудистых заболеваний, то все зависит от вида осложнения: риск ретинопатии снизился на 47 %, в то же время не отмечено влияния на риск развития нейропатии и нефропатии. Может ли МОЖ привести к уменьшению риска сердечно–сосудистых заболеваний и смертности, до сих пор остается неясным. Отмечено недостоверное снижение сердечно–сосудистой смертности, однако влияния на общую смертность не установлено.
Финское превентивное исследование (DPS)
В этом исследовании изучалось влияние МОЖ в качестве превентивных мероприятий у лиц с высоким риском развития СД. Пациенты были рандомизированы на 2 группы: группа интенсивной МОЖ и контрольная группа. Средняя продолжительность наблюдения составила около 4 лет, и средний период после завершения исследования — 10,6 года [12].
Сравнение опытной (n = 505) и контрольной группы в отношении общей (2,2 против 3,8 на 1000 человеко–лет) и кардиоваскулярной смертности (22,9 против 22,0 на 1000 человеко–лет) не выявило достоверных различий. Сравнение общей и кардиоваскулярной смертности референтной группы с данными опытной и контрольной группы исследуемых в рамках DPS не выявило различий.
Резюмируя вышеизложенное, авторы приходят к заключению, что МОЖ у лиц с НТГ не приводит к снижению кардиоваскулярной смертности в первые 10 лет наблюдения после завершения интервенции. Данные статистические различия недостаточно убедительны, так как различия между опытной и контрольной группой были незначительными. Более низкую общую смертность в референтной группе можно связать с более благоприятным кардиоваскулярным риском у лиц опытной группы к моменту завершения интервенции. Значительный успех этого исследования базировался на высокой мотивации участников, что проявилось низкой долей отказа от интервенции (6 % в первые два года наблюдения). Продолжительная МОЖ (рациональное питание плюс увеличение двигательной активности), вероятно, достаточна для снижения риска развития СД 2–го типа у лиц с высоким риском, и она должна стать краеугольным камнем профилактики СД 2–го типа.
Американское превентивное исследование (DPPOS)
В начале в DPP–исследовании приняли участие 3819 лиц с НТГ из 27 центров США, которые были рандомизированы на 4 группы:
1. Группа интенсивной МОЖ (опытная группа).
2. Группа стандартной МОЖ + плацебо.
3. Группа стандартной МОЖ + метформин.
4. Группа стандартной МОЖ + троглитазон.
В 1998 году лечение троглитазоном было прекращено из–за летального поражения печени у 1 участника исследования, а участники этой ветви переведены в другие группы наблюдения.
Интервенция продолжалась 3 года и была прекращена ввиду явных доказательств пользы интенсивной МОЖ.
В 2002–2003 гг. проведен анализ отдельных результатов интенсивной МОЖ и медикаментозной терапии метформином после интервенции 1996–1998 гг. относительно частоты развития СД 2–го типа, сердечно–сосудистых осложнений и смертности. Одномоментно обследовано 3104 пациента из 27 центров США, что составило 82 % от участников оригинальной группы DPP [13].
Установлено, что динамика массы тела в группе интенсивной МОЖ была сопоставима с таковой группы метформина. Масса тела в группе интенсивной МОЖ была еще на 2,5 кг ниже, чем в плацебо–группе. Этот эффект, наряду с известными факторами (рациональное питание, увеличение двигательной активности), связан дополнительно с изменением поведения и снижением уровня стресса. Наиболее правильным и здоровым способом снижения калорийности пищи является уменьшение содержания жира в рационе.
Практические рекомендации, вытекающие из анализа отдельных результатов превентивных исследований
На основании анализа отдельных результатов проведенных исследований можно сделать следующие выводы и сформировать практические рекомендации:
1. Интервенция в виде интенсивной МОЖ требует очень квалифицированного персонала, чтобы учитывать индивидуальные проблемы пациентов.
2. Для закрепления МОЖ требуется постоянное наблюдение, чтобы гарантировать сохранение достигнутых результатов. Примерно 50 % участников исследования достигли 7% снижения массы тела в течение шести месяцев. Успеха можно достичь в разных популяциях — главным условием является высокая мотивация пациентов.
3. Предикторами снижения массы тела являются пожилой возраст, увеличение двигательной активности, правильное представление о питании.
К завершению DPP–исследования целевых показателей достигли 37 % пациентов. Возраст свыше 66 лет был сильнейшим предиктором снижения массы тела.
К предикторам сохранения сниженной массы тела относятся:
— ограничение калорийности пищи и снижение содержания жира в рационе;
— ежедневная двигательная активность — минимум 1 час;
— постоянный контроль массы тела;
— многократный прием пищи (4–5 раз в день), включая обязательный завтрак.
Только некоторые превентивные исследования фокусировали свое внимание на предотвращении повторного набора массы. По мнению исследователей, в программе превентивных исследований необходимо обязательно интегрировать предикторы длительного поддержания сниженной массы тела.
В 2018 г. конгресс Европейской ассоциации по изучению диабета открылся лекцией Клода Бернара «Профилактика СД 2–го типа — мечта, которая осуществилась», которую прочитал Я. Туомилето, исследователь из Финляндии. Эта лекция стала лозунгом конгресса EASD. Основные тезисы этой лекции сводятся к следующему.
Я. Туомилето показал, что после выявления предпосылок для развития СД профилактика должна проводиться на протяжении 10–12 лет, пока бета–клетки поджелудочной железы функционально активны [14]. Очень важным условием профилактики СД 2–го типа является возможность идентификации периода риска, то есть предиабета. Для его идентификации рекомендуется определение уровня глюкозы натощак, проведение орального ТТГ. Показатель гликированного гемоглобина, по его мнению, недостаточно чувствителен. Два важнейших исследования — DPS и DPP — показали, что снижение массы тела, рациональное питание и модификация образа жизни существенно снижают риск развития СД 2–го типа. К группе людей, которые должны обратить внимание на свой образ жизни, относятся:
— лица с генетической предрасположенностью к развитию СД 2–го типа;
— пациенты с идентифицированным предиабетом (нарушение гликемии натощак и нарушение толерантности к глюкозе);
— люди с избыточным весом и ожирением.
Я. Туомилето пришел к заключению, что мечта о предотвращении СД в какой–то мере оправдалась. Установлено 5 целевых показателей, достижение которых позволит приостановить развитие СД 2–го типа. К ним относятся:
— потеря массы тела 5 % и более;
— уменьшение потребления жиров < 30 % от суточного;
— уменьшение потребления насыщенных жиров < 10 %;
— содержание клетчатки в пище не менее 15 г на 1000 ккал рациона;
— минимальный уровень физической нагрузки 30 минут в день.
При достижении всех пяти целевых показателей ни одного случая развития СД 2–го типа не наблюдалось.
Конфликт интересов. Авторы заявляют об отсутствии какого–либо конфликта интересов при подготовке данной статьи.

/180-1.jpg)