Газета «Новости медицины и фармации» Кардиология (314) 2010 (тематический номер)
Вернуться к номеру
Сучасні підходи до ведення пацієнтів після реваскуляризації міокарда
27 січня в Президент-готелі «Київський» відбулася конференція, присвячена сучасним можливостям лікування ішемічної хвороби серця та реваскуляризації міокарда.
У конференції взяли участь: директор Київського міського центру серця, доктор медичних наук, професор Б.М. Тодуров з доповіддю, у якій викладено погляд кардіохірурга на проблему стенокардії та представлено власний досвід хірургічного лікування таких пацієнтів;
завідувач відділу атеросклерозу та хронічної ІХС ННЦ «Інститут кардіології ім. М.Д. Стражеска», доктор медичних наук, професор М.І. Лутай, доповідь якого було присвячено сучасним підходам до ведення пацієнтів, які перенесли операцію реваскуляризації;
професор кафедри кардіології та функціональної діагностики НМАПО ім. П.Л. Шупика О.Й. Жарінов із доповіддю «Сучасне лікування стенокардії. Роль селективного зниження ЧСС».
 Конференцію відкрив директор Київського міського центру серця, доктор медичних наук, професор Б.М. Тодуров. Він відзначив, що тема ведення пацієнтів після операцій реваскуляризації міокарда зберігає свою актуальність у зв''язку із більш широким застосуванням сучасних інтервенційних технологій: методів АКШ й стентування в кардіохірургії. Прогноз пацієнта, який переніс реваскуляризацію міокарда, здебільшого залежить не лише від успішного виконання втручання, а й від подальшої стратегії медикаментозної терапії. Застосування оптимальної медикаментозної терапії дає змогу подовжити тривалість життя й поліпшити його якість, запобігти повторним інфарктам міокарда й покращити віддалений прогноз. Це пов''язано із неминучим під час втручання механічним ушкодженням коронарних артерій, яке супроводжується високим ризиком повторного порушення кровопостачання міокарда, що призводить до виснаження компенсаторних резервів міокарда і завершується розвитком дилатаційної серцевої недостатності. У даній ситуації єдиним радикальним методом переривання зачарованого кола є кардіохірургічне оперативне втручання. Це не лише добре відоме аортокоронарне шунтування, але й різні види хірургічного ремоделювання лівого шлуночка і його структур (клапанний і підклапанний апарат). У таких складних клінічних випадках, частота яких сягає до 30 %, головною складовою успішного лікування є взаєморозуміння і спадкоємність лікаря-кардіолога і кардіохірурга. Необхідне також і своєчасне визначення та прийняття концепції лікування для профілактики тяжких і часто необоротних ускладнень. Певні кроки на цьому шляху вже зроблено.
Конференцію відкрив директор Київського міського центру серця, доктор медичних наук, професор Б.М. Тодуров. Він відзначив, що тема ведення пацієнтів після операцій реваскуляризації міокарда зберігає свою актуальність у зв''язку із більш широким застосуванням сучасних інтервенційних технологій: методів АКШ й стентування в кардіохірургії. Прогноз пацієнта, який переніс реваскуляризацію міокарда, здебільшого залежить не лише від успішного виконання втручання, а й від подальшої стратегії медикаментозної терапії. Застосування оптимальної медикаментозної терапії дає змогу подовжити тривалість життя й поліпшити його якість, запобігти повторним інфарктам міокарда й покращити віддалений прогноз. Це пов''язано із неминучим під час втручання механічним ушкодженням коронарних артерій, яке супроводжується високим ризиком повторного порушення кровопостачання міокарда, що призводить до виснаження компенсаторних резервів міокарда і завершується розвитком дилатаційної серцевої недостатності. У даній ситуації єдиним радикальним методом переривання зачарованого кола є кардіохірургічне оперативне втручання. Це не лише добре відоме аортокоронарне шунтування, але й різні види хірургічного ремоделювання лівого шлуночка і його структур (клапанний і підклапанний апарат). У таких складних клінічних випадках, частота яких сягає до 30 %, головною складовою успішного лікування є взаєморозуміння і спадкоємність лікаря-кардіолога і кардіохірурга. Необхідне також і своєчасне визначення та прийняття концепції лікування для профілактики тяжких і часто необоротних ускладнень. Певні кроки на цьому шляху вже зроблено.
Сьогодні на базі Київського міського центру серця виконуються такі втручання, як стентування коронарних артерій, шунтування серця, протезування клапанів серця з використанням передових технологій.
 Із доповіддю «Тактика ведення пацієнтів з ІХС після реваскуляризації міокарда» виступив доктор медичних наук, професор М.І. Лутай.
Із доповіддю «Тактика ведення пацієнтів з ІХС після реваскуляризації міокарда» виступив доктор медичних наук, професор М.І. Лутай.
Реваскуляризація міокарда (стентування, аортокоронарне шунтування) істотно покращує якість життя пацієнтів з ішемічною хворобою серця (ІХС), усуваючи або значно зменшуючи кількість ангінозних нападів. Аортокоронарне шунтування також позитивно впливає на прогноз захворювання, але це стосується лише пацієнтів із найбільш високим ризи-
ком — зі стенозом стовбура ЛКА, трисудинним ураженням коронарних артерій, низькою фракцією викиду лівого шлуночка (ЛШ), із супутнім цукровим діабетом. Хірургічна або ендоваскулярная реваскуляризації міокарда не сприяє повному одужанню хворих, тому що не усувається основна причина ІХС — коронарний атеросклероз.
Таким чином, тактика ведення хворих, яким проводилась реваскуляризація міокарда, за винятком пацієнтів з установленими елютинг-стентами, які потребують обов''язкового проведення подвійної антитромбоцитарної терапії (аспірин + клопідогрель) із метою попередження пізніх тромбозів у стенті, принципово не відрізняється від такої у пацієнтів з ІХС без хірургічних або інтервенційних втручань.
При проведенні опитування на стенді фірми «Серв''є» (Франція) лікарів, які брали участь у Х Національному конгресі кардіологів України (2009 р.), на питання, які, на їх погляд, існують особливості ведення пацієнтів з ІХС, що перенесли операцію реваскуляризації, були отримані такі відповіді (рис. 1).


Отже, тільки трохи більше ніж половина лікарів правильно відповіли на поставлене запитання.
Щорічний ризик серцево-судинної смертності у хворих після реваскуляризації, за даними Європейського реєстру, в середньому становить 3,7 %, тому, незважаючи на проведене втручання, такі пацієнти належать до групи високого ризику й потребують подальшої медикаментозної терапії.
Загальновідомо, що позитивно впливають на прогноз ІХС, у тому числі й у пацієнтів, які пройшли реваскуляризацію міокарда, наступні групи препаратів: антитромбоцитарні (аспірин, клопідогрель), ліпідознижуючі (статини), інгібітори ангіотензинперетворюючого ферменту (АПФ) (раміприл, периндоприл), бета-адреноблокатори (без внутрішньої симпатоміметичної активності). Оскільки більшість серцево-судинних ускладнень пов''язані з процесом атеротромбозу, в першу чергу необхідно приділити увагу якості проведеної терапії препаратами, які впливають на функцію ендотелію та викликають стабілізацію атероматозної бляшки, запобігають тромбоутворенню.
Принципи ведення пацієнтів з ІХС після реваскуляризації міокарда на підставі даних доказової медицини
Ліпідознижуюча терапія
Мета: холестерин ліпопротеїдів низької щільності (ХС ЛПНЩ) нижче ніж 100 мг/дл; (якщо тригліцериди (ТГ) ≥ 200 мг/дл, рівень холестерину ліпопротеїдів високої щільності (ХС ЛПВЩ) не повинен бути нижчим за 130 мг/дл).
1. Рекомендовано починати з дієтотерапії — зменшення в раціоні легкорозчинних жирів (менше ніж 7 % від загального калоражу продуктів), жирних кислот і холестерину (менше ніж 200 мг/день) (IB).
2. Додавання рослинних станолів/стеролів (2 г/день) і/або клітковини (понад 10 г/день) з метою подальшого зниження ХС ЛПНЩ (IIа А).
3. Рекомендовані щоденна фізична активність і контроль маси тіла (IB).
4. Може бути ефективним підвищення вмісту ω-3-жирних кислот у вигляді морської риби або капсул (1 г/день) (?) для зниження ризику; для зниження ризику при високих рівнях тригліцеридів звичайно необхідні більш високі дози (IIb B).
Всім пацієнтам з ІХС необхідний систематичний моніторинг ліпідного профілю й повинна призначатися ліпідознижуюча терапія відповідно до нижчезазначеної схеми:
Може бути корисна терапія препаратами нікотинової кислоти (ніацин) та фібратами (фенофібрат).
Антитромбоцитарні препарати. Аспірин
1. Усім пацієнтам після черезшкірної транслюмінальної коронарної ангіопластики (ЧТКА) та стентування, у яких немає алергії й підвищеного ризику кровотеч, аспірин у дозі 162–325 мг/день повинен бути призначений протягом мінімум одного місяця після імплантації BMS-стентів, 3 місяців після імплантації sirolimus-елютинг-стентів і 6 місяців після імплантації paclitaxel-елютинг-стентів, після чого рекомендується подальший довгостроковий щоденний прийом аспірину в дозі 75–162 мг/доба (IB).
2. Пацієнтам із високим ризиком кровотеч прийом низьких доз аспірину 75–162 мг/день обгрунтований протягом початкового періоду після імплантації стентів (IIа С).
Антитромбоцитарні препарати. Клопідогрель
1. Усім пацієнтам з установленими DES клопідогрель призначається щодня в добовій дозі 75 мг протягом принаймні 12 місяців, якщо пацієнти не мають високого ризику кровотеч. Пацієнтам з встановленими BMS клопідогрель повинен бути призначений на строк мінімум 1 місяць (ідеально до 12 місяців). Якщо пацієнт належить до групи високого ризику кровотеч, препарат призначається мінімум на 2 тижні (IB).
2. Усім пацієнтам після проведення ЧТКА без стентування клопідогрель повинен призначатися протягом як мінімум 14 днів (IB).
3. Довгострокова підтримуюча терапія (1 рік) клопідогрелем у дозі 75 мг/день краща для всіх пацієнтів (STEMI і non-STEMI), яким виконана ЧТКА без реперфузійної терапії (IIа С).
Антикоагулянти. Варфарин
1. Титрування варфарину до INR від 2 до 3 показане при миготінні або тріпотінні передсердь, а також у пацієнтів, які перенесли інфаркт міокарда (ІМ), за наявності клінічних показань (фібриляція передсердь, тромб у лівому шлуночку) (IА).
2. Використання варфарину в поєднанні з аспірином/клопідогрелем асоціюється з підвищенням ризику кровотеч і повинне строго контролюватися (IB).
3. У пацієнтів, які потребують терапії варфарином, клопідогрелем і аспірином після проведення ЧТКА, рекомендований INR від 2 до 2,5 при низьких дозах аспірину (75–81 мг) і клопідогрелю (75 мг) (IС).
Інгібітори АПФ
1. Інгібітори АПФ повинні бути призначені та прийматися невизначено довго всіма пацієнтами із ФВ лівого шлуночка ≤ 40 %, а також за наявності артеріальної гіпертензії, цукрового діабету, захворювань нирок, за відсутності протипоказань (IA).
2. Інгібітори АПФ повинні бути призначені та прийматися невизначено довго всіма пацієнтами, у яких ризик не оцінений як «низький» (низьким вважається ризик у пацієнтів з нормальною ФВ, контрольованими факторами ризику й проведеною реваскуляризацією) за відсутності протипоказань (IB).
3. У пацієнтів із низьким ризиком (з нормальною ФВ, контрольованими факторами ризику та проведеною реваскуляризацією) призначення інгібіторів АПФ є бажаним (IIa B).
Стосовно застосування інгібіторів АПФ варто підкреслити наступне.
У дослідженні EUROPA доведено, що призначення периндоприлу (Престаріум) достовірно знижує ризик розвитку серцево-судинних ускладнень в середньому на 17,3 % (р < 0,036) у групі хворих, які пройшли реваскуляризацію міокарда (АКШ — 3132 особи, ЧТКА — 3122 особи), з нормальною фракцією викиду ЛШ і контрольованими факторами ризику. Такі інгібітори АПФ, як квінаприл (дослідження QUIET і IMAGINE) і трандолаприл (PEACE), не продемонстрували переваг призначення зазначених препаратів у пацієнтів, які пройшли реваскуляризацію міокарда.
Таким чином, ефективність впливу на прогноз ІХС у хворих, яким проводили реваскуляризацію міокарда, у різних представників інгібіторів АПФ не однакова.
І сьогодні, враховуючи доказову базу досліджень, ми можемо рекомендувати таким пацієнтам призначення периндоприлу.
Одним із пояснень високої ефективності периндоприлу у зниженні ризику коронарних подій є його здатність зменшувати прогресування атеросклерозу. Вплив препарату на ремоделювання коронарних артерій у пацієнтів зі стабільною ішемічною хворобою серця вивчався у дослідженні PERSPECTIVE (PERindopril''S Prospective Effect on Coronary aTherosclerosis by angiographical and intravascular ultrasound Evaluation) за участю 118 хворих, яким на початку дослідження й через 3 роки було проведено внутрішньосудинне ультразвукове дослідження коронарних артерій. У результаті дослідження було виявлено достовірне зменшення площі атеросклеротичного ураження у групі хворих, які приймали периндоприл (рис. 2).
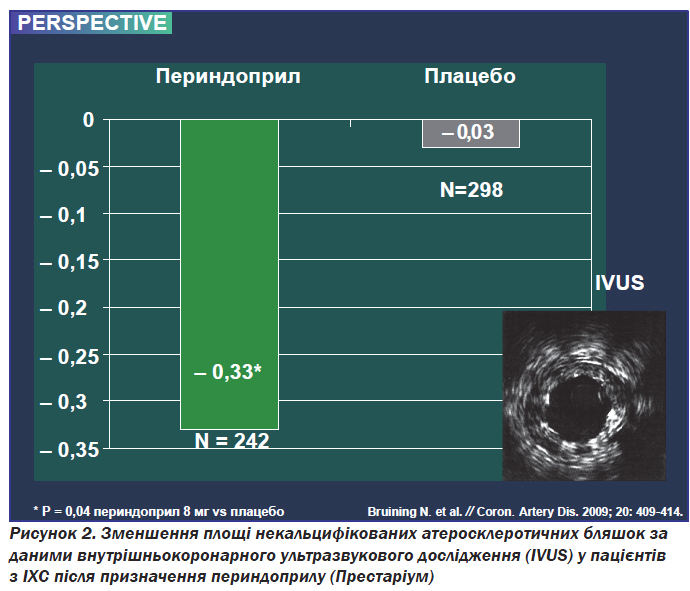
Бета-адреноблокатори
1. Бета-блокатори повинні бути призначені та прийматися невизначено довго всіма пацієнтами з перенесеними ІМ, ГКС або дисфункцією ЛШ із симптомами СН або без них за умов відсутності протипоказань (IА).
2. Бажано призначати довгострокову терапію всім пацієнтам з ІХС і/або іншими судинними захворюваннями, цукровим діабетом за умов відсутності протипоказань (IIa C).
Вакцинація від грипу
1. Пацієнти з серцево-судинними захворюваннями повинні проходити щорічну вакцинацію проти грипу (IB).
 Із доповіддю «Сучасне лікування стенокардії. Роль селективного зниження ЧСС» виступив професор кафедри кардіології та функціональної діагностики НМАПО ім. П.Л. Шупика Олег Йосипович Жарінов.
Із доповіддю «Сучасне лікування стенокардії. Роль селективного зниження ЧСС» виступив професор кафедри кардіології та функціональної діагностики НМАПО ім. П.Л. Шупика Олег Йосипович Жарінов.
Сьогодні лікар має чотири мішені для лікування ІХС: першою і основною є вплив на співвідношення потреби та постачання О2 у міокард через регуляцію тонусу коронарних судин із застосуванням класичних препаратів — нітратів, β-адреноблокаторів, антагоністів кальцію. Нині цей перелік розширений з появою нового кардіологічного препарату івабрадину, а також можливостями реваскуляризації міокарда. Другою мішенню є вплив на агрегацію тромбоцитів із застосуванням АСК, тиклопідину й клопідогрелю. Третьою мішенню є вплив на стан судинної стінки та гальмування прогресування атеросклерозу, а також вплив на рівень ліпідів, із яким дуже тісно корелюють можливості гальмування прогресування атеросклерозу — застосування статинів та інгібіторів АПФ. Четвертою мішенню є вплив на метаболізм кардіоміоцитів і потенційні можливості цитопротекції (триметазидин і ранолазин).
Таким чином, нині є чудовий квартет для лікування ІХС, який складається з антитромбоцитарного препарату, β-адреноблокатора, інгібітору АПФ, статину. Доповненням до цього квартету є івабрадин. Цей інноваційний препарат відкриває принципово нові можливості у лікуванні ІХС. Доказова база цього препарату постійно поповнюється. На двох останніх європейських конгресах кардіологів подані основні досягнення у вивченні фармакологічних властивостей івабрадину.
У Фремінгемському дослідженні на основі оцінки частоти серцевих скорочень (ЧСС) під час лікарського огляду пацієнтів, як здорових, так і з артеріальною гіпертензією та ішемічною хворобою серця, продемонстрована пряма кореляція між підвищенням показника ЧСС і ризиком раптової смерті від ІХС у чоловіків. У жінок на той час таких переконливих даних не було отримано.
У масштабному подвійному сліпому плацебо-контрольованому дослідженні BEAUTIFUL було уточнено показник ЧСС, при якому зростає ризик смерті, — понад 70 уд/хв. Тобто саме показник ЧСС — 70 уд/хв асоціюється з підвищеним ризиком серцево-судинних подій, і саме за підвищення ЧСС до такого показника виникає потреба в його зниженні. Традиційно з метою зменшення ЧСС у пацієнтів з ІХС, особливо після інфаркту міокарда, широко використовують β-адреноблокатори. Найбільш ефективними є β-адреноблокатори без внутрішньої симпатоміметичної активності, які дозволяють покращити перспективу виживання хворих.
Незважаючи на об''єктивні переваги застосування β-адреноблокаторів, на практиці з їх допомогою не завжди вдається досягти цільових рівнів ЧСС. В першу чергу це пов''язано з необхідністю обмеження дози цих препаратів, насамперед через ризик розвитку синдрому відміни в подальшому. Окрім ризику розвитку брадикардії, об''єктивними причинами обмеження дози β-адреноблокаторів, за даними дослідження MERIT-HF (2002), є артеріальна гіпотензія та посилення проявів ХСН.
Альтернативним засобом, здатним сповільнювати ЧСС, є препарат івабрадин (Кораксан), його вплив на ЧСС пояснюється здатністю селективно та специфічно зв''язуватися з If-каналами міоцитів синусового вузла, дозозалежно пригнічуючи їх. Завдяки такій дії збільшується тривалість діастоли і покращується коронарне кровонаповнення. На відміну від β-адреноблокаторів, івабрадин не погіршує ізоволюмічне розслаблення лівого шлуночка (P. Colin et al., 2002). Зниження ЧСС забезпечується як у стані спокою, так і під час фізичного навантаження.
В Україні перше дослідження препарату івабрадин було проведено на базі ННЦ «Інститут кардіології ім. М.Д. Стражеска» під керівництвом професора М.І. Лутая (2008). Це дослідження CROSS, у якому взяли участь пацієнти із стенокардією ІІ–ІІІ функціонального класу, продемонструвало зниження ЧСС на 15,8 і 21,8 % через 1 і 3 місяці із досягненням у 62,6 % хворих цільової ЧСС — 55–60 уд/хв.
На цьому фоні відзначалось вірогідне зниження (на 88 %) частоти нападів стенокардії і, що не менш важливо, на 90 % зменшувалася потреба в застосуванні засобів зняття ангінозних нападів — нітратів.
У дослідженні BEAUTIFUL взяли участь пацієнти з ІХС, що поєднувалася з систолічною дисфункцією лівого шлуночка (фракція викиду менше 40 %). Одним із критеріїв включення в це дослідження було проведення в минулому процедури реваскуляризації, а також показник ЧСС понад 60 уд/хв. Первинний вихід дослідження включав загальну кількість ускладнень, серцево-судинну смертність, інфаркт міокарда, серцеву недостатність, а також частоту госпіталізацій з приводу фатального або нефатального інфаркту міокарда. У загальній популяції пацієнтів івабардин не продемонстрував суттєвого зниження сумарної кількості випадків смерті від серцево-судинних причин, госпіталізацій з приводу гострого інфаркту міокарда або серцевої недостатності. Однак попередньо запланований аналіз показав, що у пацієнтів з ЧСС понад 70 уд/хв більше ніж на третину зменшилась кількість госпіталізацій, пов''язаних з гострим інфарктом міокарда. Суттєво зменшувалася також потреба в проведенні реваскуляризацій міокарда.
У 2009 році на Європейському конгресі кардіологів було оприлюднено дані субаналізу, проведеного у 1507 пацієнтів зі стенокардією (рис. 3). Половина з них (734 пацієнти) отримувала івабрадин, інші 773 включені в групу плацебо. При порівнянні підгрупи пацієнтів зі стенокардією і всіх учасників дослідження BEAUTIFUL було показано, що в підгрупі пацієнтів зі стенокардією було менше пацієнтів, які в минулому перенесли операцію реваскуляризації (30 %), ніж в усіх учасників дослідження (50 %). Ще один аспект полягав у тому, що в підгрупі пацієнтів зі стенокардією переважали хворі з клінічними ознаками ХСН (NYHA II).
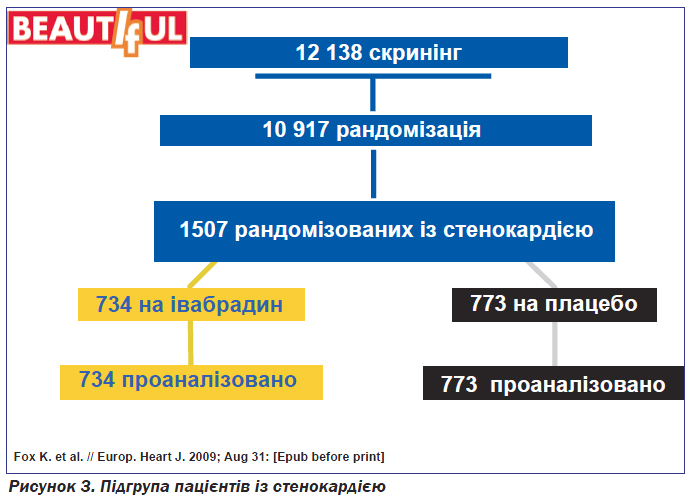
Результати дослідження показали, що у групі пацієнтів із стенокардією, які отримували івабрадин, було досягнуто зменшення первинної кінцевої точки, що включала серцево-судинну смерть, інфаркт міокарда, серцеву недостатність, на 24 % (рис. 4), а частота госпіталізації з приводу гострого інфаркту міокарда зменшилась на 42 % (рис. 5).
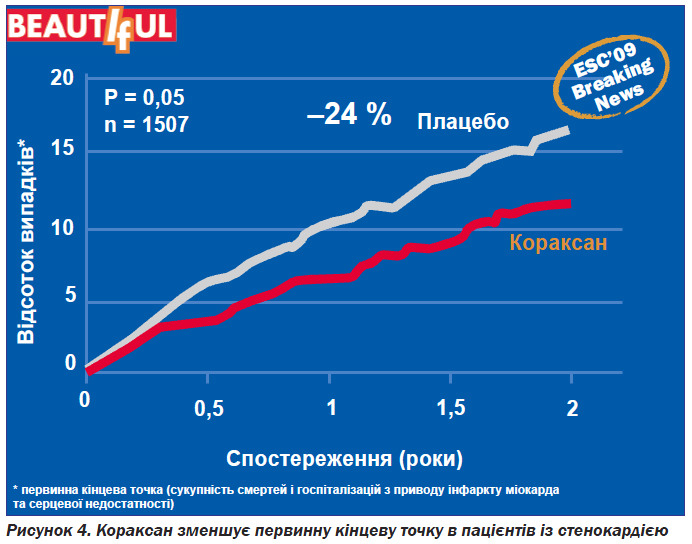
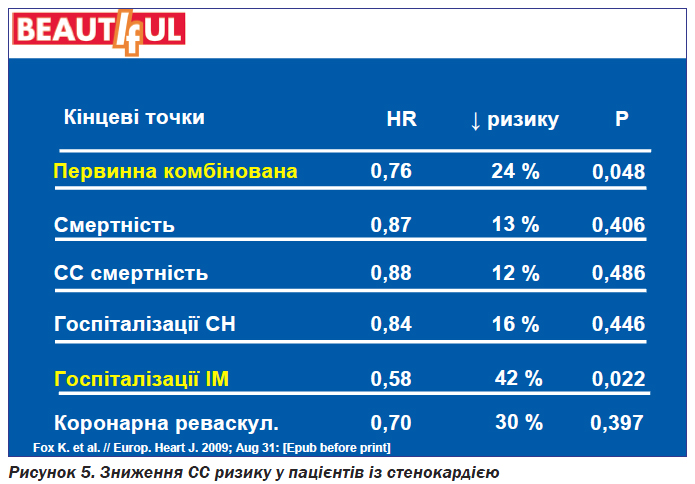
Тоді як у пацієнтів із стенокардією і збільшеною ЧСС понад 70 уд/хв досягнуто зниження первинної комбінованої точки на 31 %, показника смертності — на 17 %, частоти госпіталізації з приводу гострого інфаркту міокарда — на 73 %.
Обговорюючи питання профілактики серцево-судинних подій у пацієнтів із стенокардією та впливу основних медикаментозних засобів на прогноз виживання пацієнтів, варто зазначити, що більшість існуючих засобів усунення нападів стенокардії (покращення якості життя) не виявили в контрольованих дослідженнях здатності запобігати серцево-судинним подіям. З іншого боку, базисні засоби лікування ІХС (ацетилсаліцилова кислота і статини) не мають безпосередньої антиангінальної дії і переважно застосовуються з міркувань покращення прогнозу виживання хворих.
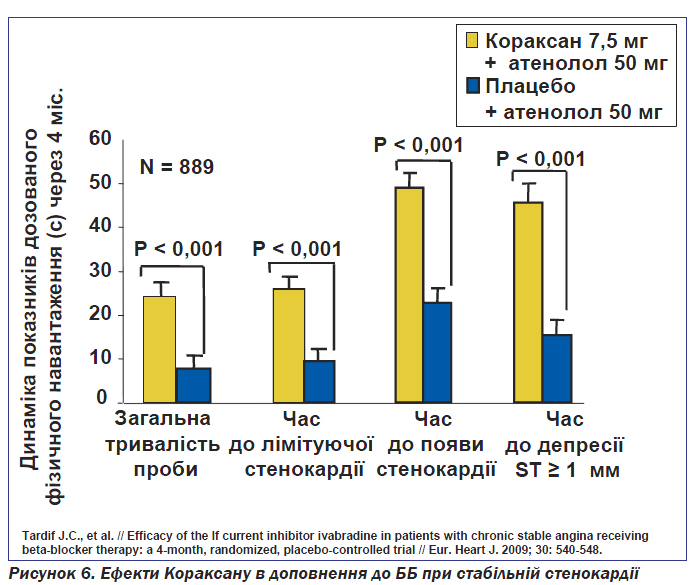

На цей час можна вважати, що у пацієнтів із підтвердженою ішемією міокарда івабрадин (Кораксан) є єдиним препаратом, який поєднує антиангінальний ефект та захист від інфаркту міокарда. Важливим є те, що івабрадин покращує прогноз у пацієнтів із стабільною стенокардією і зниженою фракцією викиду лівого шлуночка, особливо коли ЧСС перевищує 70 уд/хв. Івабрадин довів можливість покращення прогнозу навіть у пацієнтів, які приймають β-адреноблокатори (рис. 6). На сьогодні івабрадин є новим стандартом антиангінальної терапії — альтернативою або доповненням до терапії β-адреноблокаторами для досягнення цільової ЧСС і поліпшення прогнозу у пацієнтів зі стабільною стенокардією.
Підготувала Галина Бут
