Журнал «Здоровье ребенка» Том 19, №5, 2024
Вернуться к номеру
Ефективність застосування спрею з наночастинками срібла у лікуванні гострого фарингіту
Авторы: Няньковський С.Л., Яцула М.С., Городиловська М.І.
Львівський національний медичний університет імені Данила Галицького, м. Львів, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
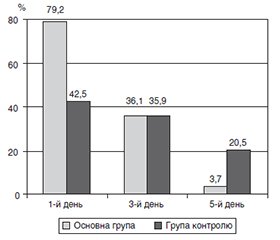
Оцінено ефективність застосування Бріомосс Сільвер спрею у комплексному лікуванні гострого фарингіту та тонзилофарингіту у пацієнтів віком від 6 років. Під спостереженням перебувало 2636 пацієнтів віком від 6 років, 2363 з яких додатково до стандартної терапії застосовували Бріомосс Сільвер спрей (основна група) і 273 не використовували медичний виріб (контрольна група). Аналіз отриманих результатів показав, що до 5-го дня лікування частка пацієнтів без болю в горлі в основній групі зросла до 76,9 % порівняно з 34,1 % у контрольній (p < 0,01). Зниження кількості пацієнтів із зернистістю задньої стінки глотки на 3-й день становило 2,2 раза в основній групі і 1,2 раза в групі контролю (p < 0,01). На 5-й день зернистість зберігалася у 3,7 та 20,5 % пацієнтів відповідно (p < 0,01). Частка хворих із вираженою гіперемією знизилась відповідно на 81,4 та 26,9 % на 3-й день терапії. До 5-го дня почервоніння не реєстрували вже у 83,6 % пацієнтів основної групи та лише у 45,2 % пацієнтів групи контролю (p < 0,01). Частота виявлення нальоту на 3-й день зменшилася порівняно з початком лікування у 2,5 раза в основній групі та в 1,8 раза в групі контролю (p < 0,01). При огляді на 5-й день лікування нальоту не спостерігали у жодного пацієнта. Побічних реакцій не зареєстровано. Додаткове застосування Бріомосс Сільвер спрею сприяло вірогідно швидшому зникненню суб’єктивних симптомів (інтенсивність болю) та об’єктивних ознак (гіперемія задньої стінки глотки, її зернистість, наліт) захворювання, навіть незважаючи на початково більш тяжкий стан пацієнтів основної групи. Таким чином, Бріомосс Сільвер спрей підвищує ефективність терапії інфекційно-запальних захворювань глотки та мигдаликів. Його використання може значно поліпшити результати терапії, особливо в умовах підвищеної стійкості мікроорганізмів до традиційних антибактеріальних засобів.
The effectiveness of Briomoss Silver Spray was evaluated in the combined treatment of acute pharyngitis and tonsillopharyngitis in patients aged 6 years and older. A total of 2636 patients aged 6 years and above were monitored, with 2363 of them receiving Briomoss Silver Spray in addition to standard therapy (the main group), and 273 not using this medical product (the control group). Analysis of the results showed that by the fifth day of treatment, the proportion of patients without sore throat increased to 76.9 % in the main group compared to 34.1 % in the control group (p < 0.01). The number of participants with granulations on the posterior pharyngeal wall reduced by 2.2 times on the third day in the main group and by 1.2 times in the control group (p < 0.01). On the fifth day, granulations persisted in 3.7 and 20.5 % of patients, respectively (p < 0.01). The proportion of patients with pronounced hyperemia decreased by 81.4 and 26.9 %, respectively, on the third day of therapy. By the fifth day, redness was no longer recorded in 83.6 % of cases in the main group and only 45.2 % of controls (p < 0.01). The frequency of detecting plaques on the third day decreased compared to the baseline by 2.5 times in the main group and by 1.8 times in the control group (p < 0.01). Examination on the fifth day of treatment revealed no plaques in any of the patients. There were no adverse reactions. The additional use of Briomoss Silver Spray led to a significantly faster resolution of subjective symptoms (pain intensity) and objective signs (posterior pharyngeal wall hyperemia, granulations, plaques) of the disease, despite the initially more severe condition of patients in the main group. Thus, Briomoss Silver Spray enhances the effectiveness of therapy for infectious-inflammatory diseases of the throat and tonsils. Its use can significantly improve therapeutic outcomes, especially in the context of increased microorganism resistance to traditional antibacterial agents.
наночастинки срібла; Бріомосс Сільвер спрей; гострий фарингіт; гострий тонзилофарингіт; протимікробна дія
silver nanoparticles; Briomoss Silver Spray; acute pharyngitis; acute tonsillopharyngitis; antimicrobial activity
Вступ
Матеріали та методи
Результати та обговорення
/56.jpg)
/57.jpg)
/58.jpg)
/58_2.jpg)
Висновки
- Anderson J., Paterek E. Tonsillitis. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing. 2023. URL: https://www.ncbi.nlm.nih.gov/books/NB44342/
- Calò L., Passàli G.C., Galli J. et al. Role of biofilms in chronic inflammatory diseases of the upper airways. Adv. Otorhinolaryngol. 2011. Vol. 72. P. 93-96.
- Cavassin E.D., de Figueiredo L.F.P., Otoch J.P. et al. Comparison of methods to detect the in vitro activity of silver nanoparticles (AgNP) against multidrug resistant bacteria. J. Nanobiotechnol. 2015. Vol. 13. P. 1-16.
- Chen M., Shou Z., Jin X. et al. Emerging strategies in nanotechnology to treat respiratory tract infections: realizing current trends for future clinical perspectives. Drug Deliv. 2022. Vol. 29. № 1. P. 2442-2458.
- Dakal T.C., Kumar A., Majumdar R.S. et al. Mechanistic basis of antimicrobial actions of silver nanoparticles. Front. Microbiol. 2016. Vol. 7. P. 1831.
- Freysdottir J., Omarsdottir S., Ingólfsdóttir K. et al. In vitro and in vivo immunomodulating effects of traditionally prepared extract and purified compounds from Cetraria islandica. Int. Immunopharmacol. 2008. Vol. 8. № 3. P. 423-430.
- Gakiya-Teruya L., Palomino-Marcelo S., Pierce A.M. et al. Enhanced antimicrobial activity of silver nanoparticles conjugated with synthetic peptide by click chemistry. J. Nanopart. Res. 2020. Vol. 22. № 4. P. 1-11.
- Hussain F., Abro N., Khan N. et al. Nano-antivirals: A comprehensive review. Frontiers in Nanotechnology. 2022. Vol. 4.
- Palm J., Fuchs K., Stammer H. et al. Efficacy and safety of a triple active sore throat lozenge in the treatment of patients with acute pharyngitis: Results of a multi-centre, randomised, placebo-controlled, double-blind, pa–rallel-group trial (DoriPha). Int. J. Clin. Pract. 2018. Vol. 72. № 12. P. e13272.
- Passàli D.M., Lauriello G.C., Passàli F.M., Passàli and Bellussi L., Group A streptococcus and its antibiotic resistance. Acta Otorhinolaryngol. Ital. 2007. Vol. 27. № 1. Р. 27.
- Pompilio A., Geminiani C., Bosco D. et al. Electrochemically synthesized silver nanoparticles are active against planktonic and biofilm cells of Pseudomonas aeruginosa and other cystic fibrosis-associated bacterial pathogens. Front. Microbiol. 2018. Vol. 9. P. 1349.
- Saeb A.T.M., Alshammari A.S., Al-Brahim H., Al-Rubeaan K.A. Production of silver nanoparticles with strong and stable antimicrobial activity against highly pathogenic and multidrug resistant bacteria. Sci. World J. 2014. Vol. 2014. P. 704708.
- Windfuhr J.P., Toepfner N., Steffen G. et al. Clinical practice guideline: tonsillitis I. Diagnostics and nonsurgical management. Eur. Arch. Otorhinolaryngol. 2016. Vol. 273. № 4. P. 973-987.
- Wolford R.W., Goyal A., Belgam Syed S.Y. et al. Pharyngitis. [Updated 2023 May 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK519550/
- Клінічна настанова, заснована на доказах. Тонзиліт. 2021. URL: https://www.dec.gov.ua/wp-content/uploads/2021/04/2021_639_kn_tonzylit.pdf.
- Няньковський С.Л., Яцула М.С., Койро О.О. Захворювання горла та ротової порожнини: розчини наносрібла як ключ до успішного лікування. Здоров`я дитини. 2024. Т. 19. № 1. С. 1-8.
- Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги. Тонзиліт. 2021. URL: https://www.dec.gov.ua/wp-content/uploads/2021/04/2021_639_ykpmd_tonzylit_dd.pdf.

/57_2.jpg)