Резюме
Актуальність. Для досягнення успіху в інкорпорації кісткових алоімплантатів та кістки реципієнта береться до уваги багато чинників, які можна розділити на дві основні групи — фактори, що стосуються стерилізації та обробки кісткового алоімплантату, та фактори, що впливають на надійність фіксації імплантату у кістці реципієнта. Другим важливим фактором є методика фіксації алоімплантатів та кістки реципієнта. Мета: визначити механічні властивості кістки після сегментарної кісткової алопластики. Матеріали та методи. Хвора Ш., 30 років, із діагнозом «остеогенна саркома дистального відділу лівої великогомілкової кістки T2N0M0 GIII, II стадія, II клінічна група», якій було проведено курси поліхіміотерапії, оперативне втручання за розробленою методикою. Видалено пухлини en block, заміщено післярезекційний дефект артикулюючим сегментарним кістковим алоімплантатом, який було фіксовано до кістки реципієнта через сходинкоподібну остеотомію, та інтрамедулярним блоківним стрижнем. У зоні контакту алоімплантату та кістки реципієнта додатково розміщено кіст-кові автотрансплантати. Через 2 роки пацієнтці було проведено оперативне втручання: ампутація лівої нижньої кінцівки на рівні н/3 стегна. Рентгенологічно відзначалося зрощення алоімплантату та кістки реципієнта. Проведено експериментальне дослідження межі міцності великогомілкової кістки після сегментарної алопластики післярезекційного дефекту із застосуванням розробленої методики оперативного втручання та сегментарного алоімплантату. Результати. Для порівняння результатів експериментального дослідження препарату великогомілкової кістки після сегментарної кісткової алопластики були відібрані дані про величини межі міцності кісткової тканини при навантаженнях на стиск і згин. Як показав проведений експеримент, межа міцності препарату великогомілкової кістки після її кісткової алопластики дорівнює 51,82 МПа. Це значення відповідає мінімальній величині межі міцності компактної кістки при згинанні — 51 МПа. Хоча це вдвічі поступається максимальному значенню межі міцності компактної кістки на згін (133 МПа), але треба зважати на те, що всі наведені довідкові показники були отримані при випробуваннях неушкоджених препаратів компактної кістки. Висновки. Застосування сегментарного кісткового алоімплантату для заміщення післярезекційного дефекту довгої кістки з фіксацією його до кістки реципієнта через сходинкоподібну остеотомію та інтрамедулярний блоківний остеосинтез із додатковою кістковою автопластикою у зоні контакту алоімплантату та кістки реципієнта дозволяє отримати в зоні остеотомії кістку, межа міцності якої відповідає неушкодженій компактній кістковій тканині.
Background. To achieve success in the incorporation of allografts and bone of the recipient, many factors are taken into account, which can be divided into two main groups: those related to sterilization and processing of the bone allograft and factors affecting the reliability of implant fixation in the bone of the recipient. The second important factor is the method for fixing the allografts and the bone of the recipient. The purpose was to determine the mechanical properties of bone after segmental bone alloplasty. Materials and methods. Female patient Sh., 30 years old, diagnosed with osteosarcoma of the left distal tibia T2N0M0 GIII, degree II, clinical group II, underwent polychemotherapy courses, surgical intervention according to the developed method. The tumor was removed en block, a post-resection defect was replaced with an articulating segmental bone allograft, fixed to the recipient’s bone through a stepped osteotomy and an intramedullary locked nail. Bone autografts were additionally placed into the area of the allograft contact with the recipient’s bone. After 2 years, the patient underwent surgery: amputation at the left third of the thigh. Radiographically, fusion of the allograft and the recipient’s bone was noted. An experimental study of the tensile strength of the tibia after segmental alloplasty of a post-resection defect was carried out using the developed surgical technique and a segmental allograft. Results. To compare the results of an experimental study of the tibia preparation after segmental bone alloplasty, data about the values of the ultimate strength of the bone tissue under compression and bending loads were selected. As shown by the experiment, the ultimate strength of the tibia preparation after its bone alloplasty was 51.82 MPa. This value corresponds to the minimum ultimate strength of a compact bone in bending — 51 MPa. Although this is twice as low as the maximum value of the ultimate strength of a compact bone in bending (133 MPa), it should be borne in mind that all the given reference values were obtained when testing intact preparations of a compact bone. Conclusions. The use of a segmental bone allograft to replace a post-resection defect in a long bone with its fixation to the recipient’s bone through a stepped osteotomy and locked intramedullary nailing with additional bone autoplasty in the area of the allograft contact with the recipient’s bone makes it possible to obtain in the osteotomy zone the bone, the ultimate strength of which corresponds to that of the intact tissue.
Вступ
Застосування кісткових сегментарних алоімплантатів у онкоортопедії — часто вживана методика. Для досягнення успіху в інкорпорації кісткових алоімплантатів та кістки реципієнта береться до уваги багато чинників, які можна розділити на дві основні групи — фактори, що стосуються стерилізації та обробки кісткового алоімплантату, та фактори, що впливають на надійність фіксації імплантату у кістці реципієнта. Незважаючи на те, що кісткова алопластика вже багато десятиріч широко застосовується в ортопедії, досі ведуться пошуки нових методик стерилізації та обробки алоімплантатів, спрямованих на забезпечення надійної стерилізації (ефективне знищення бактерій, грибків, вірусів, спор), а також збереження механічних властивостей кістки, що наближаються до нормальної кістки [1–4].
Другим важливим фактором, що впливає на процес ремоделювання кісткової тканини у разі застосування сегментарних кісткових алоімплантатів для заміщення великих післярезекційних дефектів довгих кісток, є методика фіксації алоімплантатів та кістки реципієнта (хірургічна техніка). Одними з основних вимог у цих випадках є стабільність фіксації та досягнення найбільшого контакту між алоімплантатом та кісткою реципієнта [5–9]. Отже, поліпшення різних умов для досягнення максимально гарного результату у процесах інкорпорації сегментарних кісткових алоімплантатів є натепер актуальним питанням.
Біомеханічні дослідження механічних властивостей кісткових алоімплантатів мають велике значення у дослідженнях цієї проблеми [10–13]. Часто використовуються стандартні процедури навантаження на дослідні моделі кісток — осьове, ротаційне, на згин.
Мета: визначити механічні властивості (міцність) кістки після сегментарної кісткової алопластики.
Матеріали та методи
Техніка оперативного втручання
У клініці ДУ «ІПХС ім. проф. М.І. Ситенка НАМН України» перебувала на лікуванні хвора Ш., 30 років, із діагнозом «остеогенна саркома дистального відділу лівої великогомілкової кістки T2N0M0 GIII, II стадії, II клінічна група». Хворій було проведено курси поліхіміотерапії, оперативне втручання за розробленою методикою [14]. Під час оперативного втручання здійснено видалення пухлини en block, заміщення післярезекційного дефекту дистального відділу великогомілкової кістки артикулюючим сегментарним кістковим алоімплантатом, який було фіксовано до кістки реципієнта через сходинкоподібну остеотомію, та інтрамедулярним блоківним стрижнем.
У зоні контакту алоімплантату та кістки реципієнта додатково розміщено кісткові автотрансплантати (рис. 1).
Стерилізація кісткового алоімплантату
Стерилізацію кісткового алоімплантату проводили радіаційним γ-випромінюванням (обробку алоімплантатів здійснювали у Харківському фізико-технічному інституті, науково-дослідному комплексі «Прискорювач» за допомогою прискорювача «ЛУ-10», методом дозиметрії з використанням детекторів Harwell Perpex 4034 (ISO/ASTM 51276)).
Через 2 роки після лікування у хворої виявили декілька вогнищ остеосаркоми у грудних хребцях, лопатці, правій стегновій кістці та у проксимальному відділі лівої великогомілкової кістки. Встановлено діагноз: мультицентрична остеосаркома, метахронний тип.
Через наявність патологічного вогнища у в/3 лівої великогомілкової кістки та вираженого больового синдрому пацієнтці було проведено оперативне втручання: ампутація лівої нижньої кінцівки на рівні н/3 стегна.
Біомеханічні дослідження
Видалений препарат було досліджено у лабораторії біомеханіки. Перед дослідженням проведено рентгенографію препарату гомілки з наявністю інтрамедулярного стрижня та після його видалення (рис. 2). Рентгенологічно відзначалося зрощення алоімплантату та кістки реципієнта.
У лабораторії біомеханіки ДУ «ІПХС ім. проф. М.І. Ситенка НАМН України» було проведено експериментальне дослідження міцності великогомілкової кістки після сегментарної алопластики післярезекційного дефекту із застосуванням розробленої методики оперативного втручання (фіксація алоімплантату через сходинкоподібну остеотомію, інтрамедулярний блоківний остеосинтез, додаткове застосування кісткових автотрансплантатів) та сегментарного алоімплантату, що був стерилізований γ-випромінюванням. Препарат було виготовлено у лабораторії патоморфології сполучної тканини (рис. 3).
Під час експерименту проводили біомеханічне дослідження міцності кістки з навантаженням на згин (рис. 4а). Згинаюче навантаження прикладали в зоні з’єднання алоімплантату та кістки реципієнта (рис. 4б).
Величину навантаження вимірювали за допомогою тензодинамометричного датчика SBA-100L. Результати фіксували пристроєм реєстрації даних CAS типу CI-2001A.
Величину переміщень в системі «кістковий алоімплантат — кістка реципієнта» вимірювали за допомогою мікрометричного індикатора часового типу. Геометричні показники вимірювали за допомогою штангенциркуля.
За даними експерименту розраховували межу міцності препарату великогомілкової кістки. Результат розрахунку порівнювали з довідковими даними, наведеними в науковій літературі [15–18].
Результати
Для обробки даних була розроблена розрахункова схема експерименту, наведена на рис. 5.
Під час експерименту були отримані такі значення параметрів, необхідних для розрахунків: D = 22 мм; d = 15 мм; L = 140 мм; L/2 = 70 мм. У результаті проведеного випробування були отримані значення
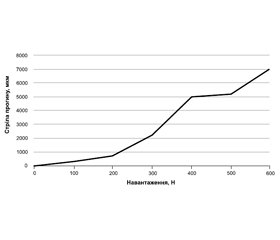
величини стріли прогину кістки (∆l) залежно від величини згинаючої сили (F). Отримані дані наведено в табл. 1.
На рис. 6 наведено графік залежності величини стріли прогину препарату від величини згинаючого навантаження.
Величину межі міцності препарату великогомілкової кістки розраховували за формулою [19]:
де M — момент дії згинаючої сили F; W — момент опору зразка.
Для об’єктів, що мають кільцевий перетин, момент опору розраховують за формулою [19]:
Момент дії згинаючої сили визначається як добуток її величини на величину важеля її дії:
Підставимо вирази (2) і (3) до рівняння (1) та отримаємо остаточну формулу для визначення величини межі міцності для зразка з кільцевим перетином:
Підставимо в рівняння (4) вихідні дані для розрахунку та отримаємо величину межі міцності дослідженого препарату:
Для порівняння результатів експериментального дослідження препарату великогомілкової кістки після сегментарної кісткової алопластики були відібрані дані про величини межі міцності кісткової тканини при навантаженнях на стиск і на згин. Дані з наукової літератури наведені в табл. 2.
Як показав проведений експеримент, межа міцності препарату великогомілкової кістки після її кісткової алопластики дорівнює 51,82 МПа. Це значення відповідає мінімальній величині межі міцності компактної кістки при згинанні — 51 МПа [17]. Хоча це вдвічі поступається максимальному значенню межі міцності компактної кістки на згін (133 МПа), але треба зважати на те, що всі наведені довідкові показники були отримані при випробуваннях неушкоджених препаратів компактної кістки.
Обговорення
З літературних даних відомо, що різні методи стерилізації кісткових алоімплантатів (такі як автоклавування, обробка хімічними препаратами — оксидом етилену та перекисом водню) можуть негативно впливати на їхні механічні та біологічні властивості. Обробка алоімплантату високими температурами (вище 60 ºС) знижує їхню міцність та погіршує остеоіндуктивність [20]. Хімічна обробка (за допомогою оксиду етилену та перекису водню) також порушує процес остеоіндуктивності. Стерилізація γ-випромінюванням призводить до втрати міцності кістки, але в цих дослідженнях вказано різні дози випромінювання і не враховувався часовий інтервал виживаності алоімплантатів [20]. Islam та співавт. вивчали вплив багатоциклічного навантаження на алокістку, що була стерилізована γ-випромінюванням, та виживаність алоімплантатів. У цьому дослідженні було встановлено зниження міцності кісткового алоімплантату [21]. Більшість біомеханічних випробувань проводилися на алоімплантатах, що не були піддані імплантації у кістку пацієнта, а також вивчалися міцнісні характеристики імплантатів залежно від різних способів їх стерилізації. В нашому дослідженні використовувалась біологічна система «кістковий алоімплантат — кістка реципієнта» після завершення процесів ремоделювання кісткової тканини, а також вивчалась міцність фіксації алоімплантату за запропонованою методикою хірургічного втручання. Отже, на міцність з’єднання алоімплантату та кістки реципієнта впливає не тільки спосіб стерилізації алоімплантатів (та їхні біологічні й механічні властивості), але і спосіб фіксації їх у кістці реципієнта.
За даними Fatih Yildis та співавт., під час проведення біомеханічного дослідження на стенді моделі стегнової кістки з різними видами остеотомії її проксимального відділу та фіксацією ніжкою ендопротеза кульшового суглоба виявили, що вид остеотомії (сходинкоподібна та коса) і різні варіанти ніжок ендопротеза не сприяють впливу на стійкість усієї системи «ендопротез — стегнова кістка» [22]. Але в іншому дослідженні Brett M. Cascio та співавт. біомеханічно довели, що під час застосування сходинкоподібної остеотомії підвищується концентрація напруження у її крайніх точках (у кутах 90 ºС), що призводить під час навантаження до появи тріщин. Для того, щоб запобігти цьому ефекту, автори запропонували сигмоподібну остеотомію, яка згладжує кути та зменшує концентрацію напруження в зоні остеотомії і поширює його рівномірно на всю поверхню взаємодії кісток. Також було розраховано площу контакту кісток після різних видів остеотомій. Так, поперечна становила 2,57 см2, сходинкоподібна та сигмоподібна — 4,49 см2 та 3,72 см2 (що не являло статистично вірогідної різниці). Отже, площа контакту кісток значно більше у разі застосування саме двох останніх видів остеотомій, що, в свою чергу, покращує умови для ремоделювання кісткової тканини [23].
У наведеному дослідженні вивчалась міцність з’єднання сегментарного кісткового алоімплантату та кістки реципієнта. З’єднання кісток здійснювалося через сходинкоподібну остеотомію та фіксацію інтрамедулярним стрижнем. У цьому експерименті вивчалась кістка після процесів ремоделювання кісткової тканини. В результаті проведеного експерименту на біомеханічному стенді було виявлено ефективне зрощення алокісткового імплантату та кістки реципієнта, наведено міцність кістки у зоні контакту, що наближається до міцності здорової компактної кістки.
Висновки
Застосування сегментарного кісткового алоімплантату для заміщення післярезекційного дефекту довгої кістки з фіксацією його до кістки реципієнта через сходинкоподібну остеотомію й інтрамедулярний блоківний остеосинтез із додатковою кістковою автопластикою у зоні контакту алоімплантату та кістки реципієнта дозволяє отримати в зоні остеотомії кістку, межа міцності якої відповідає неушкодженій компактній кістковій тканині.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 01.10.2021
Рецензовано/Revised 12.10.2021
Прийнято до друку/Accepted 29.10.2021
Список литературы
1. Gautam D., Arora N., Gupta S., George J., Malhotra R. Megaprosthesis Versus allograft prosthesis composite for the management of massive skeletal defects: a meta-analysis of comparative studies. Current reviews in Musculoskeletal Medicine. 2021. Vol. 14(3). P. 255-270. doi: https://doi.org/10.1007/s12178-021-09707-6.
2. Gharedaghi M., Peivandi M.T., Mazloomi M., Shoorin H.R., Hasani M., Seyf P., Khazaee F. Evaluation of clinical results and complications of structural allograft reconstruction after bone tumor surgery. Arch. Bone Joint Surgery. 2016. Vol. 4(3). P. 236-242. Retrieved from https://pubmed.ncbi.nlm.nih.gov/27517069.
3. Вырва О.Е., Головина Я.А., Малык Р.В. Аллокомпозитное эндопротезирование при хирургическом лечении пациентов со злокачественными опухолями длинных костей (обзор литературы). Ортопедия, травматология, протезирование. 2015. № 2. C. 120-125. doi: https://doi.org/10.15674/0030-598720152120-125.
4. Nguyen H., Morgan D.A., Forwood M.R. Sterilization of allograft bone: effects of gamma irradiation on allograft biology and biomechanics. Cell and tissue banking. 2007. Vol. 8(2).
P. 93-105. doi: https://doi.org/10.1007/s10561-006-9020-1
5. Вирва О.Є., Головіна Я.О., Малик Р.В., Головіна О.О. Системний огляд і метааналіз результатів модульного й алокомпозитного ендопротезування за умов кістково-суглобових дефектів після резекції пухлини. Ортопедія, травматологія і протезування. 2020. № 2. С. 5-15. doi: https://doi.org/10.15674/0030-5987202025-15.
6. Вирва О.Є., Бурлака В.В., Карпінський М.Ю. Напружено-деформовані стани в системі «ендопротез — променева кістка» (біомеханічне дослідження). Ортопедия, травматология и протезирование. 2012. № 3. С. 14-19. doi: 10.15674/0030-59872012314-19.
7. Vyrva O., Burlaka V., Karpinsky M. Tumor endoprothesis-radius bone system stress-deformity state. Biomechanical study. Muskuloskeletal Tumor Society: Annual Meeting, September, 20-22. 2012. 158.
8. Вирва О.Є., Міхановський Д.О., Карпінський М.Ю. Біомеханічне дослідження напружено-деформованих станів системи «ендопротез — плечова кістка» за умов резекції пухлини. Ортопедия, травматология и протезирование. 2015. № 3. С. 14-20. doi: 10.15674/0030-59872015314-20.
9. Вирва О.Є., Міхановський Д.О., Головіна Я.О., Нікольченко О.А., Карпінський М.Ю. Експериментальне обґрунтування комбінованої фіксації пухлинного ендопротеза для заміщення діафізарних дефектів довгих кісток у щурів. Ортопедия, травматология и протезирование. 2015. № 4. С. 49-54. doi: 10.15674/0030-59872015449-54.
10. Вирва О.Є., Міхановський Д.О., Карпінський М.Ю., Нікольченко О.А. Комбінована фіксація модульного пухлинного ендопротеза проксимального відділу плечової кістки (експериментально-клінічне дослідження). Ортопедия, травматология и протезирование. 2017. № 3. С. 99-104. doi: 10.15674/0030-59872017399-104.
11. Вирва О.Є., Головіна Я.О., Карпінський М.Ю., Яресько О.В., Малик Р.В. Дослідження напружено-деформованого стану в системі «імплантат — кістка» на моделі алокомпозитного ендопротеза проксимального відділу стегнової кістки. Травма. 2020. № 21(1). С. 38-48. doi: 10.22141/1608-1706.1.21.2020.197797.
12. Вирва О.Є., Головіна Я.О., Карпінська О.Д., Карпінський М.Ю. Біомеханічне експериментальне обґрунтування методики фіксації кісткового алоімплантата і кістки реципієнта. Ортопедия, травматология и протезирование. 2020. № 1. С. 40-45. doi: 10.15674/0030-59872020140-45.
13. Вирва О.Є., Головіна Я.О., Малик Р.В., Карпінський М.Ю., Яресько О.В. Порівняльний аналіз даних напружено-деформованого стану математичних моделей індивідуального ендопротеза й алокомпозитного ендопротеза у разі заміщення дефектів довгих кісток. Травма. 2021. № 22(4). С. 37-45. doi: 10.22141/1608-1706.4.22.2021.239708.
14. Патент України № 145498 «Спосіб алокомпозитного ендопротезування». Вирва О.Є., Головіна Я.О., Малик Р.В.; опубл. 10.12.2020.
15. Аврунин А.С. Механизм жесткости и прочности кости в норме и при старении организма. Наноуровневая модель. Гений ортопедии. 2008. № 3. С. 59-66.
16. Olson S.A. Designing a biomechanics investigation: choosing the right model. J. Orthop. Trauma. 2012 Dec. Vol. 26(12). P. 672-7.
17. Hart N.H., Nimphius S., Rantalainen T., Ireland A., Siafarikas A., Newton R.U. Mechanical basis of bone strength: influence of bone material, bone structure and muscle action. J. Musculoskelet Neuronal. Interact. 2017 Sep. Vol. 17(3). P. 114-139. PMID: 28860414
18. Dong X.N., Acuna R.L., Luo Q. et al. Orientation dependence of progressive post-yield behavior of human cortical bone in compression. J. Biomech. 2012. Vol. 45. P. 2829-2834.
19. Александров А.В., Потапов В.Д., Державин Б.П. Сопротивление материалов. М.: Высшая школа, 2000. 560 с.
20. Nguyen H., Morgan D.A., Forwood M.R. Sterilization of allograft bone: effects of gamma irradiation on allograft biology and biomechanics. Cell and tissue banking. 2007. Vol. 8(2). P. 93-105. doi: https://doi.org/10.1007/s10561-006-9020-1.
21. Islam A., Chapin K., Moore E., Ford J., Rimnac C., Akkus O. Gamma radiation sterilization reduces the high-cycle fatigue life of allograft bone. Clinical Orthopaedics and Related Research. 2016. Vol. 474(3). P. 827-835. doi: https://doi.org/10.1007/s11999-015-4589-y.
22. Fatih Yıldız, Onder Kılıçoglu, Goksel Dikmen, Ergun Bozdag, Emin Sünbüloglu, Meral Tuna. Biomechanical comparison of oblique and step-cut osteotomies used in total hip arthroplasty with femoral shortening. http://dx.doi.org/10.1016/j.jos.2016.04.015. Journal of Orthopaedic. Science. 2016. Vol. 21. P. 640e646.
23. Brett M. Cascio, Kevin A. Thomas, Scott C. Wilson. A Mechanical Comparison and Review of Transverse, Step-Cut, and Sigmoid Osteotomies. Сlinical orthopaedics and related research. 2003. Vol. 411. P. 296-304. doi: 10.1097/01.blo.0000069895.31220.e8.
/32.jpg)
/33_2.jpg)
/34.jpg)
/34_2.jpg)
/35.jpg)
/35_2.jpg)
/35_3.jpg)
/35_4.jpg)

/33.jpg)
/34_3.jpg)
/35_6.jpg)
/35_5.jpg)