Резюме
У статті наводяться результати ендопротезування суглобів і кісток у 19 пацієнтів з метастатичними пухлинами кістки. У результаті ендопротезування суглобів і кісток при метастатичних пухлинах кісток ускладнення спостерігалися у 4 (21,1 %) пацієнтів і рецидиви пухлини — у 2 (10,5 %) хворих. У передопераційному періоді 19 пацієнтам було проведено курс дистанційної променевої терапії до сумарної осередкової дози 40 Грей при разовій осередковій дозі 2–2,5 Грей. Також усі хворі отримували курси передопераційної поліхіміотерапії згідно з першоджерелом пухлини, а при гормонозалежних пухлинах — гормонотерапію. Залежно від конкретних анатомо-функціональних змін застосовувалися спеціальні конструкції імплантів, інструментарія та методичні прийоми, що доповнювали стандартну техніку операцій. При ендопротезуванні кісток і суглобів дотримувалися основних принципів онкохірургії — футлярності та абластичності, видалення одним блоком зони біопсії. При ендопротезуванні використовували цементний тип фіксації ендопротеза. Для адекватного формування м’язового футляра ендопротеза проводили пластичний етап операції, що дозволяв адекватно вкрити встановлений ендопротез і тим самим зменшити ризик розвитку інфекційних ускладнень. Як пластичний матеріал застосовували як переміщені, так і вільні васкуляризовані шкірно-м’язові клапті на мікросудинних анастомозах. З метою обмеження контакту металевої частини ендопротеза з прилеглими тканинами та з метою реконструкції сухожильно-зв’язкового апарату застосовували трубку з поліетилентетрафталату, до неї підшивалися резеційовані м’язи та сухожилля, що дозволяло більш повно відновити функцію суглоба. Функція кінцівки за шкалою MSTS після ендопротезування суглобів становила від 70 до 92 %, також підвищилася якість життя хворих до 70–75 балів.
The article presents the results of endoprosthesis replacement of joints and bones in 19 patients with bone metastasis. The complications resulted from endoprosthesis replacement of joints and bones in cases of bone metastasis were observed in 4 (21.1 %) patients, and tumor recurrences were observed in 2 (10.5 %) patients. In the preoperative period, 19 patients underwent courses of external beam radiotherapy with a total radiation dose (TRD) of 40 Gray, with a single mediated dose (SMD) of 2–2.5 Gray. Also, all patients received preoperative multiagent chemotherapy treatment cycles depending on the primary source of the tumor, and in cases of hormone-dependent tumors, the patients received hormone therapy. Depending on the specific anatomical and functional changes, special implant designs, tools, and techniques were used, which complemented the standard technique of operations. The basic principles of oncosurgery have been adhered to during endoprosthesis replacement of joints and bones, i.e. standard principles of resection and ablastics, removing en bloc of a biopsy area. In endoprosthesis replacement, a cement type of endoprosthesis fixation was used. For an adequate formation of the muscle envelope of the endoprosthesis, a plastic stage of the ope-ration was performed, which allowed to adequately cover the installed endoprosthesis, and thus, reduce the risk of infectious complications. Both displaced and free vascularized musculocutaneous flaps on microvascular anastomoses were used as plastic material. To limit the contact of the metal part of the endoprosthesis with the surrounding tissues and to reconstruct the tendon ligamentous apparatus, a tube of polyethylene tetraphthalate was used, resected tendon and muscles were sutured to it, which allowed to more fully restore joint action. The functioning of extremity according to the MSTS scale after endoprosthesis replacement of joints ranged from 70 to 92 %, and also the quality of life of patients improved up to 70–75 points.
Вступ
За даними літератури, метастатичне ураження скелета є третьою за частотою локалізацією після метастатичного ураження легенів і печінки. Причому в скелеті ураження хребта злоякісними пухлинами зустрічається у 70 % хворих, кісток таза і кінцівок — у 40 %, ділянки кульшового суглоба — у 25 % [1, 2]. Ризик патологічних переломів у довгих трубчастих кістках корелює зі ступенем деструкції кортикального шару. Перелом стає можливим при ураженні кортикального шару більше ніж на 50 % [3, 4]. Патологічні переломи, що вимагають хірургічного лікування, зустрічаються у 9 % хворих з метастазами в кістки [5]. У літературі повідомляється, що головними показаннями до хірургічного лікування метастатичного ураження кісток є солітарні метастази, явний больовий синдром, патологічний перелом або загроза його виникнення, але застосування тільки хірургічних методів лікування призводить до 45,6 % рецидивів пухлини [6–8]. Хірургічне лікування, що є паліативним методом в комбінованій терапії метастазів у кістки, відіграє важливу роль в адаптації хворих і полегшує їм проведення подальшого лікування [9, 10]. На даний час у світовій онкоортопедії хірургічні методи метастатичного ураження кісток представлені ендопротезуванням, інтрамедулярним і накістковим остеосинтезом, кюретажем пухлини з використанням кісткового цементу, черезкістковим позавогнищевим остеосинтезом і стабілізуючими оперативними втручаннями на хребті [11–14]. Ендопротезування суглобів практично завжди обґрунтоване й є методом вибору при метастатичному ураженні суглобових сегментів кістки, але використання ендопротезів, що заміщюють 2/3 або цілу кістку при ураженні діафіза кістки [15, 16], дуже травматичне і виправдане тільки при солітарних метастазах, коли воно спрямоване на лікування хворого. Виконання ендопротезування при пухлинах кісток — завжди складне завдання, яке залежить від морфологічної структури пухлини, її розмірів, залучення в пухлинний процес оточуючих м’яких тканин і судинно-нервових сплетінь, реакції організму хворого на встановлений ендопротез та інших факторів [17]. У літературі повідомляється, що при ендопротезуванні суглобів з приводу пухлин кісток застосовувалися модульні ендопротези різних конструкцій, як з цементним, так і безцементним типом фіксації [18, 19]. Після проведення хірургічного лікування при метастатичному ураженні довгих трубчастих кісток вдається поліпшити опороспроможність і функцію кінцівки, покращити якість життя хворих [20, 21]. Застосування ендопротезування в хірургії пухлин кісток, а також нових схем протипухлинної хіміотерапії дозволило покращити безпосередні та віддалені результати лікування й підвищити трирічну та п’ятирічну виживаність даної категорії хворих [22]. У нашій роботі ми показали випадки ендопротезування кісток і суглобів при метастатичному ураженні кісток.
Матеріали та методи
У клінічному відділі ДУ «Інститут травматології та ортопедії НАМН України» виконано 19 органозберігаючих операцій в обсязі сегментарної резекції з наступним ендопротезуванням суглобів і діафізів кісток при метастатичному ураженні. Середній вік хворих становив 48,6 ± 1,6 року (від 35 до 76 років), жінок було 14 (73,7 %), чоловіків — 5 (26,3 %). У 13 пацієнтів застосовані індивідуальні онкологічні ендопротези НВО «Інмед» (Україна), у 4 — фірми «Valdemar Link» (Німеччина), в 1 — «Beznoska» (Чехія), в 1 — «ImplantСast» (Німеччина). У табл. 1 наведені морфологічні форми пухлин, що зустрічалися.
У табл. 2 наведені локалізація та кількість випадків при ендопротезуванні суглобів і кісток.
/76.jpg)
Передопераційне обстеження включало клініко-рентгенологічне (при необхідності комп’ютерну томографію (КТ), магнітно-резонансну томографію (МРТ)) обстеження, обов’язково проводилась трепан- або відкрита біопсія ураженого сегмента кістки з метою верифікації процесу, а також розрахунок протяжності резекції сегмента кістки та розрахунок розмірів ендопротеза за даними рентгенографії, КТ або МРТ ураженої кістки. Усім 19 пацієнтам у передопераційному періоді було проведено курс дистанційної променевої терапії до сумарної осередкової дози 40 Грей при разовій осередковій дозі 2–2,5 Грей. Променева терапія була показана при метастатичних пухлинах кісток у зв’язку з тим, що ці пухлини, за даними експериментально-клінічного дослідження, чутливі до променевої терапії. Також усі хворі отримували курси перед-операційної поліхіміотерапії згідно з першоджерелом пухлини, а при гормонозалежних пухлинах — гормонотерапію. Абластичне видалення пухлини суглобового сегмента понукало виконувати широку резекцію новоутворення. При ендопротезуванні кісток і суглобів дотримувалися основних принципів онкохірургії — футлярності та абластичності, видалення одним блоком зони біопсії, виконували адекватну м’язову пластику, закриваючи ендопротез м’якими тканинами для зменшення ризику інфікування. Залежно від конкретних анатомо-функціональних змін застосовувалися спеціальні конструкції імплантів, інструментарія та методичні прийоми, що доповнювали стандартну техніку операцій. При ендопротезуванні використовували цементний тип фіксації ендопротеза. Одним з протипоказань при ендопротезуванні є неможливість адекватного формування м’язового футляра імпланта, оскільки це збільшує ризик інфекційних ускладнень і тим самим погіршує функціональні результати кінцівки. Для вирішення цієї проблеми ми проводили пластичний етап операції, що дозволяє адекватно вкрити встановлений ендопротез і тим самим зменшити ризик розвитку інфекційних ускладнень. Як пластичний матеріал ми застосовували як переміщені, так і вільні васкуляризовані клапті на мікросудинних анастомозах. У всіх 19 пацієнтів з метою обмеження контакту металевої частини ендопротеза з прилеглими тканинами та з метою реконструкції сухожильно-зв’язкового апарату ми застосовували трубку з поліетилентетрафталату фірми «ImplantСast» (Німеччина), до неї підшивалися резеційовані м’язи та сухожилля, що дозволяло більш повно відновити функцію суглоба. Результати функціональної активності прооперованого відділу скелета визначалися нами за шкалою MSTS (Musculoskeletal Tumor Society). Якість життя визначали за опитувальником EORTC-QLQ-С30 (у балах). Виживаність пацієнтів оцінена методом Каплана — Мейєра.
Результати
У результаті ендопротезування суглобів і кісток при метастатичному ураженні ускладнення спостерігалися у 4 (21,1 %) пацієнтів. Серед ускладнень: асептичне розхитування ніжки ендопротеза у 2 пацієнтів після ендопротезування ліктьового суглоба та в 1 пацієнта — після ендопротезування діафіза плечової кістки. Інфекційні ускладнення спостерігалися в 1 пацієнта після ендопротезування колінного суглоба.
При асептичному розхитуванні ніжки ендопротеза виконували реендопротезування. При інфекційному ускладненні, незважаючи на проведення консервативного та хірургічного лікування, нам не вдалося ліквідувати інфекцію, тому виконали ампутацію нижньої кінцівки на рівні верхньої третини стегна.
Рецидиви пухлини спостерігалися у 2 (10,5 %) хворих після ендопротезування ліктьового суглоба та в 1 пацієнта — після ендопротезування плечового суглоба, виконано в 1 випадку екзартикуляцію верхньої кінцівки в плечовому суглобі, в іншому випадку — ампутацію верхньої кінцівки в верхній третині плеча.
Приклади з практики
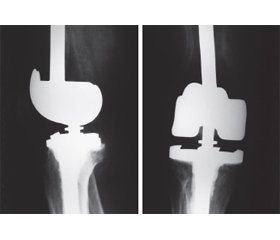
Хвора К., 50 років, надійшла до відділення з діагнозом «метастаз раку слинної залози в дистальний відділ лівої плечової кістки, стан після комбінованого лікування (передопераційна поліхіміотерапія та променева терапія), кл. гр. II». 23.03.2021 року хворій виконана операція в обсязі резекції дистального відділу плечової кістки з пухлиною та ендопротезування ліктьового суглоба ендопротезом фірми «Інмed» (Україна). На рис. 1 наведені фотовідбитки рентгенограм хворої К. з метастатичною пухлиною дистального відділу плечової кістки. На рис. 2 — фотовідбитки рентгенограм хворої К., стан після резекції дистального відділу плечової кістки з метастатичною пухлиною та ендопротезування ліктьового суглоба.
/77.jpg)
Хворий П., 62 років, надійшов до відділення з діагнозом «метастаз раку нирки в дистальний відділ правої стегнової кістки, стан після комплексного лікування (передопераційна променева терапія та поліхіміотерапія, бісфосфонати, імунотерапія, гормонотерапія)». 01.02.2021 року хворому виконана операція в обсязі сегментарної резекції дистального відділу правої стегнової кістки та ендопротезування колінного суглоба ендопротезом фірми «Beznoska» (Чехія). На рис. 3 наведені фотовідбитки рентгенограм хворого П. з метастатичною пухлиною дистального відділу стегнової кістки. На рис. 4 — фотовідбитки рентгенограм хворого П., стан після резекції дистального відділу стегнової кістки з метастатичною пухлиною та ендопротезування колінного суглоба.
Функція кінцівки за шкалою MSTS становила після ендопротезування плечового суглоба 70 %, діафіза плечової кістки — 92 %, ліктьового суглоба — 75 %, кульшового суглоба — 80 %, діафіза стегнової кістки — 90 %, колінного суглоба — 88 %.
Якість життя хворих за опитувальником EORTC QLQ-30 становила 20–30 балів до ендопротезування і підвищилась в середньому до 70–75 балів після ендопротезування. Трирічна загальна виживаність пацієнтів становила 42,3 ± 8,7 %, п’ятирічна загальна виживаність пацієнтів — 22,2 ± 8,5 %.
Обговорення
Лікування хворих з метастатичними пухлинами довгих кісток кінцівок є складною проблемою клінічної онкоортопедії, що обумовлене несвоєчасною діагностикою, агресивним перебігом процесу, низькими показниками виживаності хворих, а також інвалідизацією пацієнтів у випадках втрати кінцівки. Лікувальна тактика у пацієнтів з метастатичним ураженням кісток визначалася в першу чергу загальним станом пацієнта, наявністю метастазів в інших органах і системах. Ту чи іншу ортопедичну тактику визначали: поодинокий метастаз в довгу кістку, наявність множинних метастазів у кістках або вісцеральних органах (легенях, печінці, головному мозку), локалізації метастатичного вогнища в кістці і залучення в процес навколишніх м’яких тканин, нервів, судин. У всіх хворих з метастатичними ураженням довгої кістки хірургічне втручання було одним з етапів комплексного лікування, що включало в себе променеву терапію, хіміотерапію, гормонотерапію, імунотерапію. Променева терапія з успіхом застосовується при лікуванні багатьох злоякісних новоутворень різної локалізації. Основну масу становлять хворі з метастатичним ураженням кісток, які страждають від больового синдрому і в яких проведення променевої терапії призводить до зменшення або зникнення болю [12]. За даними літератури, завдяки опроміненню часткового ефекту вдається досягти у 60–80 %, а повного знеболювання — у 15–40 % пацієнтів [6]. Крім того, при метастатичних ураженнях кісток, що супроводжуються м’якотканинним компонентом, проводиться більш широка резекція оточуючих пухлину м’яких тканин, що вимагає застосування окремих видів коригуючих шкірно-пластичних операцій [10]. Коли є показання до ендопротезування суглобів, саме стан навколосуглобових покривних тканин і м’яких тканин, що глибоко залягають, виявляється тим чинником, що майже повністю визначає успіх, а іноді й саму можливість проведення цієї операції. У цілому отримані нами результати вказують на те, що у пацієнтів, які потребують ендопротезування суглобів, застосування пластичних методик при дефіциті м’яких тканин сприяє зменшенню кількості післяопераційних ускладнень і рецидивів пухлини. Слід зазначити, що з підвищенням ефективності комбінованого лікування метастатичних пухлин кісток збільшилася тривалість життя хворих [9]. Таким чином, покращання результатів лікування хворих з метастатичними пухлинами кісток пов’язане з дотриманням абластики та асептики під час ендопротезування, удосконаленням конструкцій ендопротезів і техніки їх встановлення, стану оточуючих суглоб тканин. Ендопротезування при метастатичному ураженні кісток в комплексі з іншими методами лікування забезпечує відновлення функції та опороспроможності кінцівки й підвищує якість життя хворого.
Висновки
1. У результаті ендопротезування суглобів і кісток при метастатичних пухлинах кісток ускладнення спостерігалися у 4 (21,1 %) пацієнтів та рецидиви пухлини — у 2 (10,5 %) хворих.
2. Пластичні методики при дефіциті м’яких тканин дозволили розширити показання до проведення ендопротезування суглобів і кісток при метастатичних пухлинах кісток, що дозволило зменшити кількість післяопераційних ускладнень у ложі ендопротеза.
3. Проведення в передопераційному періоді променевої терапії на метастатичну пухлину кістки дозволило зменшити кількість рецидивів пухлини в післяопераційному періоді.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 15.05.2021
Рецензовано/Revised 28.05.2021
Прийнято до друку/Accepted 15.06.2021
Список литературы
1. García Carretero R., Romero Brugera M., Rebollo-Aparicio N., El Bouayadi Mohamed L. Primary bone metastasis as first manifestation of an unknown primary tumour. BMJ Case Rep. 2015 Sep 3. 2015. bcr2015211302. doi: 10.1136/bcr-2015-211302. PMID: 26338244; PMCID: PMC4567768.
2. Asdourian P.L. Metastatic disease of the spine. The Textbook of spinal surgery. 2nd ed. Philadelphia, 1997. 2007-2048.
3. Van der Linden Y.M., Dijkstra P.D., Kroon H.M., Lok J.J., Noordijk E.M., Leer J.W., Marijnen C.A. Comparative analysis of risk factors for pathological fracture with femoral metastases. J. Bone Joint Surg. Br. 2004 May. 86(4). 566-73. PMID: 15174555.
4. Mirels H. Metastatic disease in long bones. A proposed scoring system for diagnosing impending pathologic fractures. Clin. Orthop. Relat. Res. 1989 Dec. (249). 256-64. PMID: 2684463.
5. Алиев М.Д., Тепляков В.В., Каллистов В.Е., Валиев А.К., Карпенко В.Ю., Трапезников Н.Н. Современные подходы к хирургическому лечению метастазов злокачественных опухолей в кости. Практическая онкология: избранные лекции. СПб., 2004. 738-748.
6. Argentiero A., Solimando A.G., Brunetti O., Calabrese A., Pantano F., Iuliani M., Santini D., Silvestris N., Vacca A. Ske-letal Metastases of Unknown Primary: Biological Landscape and Clinical Overview. Cancers (Basel). 2019 Aug 29. 11(9). 1270. doi: 10.3390/cancers11091270. PMID: 31470608; PMCID: PMC6770264.
7. Kask G., Nieminen J., Parry M.C., van Iterson V., Paka-rinen T.K., Ratasvuori M., Laitinen M.K. Revision rate of reconstructions in surgically treated diaphyseal metastases of bone. Eur. J. Surg. Oncol. 2019 Dec. 45(12). 2424-2430. doi: 10.1016/j.ejso.2019.05.021. Epub 2019 May 21. PMID: 31133372.
8. Liska F., Schmitz P., Harrasser N., Prodinger P., Rechl H., von Eisenhart-Rothe R. Metastasen der Extremitäten: Übersicht über operative Versorgungsstrategien [Metastatic disease in long bones: Review of surgical treatment options]. Unfallchirurg. 2018 Jan. 121(1). 37-46. German. doi: 10.1007/s00113-016-0282-1. PMID: 27904933.
9. Cheung F.H. The practicing orthopedic surgeon's guide to managing long bone metastases. Orthop. Clin. North Am. 2014 Jan. 45(1). 109-19. doi: 10.1016/j.ocl.2013.09.003. Epub 2013 Oct 31. PMID: 24267212.
10. Солоницын Е.А., Климовицкий Ф.В., Проценко В.В. Метастазы анонимного рака в длинные кости конечностей: подходы к обследованию и лечению. Травма. 2017. 18(1). 97-102. doi: 10.22141/1608-1706.1.18.2017.95597.
11. Rath B., Tingart M., Migliorini F., Eschweiler J., Zureik R., Hardes J. Differenzierte Therapiestrategien bei Knochenmetastasen der Extremitäten [Differentiated treatment strategies for bone metastases of the extremities]. Orthopade. 2019 Sep. 48(9). 752-759. German. doi: 10.1007/s00132-019-03791-w. PMID: 31444515.
12. Вырва О.Е., Головина Я.А., Головина О.А., Малык Р.В. Дифференцированный подход к лечению больных с метастатическим поражением длинных костей конечностей. Клиническая онкология. 2012. № 1. 43-48. Режим доступа: http://nbuv.gov.ua/UJRN/klinonk_2012_1_9.
13. Zhao J., Xu M., Zheng K., Yu X. Limb salvage surgery with joint preservation for malignant humeral bone tumors: operative procedures and clinical application. BMC Surg. 2019 May 30. 19(1). 57. doi: 10.1186/s12893-019-0519-3. PMID: 31146705; PMCID: PMC6543608.
14. Angelini A., Trovarelli G., Berizzi A., Pala E., Breda A., Maraldi M., Ruggieri P. Treatment of pathologic fractures of the proximal femur. Injury. 2018 Nov. 49(3). S77-S83. doi: 10.1016/j.injury.2018.09.044. PMID: 30415673.
15. Tanaka A., Katagiri H., Murata H., Wasa J., Miyagi M., Honda Y., Takahashi M. Surgery for femoral metastases. Bone Joint J. 2020 Mar. 102-B(3). 285-292. doi: 10.1302/0301-620X.102B3.BJJ-2019-0976.R1. PMID: 32114815.
16. Anract P., Biau D., Boudou-Rouquette P. Metastatic fractures of long limb bones. Orthop. Traumatol. Surg. Res. 2017 Feb. 103(1S). S41-S51. doi: 10.1016/j.otsr.2016.11.001. Epub 2017 Jan 11. PMID: 28089230.
17. Lenze U., Knebel C., Lenze F. et al. Endoprothetischer Totalersatz von Femur, Humerus und Tibia. Orthopäde. 2019. 48. 555-562. doi: 10.1007/s00132-019-03762-1.
18. Windhager R. CORR Insights®: Outcomes of a Modular Intercalary Endoprosthesis as Treatment for Segmental Defects of the Femur, Tibia, and Humerus. Clin. Orthop. Relat. Res. 2016 Feb. 474(2). 549-50. doi: 10.1007/s11999-015-4635-9. Epub 2015 Nov 19. PMID: 26584801; PMCID: PMC4709279.
19. Проценко В.В., Дуда Б.С. Переваги модульного ендопротезування колінного суглоба у хворих із пухлинами кісток. Онкология. 2015. 17(2). 129-133. http://nbuv.gov.ua/UJRN/OL_2015_17_2_11.
20. Guzik G. Oncological and functional results after surgical treatment of bone metastases at the proximal femur. BMC Surg. 2018 Jan 25. 18(1). 5. doi: 10.1186/s12893-018-0336-0. PMID: 29370790; PMCID: PMC5784608.
21. Nilsson J., Gustafson P. Surgery for metastatic lesions of the femur: good outcome after 245 operations in 216 patients. Injury. 2008 Apr. 39(4). 404-10. doi: 10.1016/j.injury.2007.07.006. Epub 2007 Nov 9. PMID: 17996870.
22. Ferreira S., Dormehl I., Botelho M.F. Radiopharmaceuticals for bone metastasis therapy and beyond: a vo-yage from the past to the present and a look to the future. Cancer Biother. Radiopharm. 2012 Nov. 27(9). 535-51. doi: 10.1089/cbr.2012.1258. Epub 2012 Oct 17. PMID: 23075374.

/76.jpg)
/77.jpg)
/78.jpg)