Международный эндокринологический журнал Том 15, №1, 2019
Вернуться к номеру
Роль фракталкіну в розвитку діабетичного макулярного набряку у хворих на цукровий діабет 2-го типу
Авторы: Кирилюк М.Л.(3), Сук С.А.(1, 2), Риков С.О.(1), Могілевський С.Ю.(1)
1 - Національна медична академія післядипломної освіти імені П.Л. Шупика МОЗ України, м. Київ, Україна
2 - Київська міська клінічна офтальмологічна лікарня, м. Київ, Україна
3 - Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
Актуальность. Диабетический макулярный отек (ДМО) — серьезное осложнение сахарного диабета (СД) и ведущая причина потери зрения у работоспособного населения большинства развитых стран. Цель исследования: изучить особенности содержания фракталкина в сыворотке крови и провести анализ связи фракталкина с толщиной слоев макулы при разных формах ДМО у больных СД 2-го типа. Материалы и методы. Исследования проведены у 82 больных СД 2-го типа (145 глаз), разделенных на 4 группы в соответствии с формой ДМО. Результаты получены с помощью однофакторного дисперсионного и регрессионного анализа, методикой построения логистических моделей регрессии. Результаты. Фракталкин крови не ассоциируется как с риском ненизкого значения (значения больше QI) толщины слоя нервных волокон, слоя ганглионарных клеток, внутреннего пограничного слоя, центральной толщины сетчатки, объема макулы и центральной ямки, так и с общим высоким риском ухудшения состояния макулы. Выводы. Фракталкин представляет собой новый перспективный терапевтический метод лечения диабетических заболеваний сетчатки.
Актуальність. Діабетичний макулярний набряк (ДМН) — серйозне ускладнення цукрового діабету (ЦД) і провідна причина втрати зору у працездатного населення більшості розвинених країн. Мета дослідження: вивчити особливості вмісту фракталкіну в сироватці крові та провести аналіз зв’язку фракталкіну із товщиною шарів макули при різних формах ДМН у хворих на ЦД 2-го типу. Матеріали та методи. Дослідження проведені у 82 хворих на ЦД 2-го типу (145 очей), розділених на 4 групи відповідно до форми ДМН. Результати отримані за допомогою однофакторного дисперсійного і регресійного аналізу, методикою побудови логістичних моделей регресії. Результати. Фракталкін крові не асоціюється як із ризиком ненизького значення (значення більші QI) товщини шару нервових волокон, шару гангліонарних клітин, внутрішнього граничного шару, центральної товщини сітківки, об’єму макули та центральної ямки, так і з загальним високим ризиком погіршення стану макули. Висновки. Фракталкін являє собою новий перспективний терапeвтичний засіб лікування діабетичних захворювань сітківки.
Background. Diabetic macular edema (DME) is a severe complication of type 2 diabetes mellitus (DM) and a leading cause of vision loss in the working age population of most developed countries. The gold standard for DME treatment should be based on a good control of glycemia along with control of lipids and renal function. However, despite the systemic metabolic control values being essential for patients with diabetic retinopathy, it has proven to be insufficient for DME if it appears. In these patients, additional measures are needed in order to avoid the subsequent loss of vision. The aim of the work was to assess the content of blood fractalkine in patients with type 2 DM and DME in conjunction with the indicators of the thickness of the macula layers. Materials and methods. The study involved 82 patients with type 2 DM (145 eyes), divided into 4 groups in accordance with the DME form. The average age of patients was 65.25 ± 10.85 years, the average duration of DM — 14.00 ± 7.05 years, the average level of HbA1c — 8.40 ± 1.58 %. Results. Using analysis of variance and regression analysis, methods for constructing logistic regression models, we have shown that fractalkine is not associated with the risk of not low values (> QI) of nerve fiber layer, ganglion cell layer, inner plexiform layer, central sector of macula, thickness of fovea. Conclusions. Fractalkine may be a promising new therapeutic method for the treatment of diabetic retinal diseases. DME tends to be a chronic disease, although spontaneous recovery is not uncommon. It is important to recognize that 35 % of patients with macular edema had spontaneous resolution after 6 months if untreated.
сахарный диабет; фракталкин; диабетический макулярный отек
цукровий діабет; фракталкін; діабетичний макулярний набряк
diabetes mellitus; fractalkine; diabetic macular edema
Вступ
Діабетичний макулярний набряк (ДМН) є серйозним ускладненням цукрового діабету (ЦД) і провідною причиною втрати зору у працездатного населення більшості розвинених країн [1, 2]. Макулярний набряк присутній загалом у 25 % хворих на ЦД, залишається клінічною ознакою, найбільш тісно асоційованою із потовщенням центральної ямки (визначається на оптичній когерентній томографії) і просочуванням флуоресцеїну (виявляється при ангіографічних дослідженнях) [3].
Нормальний зір потребує скоординованої клітинно-клітинної комунікації серед резидентних ней–ронів сітківки, клітин Мюллера, астроцитів. Тому, незважаючи на наявність за ЦД судинних аномалій у вигляді діабетичної ретинопатії (ДР), втрата клітин у нейронній сітківці підтримує думку про діабетичне ураження сітківки в тому числі і як про нейродегенеративне захворювання [4]. Так, мікрогліальна активація спостерігається в експериментальних моделях ранньої (початкової) ДР [5, 6], а дослідження in vitro показують, що гліковані сполуки, які вступають в реакцію з мікроглією, сприяють активації клітин мікроглії та індукують виділення прозапальних цитокінів [7]. При цьому внесок мікроглії в опосередковане запаленням пошкодження сітківки за ЦД ще недостатньо зрозумілий.
Розвиток будь-якої запальної реакції, у тому числі неспецифічної, яка спостерігається за ЦД 2-го типу, ініціює каскад різних імунологічних реакцій, значиму роль в якому відіграють гормони жирової тканини [8, 9] та цитокіни, що відповідають за активацію, проліферацію і хемотаксис. Ці невеликі за розміром білки отримали назву «хемокіни» через здатність викликати так званий спрямований хемотаксис [10]. Одним із членів великої родини хемокінів є хемокін CX3CL1, або фракталкін (названий так завдяки своїй фрактальній геометрії).
Фракталкін експресується на мембранах здорових нейронів, і його сигнали до мікроглії опосередковуються унікальним хемокіновим рецептором CX3CR1, відомим як пов’язаний з G-білком рецептор 13 (GPR13). CX3CR1 — білок, який у людини кодується геном CX3CR1 [11]. Фракталкін впливає на розчинний домен хемоатрактантів і через CX3CR1 активується на клітинах макрофагах мікроглії та інших периферичних лейкоцитах [12]. Його унікальність забезпечується наявністю у нього фіксованої і розчинної форм. У мембранозв’язаному стані фракталкін проявляє властивості молекули адгезії на ендотеліальних і епітеліальних клітинах [13]. Розчинний хемокіновий домен людського фракталкіну є хемотаксичним для Т-клітин і моноцитів. Фракталкін підсилює міграцію лейкоцитів з кров’яного русла в тканини за рахунок підвищення селектин-опосередкованого зв’язування, викликаючи адгезію і, в кінцевому підсумку, міграцію лейкоцитів через шар ендотеліальних клітин.
В експерименті виявлено зменшення розчинного фракталкіну в тканинах сітківки мишей Ins2Akita-KO, зниження кількості нейронів, збільшення кількості мікроглії сітківки і посилення морфологічної активації в діабетичній сітківці мишей, у яких відсутній ген CX3CR1 (Ins2Akita CX3CR1-Wild-тип мишей) [14]. В клінічній офтальмології були спроби дослідження рівня фракталкіну в рідкій волозі очей разом з епідермальним фактором росту, фактором росту фібробластів 2, трансформуючим фактором росту α, інтерфероном-α2 і -γ, інтерлейкінами і TNF-α у взаємозв’язку з товщиною макули після інтравітреального введення ранібізумабу при ДМН [15]. Все вищевикладене говорить про необхідність подальшого вивчення ролі фракталкіну в розвитку ДМН у хворих на ЦД 2-го типу, дослідження внеску мікроглії в опосередковане запаленням пошкодження сітківки за ЦД, особливо у взаємозв’язку із товщиною шарів макули.
Мета дослідження: вивчити особливості вмісту фракталкіну в сироватці крові та провести аналіз зв’язку фракталкіну із товщиною шарів макули при різних формах діабетичного макулярного набряку у хворих на цукровий діабет 2-го типу.
Матеріали та методи
Дослідження проведені у 82 хворих на ЦД 2-го типу (145 очей), розділених на 4 групи відповідно до форми ДМН. Усім пацієнтам було проведено лабораторне (глікований гемоглобін (HbA1с), фракталкін) та комплексне офтальмологічне обстеження. Середній вік пацієнтів становив 65,25 ± 10,85 року, середня тривалість ЦД — 14,00 ± 7,05 року (± SD), середній рівень HbA1с — 8,40 ± 1,58 % (± SD). При визначенні форми ДМН ми віддавали перевагу класифікації Американської академії офтальмології [16]. Відповідно до цієї класифікації ми розділили хворих з ДМН на 4 групи: 0 — ДМН відсутній, 1 — ДМН легкий, 2 — ДМН помірний, 3 — ДМН тяжкий.
Критеріями включення у відкрите дослідження були добровільна інформована згода на участь у дослідженні, вік понад 18 років, наявність ЦД 2-го типу. Критеріями невключення були вагітність, наявність ендокринних захворювань, що призводять до ЦД за типом 2 при ендокринопатіях (синдром Кушинга, диспітуїтаризм, синдром полікістозних яєчників, спадкові ендокринопатії), ЦД 1-го типу, гострі інфекційні захворювання, онкологічні захворювання (в тому числі в анамнезі), декомпенсація коморбідної патології, психічні розлади, прийом нейролептиків, антидепресантів, наявність протеїнурії, пошкодження зорового нерва, глаукоми і зрілої катаракти.
Концентрацію фракталкіну в сироватці крові визначали методом імуноферментного аналізу за допомогою набору для кількісного визначення фракталкіну людини RayBio® Human Fractalkine ELISA Kit Protocol фірми Ray Biotech, Inc (США) з використанням аналізатора IEMS Reader MF (Labsystems, Фінляндія).
Офтальмологічне обстеження включало візо–метрію, периметрію, тонометрію, рефрактометрію, біомікроскопію, гоніоскопію, офтальмоскопію, оптичну когерентну томографію з ангіографією, фундусскопію (з фотографуванням очного дна). Для аналізу були використані такі інструментальні показники: товщина шару нервових волокон (nerve fibre layer — NFL), шару гангліонарних клітин (ganglion cell layer — GCL), внутрішнього граничного шару (inner posterior layer — IPL), центральна товщина сітківки (central sector), об’єм макули (volume macula) та центральної ямки (volu–me fovea), мінімальна товщина центральної ямки (minimum in fovea), середня товщина макули (area thickness).
Статистичний аналіз результатів дослідження здійснювався в пакеті MedCalc v. 18.11 (MedCalc Software Inc, Broekstraat, Бельгія), включав однофакторний дисперсійний і регресійний аналіз. Аналіз результатів дослідження проводився також з використанням статистичного пакета EZR v. 1.35 (Saitama Medical Center, Jichi Medical University, Saitama, Японія), що представляє графічний інтерфейс до R (The R Foundation for Statistical Computing, Vienna, Австрія). При проведенні статистичного аналізу використано критерій Крускала — Уолліса, критерій порівняння Бартлетта, метод побудови логістичних моделей регресії. Ступінь і напрямок зв’язку факторних і результуючої ознак оцінювалися за показником відношення шансів (ВШ), розраховувався 95% довірчий інтервал (ДІ) показника [17–19]. Критичний рівень статистичної значимості відмінностей p < 0,05.
Результати
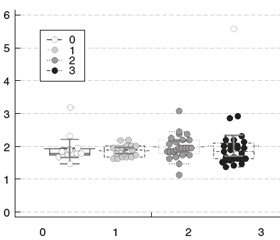
Вміст фракталкіну в сироватці крові в пацієнтів з ЦД 2-го типу при різних формах ДМН подано на рис. 1.
При проведенні статистичного аналізу концентрації фракталкіну в сироватці крові (центрів розподілу) не було виявлено відмінностей за медіанним значенням між пацієнтами чотирьох груп (p = 0,50 за критерієм Крускала — Уолліса).
При проведенні порівняння ступеня варіабельності (дисперсії) показників рівня фракталкіну в крові для пацієнтів чотирьох груп нами не виявлено статистично значимої відмінності між групами (p = 0,06 за критерієм Бартлетта). У той же час слід зазначити, що варіабельність показника (стандартне відхилення SD = 0,64 нг/мл) для умовно об’єднаної групи ДМН 2–3 було статистично значимо вище, ніж в іншій умовно об’єднаній групі ДМН 0–1 (стандартне відхилення SD = 0,31 нг/мл) (p = 0,003, F = 4,3, дисперсія вища більше ніж в 4 рази).
Для аналізу зв’язку рівня показників фракталкіну із непогіршенням стану макули за даними NFL, GCL, IPL, центральної товщини сітківки (central sector), об’єму макули (volume macula) та центральної ямки (volume fovea), мінімальної товщини центральної ямки (minimum in fovea), середньої товщини макули (area thickness) були використані методи побудови та аналізу однофакторних моделей регресії.
Аналіз зв’язку вмісту фракталкіну в крові із товщиною NFL + GCL + IPL. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат NFL + GCL + IPL > 115 мкн (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (> 115 мкн) значення товщини NFL + GCL + IPL. У табл. 1 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з шансом наявності ненизького значення товщини NFL + GCL + IPL (p > 0,05).
Аналіз зв’язку із NFL. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат NFL > 31 мкн (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (NFL > 31 мкн) значення NFL. У табл. 2 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з шансом наявності ненизького значення товщини NFL (p = 0,97).
Аналіз зв’язку із GCL. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат GCL > 84 мкн (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (GCL > 84 мкн) значення товщини GCL. У табл. 3 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з шансом наявності ненизького значення товщини GCL (p > 0,05).
Аналіз зв’язку із minimum in fovea. При проведенні аналізу негативним (вихідна змінна Y = 1) прий–нято результат мінімального значення товщини fovea > 195 мкн (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику наявності ненизького (minimum in fovea > 195 мкн) значення мінімальної товщини центральної ямки. У табл. 4 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з шансами наявності ненизького мінімального значення товщини fovea (p > 0,05).
Аналіз зв’язку із central sector. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат central sector ≥ 248 мкн (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (central sector ≥ 248 мкн) значення товщини central sector. У табл. 5 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з ризиком ненизького значення товщини central sector (p > 0,05).
Аналіз зв’язку із area thickness. При проведенні аналізу негативним (вихідна змінна Y = 1) прий–нято результат area thickness > 284 мкн (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (area thickness > 284 мкн) значення товщини area thickness. У табл. 6 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з ризиком ненизького значення товщини area thickness (p > 0,05).
Аналіз зв’язку із volume macula. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат volume macula > 8,03 мм3 (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (volume macula > 8,03 мм3) значення volume macula. У табл. 7 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з ризиком ненизького значення volume macula (p > 0,05).
Аналіз зв’язку із volume fovea. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат volume fovea > 0,19 мм3 (значення більші QI), інакше Y = 0. Таким чином проводився аналіз ризику ненизького (volume fovea > 0,19 мм3) значення volume fovea. У табл. 8 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено зв’язку рівня фракталкіну з ризиком ненизького значення volume fovea (p > 0,05).
Аналіз зв’язку із загальним ризиком. При проведенні аналізу негативним (вихідна змінна Y = 1) прийнято результат, коли негативний результат був за ≥ 4 показниками, інакше Y = 0. Таким чином проводився аналіз ймовірності високого загального ризику. У табл. 9 наведені результати однофакторного аналізу.
При проведенні аналізу не виявлено вірогідного зв’язку рівня фракталкіну з високим значенням загального ризику погіршення стану макули (p > 0,05).
Обговорення
Власні результати дослідження концентрації фракталкіну в сироватці крові хворих на ЦД 2-го типу показали відсутність вірогідних відмінностей (за критерієм Крускала — Уолліса) центрів розподілу фракталкіну між пацієнтами із різними формами ДМН порівняно із діабетичними пацієнтами без ДМН.
Але спостерігається зміщення вгору центрів розподілу рівнів фракталкіну в крові із збільшенням тяжкості ДМН, про що опосередковано свідчить вірогідне зростання (в 4 рази) дисперсії рівнів фракталкіну із збільшенням тяжкості ДМН. Середній рівень концентрації фракталкіну в сироватці крові у наших дослідженнях відповідає результатам дослідження фракталкіну у хворих із ускладненим ЦД 2-го типу та ожирінням (0,989–1,031 нг/мл) [20].
В нашій роботі показано, що у хворих на ЦД 2-го типу вміст фракталкіну в крові не асоціюється із загальним високим ризиком погіршення стану макули та із ризиком ненизького значення (значення більші QI) товщини шару нервових волокон, шару гангліонарних клітин, внутрішнього граничного шару, центральної товщини сітківки, об’єму макули та центральної ямки, мінімальної товщини центральної ямки, середньої товщини макули.
Показано, що інтравітреальне введення рекомбінантного фракталкіну мишам з діабетом знижує осадження фібриногену і периваскулярну кластеризацію мікроглії в сітківці при системному запаленні. Ці дані свідчать про те, що дерегуляція мікрогліальної активації за допомогою втрати сигналу фракталкін/CX3CR1 порушує цілісність судин у сітківці при системному запаленні [21]. Потенційні переваги застосування фракталкіну являють собою перс–пективний сценарій для лікування діабетичних та інших захворювань сітківки [14].
Висновки
1. У хворих на ЦД 2-го типу вміст фракталкіну в крові не асоціюється із ризиком ненизького значення (значення більші QI) товщини шару нервових волокон, шару гангліонарних клітин, внутрішнього граничного шару, центральної товщини сітківки, об’єму макули та центральної ямки, мінімальної товщини центральної ямки, середньої товщини макули та із загальним високим ризиком погіршення стану макули.
2. У хворих на ЦД 2-го типу із збільшенням тяжкості ДМН вірогідно (p = 0,003) у 4 рази зростає дисперсія рівнів фракталкіну в крові.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.

/12-1.jpg)
/12-2.jpg)
/13-1.jpg)