Журнал «» №4 (60), 2018
Вернуться к номеру
Матеріали Міжнародного симпозіуму «Оцінка функції та структури артерій — клінічні аспекти» (м. Одеса, 30–31 травня — 1 червня 2018 року) - Оцінка жорсткості артерій: огляд методів і приладів
Авторы: Торбас О.О.
ДУ «ННЦ «Інститут кардіології ім. акад. М.Д. Стражеска» НАМН України», м. Київ, Україна
Рубрики: Кардиология
Разделы: Медицинские форумы
Версия для печати
Протягом останніх десятирічь ми спостерігаємо бурхливий розвиток новітніх високотехнологічних методів діагностики та лікування пацієнтів із артеріальною гіпертензією (АГ). Як результат — багато в чому наші знання про патогенез і перебіг цього захворювання значно змінилися, з’явилися нові цікаві дані стосовно впливу відомих представників різних груп антигіпертензивної терапії, у певному сенсі змінився підхід до оцінки серцево-судинного ризику. Удосконалення технологій аналізу пульсової хвилі (ПХ) та широке впровадження цього методу у наукову діяльність відігравало велику роль у поглибленні наших знань про проблему ураження судин як органа-мішені, а також дозволило розробити нові терапевтичні підходи і, як результат, покращити прогноз у багатьох пацієнтів із АГ. Проте останнім часом такі прилади почали набувати все більшої популярності не лише в межах наукових розробок, але і в умовах реальної клінічної практики, адже надають практичному лікарю унікальну інформацію, на основі якої можливо не лише оптимізувати, але й індивідуалізувати лікування, більш чітко оцінити прогноз, виявити ознаки ураження органів-мішеней на субклінічному етапі та, що найголовніше, якомога раніше зупинити прогресування ускладнень АГ, забезпечити набагато більшу органопротекторну дію призначеної терапії. Основні причини того, чому ця методика стає дедалі популярнішою, — сучасні прилади доступні за ціною, прості у використанні, із доволі зрозумілим програмним забезпеченням, але при цьому забезпечують високу точність діагностики, майже виключаючи вплив людського фактора на якість виконання обстеження. Саме тому в умовах сучасної діяльності лікаря важливо розуміти принцип роботи таких приладів, особливості кожного із них, а головне — які показники можливо отримати за допомогою кожної з методик.
Взагалі принцип роботи всіх діагностичних приладів схожий. Є три блоки: блок введення інформації від пацієнта, блок обробки даних і блок виведення інформації оператору (рис. 1). Прилади, що надалі будуть розглядатися, як інформацію від пацієнта використовують вихідний сигнал пульсової хвилі. Блок обробки даних, як правило, вміщує в себе методи швидкісного та контурного аналізу ПХ (рис. 1), що виконується за допомогою спеціального програмного забезпечення. У багатьох сучасних приладах обидві ці методики поєднані в одному приладі. Виведення інформації у даному випадку абсолютно стандартне — інформація виводиться на монітор та/або друкується на паперовому носії.
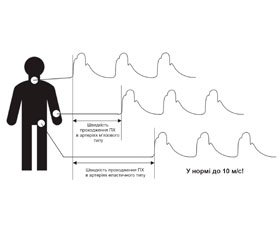
Перша методика швидкісного аналізу пульсової хвилі — це оцінка швидкості поширення пульсової хвилі (ШППХ) у різних сегментах артеріального дерева. Цей метод з’явився найпершим і на сьогодні має найбільшу доказову базу. На рис. 2 схематично зображено реєстрацію всіх трьох хвиль пульсу одночасно за допомогою еталонного приладу Complior, детальний опис якого буде наведено нижче.
Залежно від того, який тип артерій домінує на сегменті, що вивчається, — крупні еластичні або дрібні м’язові, розрізняють ШППХ по артеріях еластичного і м’язового типу. Норми ШППХ в артеріях еластичного типу встановлюються індивідуально, відповідно до віку пацієнта, дані про які були попередньо отримані у популяційних дослідженнях. Однак доведено, що збільшення цього показника понад 10 м/с в осіб усіх вікових груп пов’язане із достовірним зростанням серцево-судинного ризику.
У літературі ШППХ в артеріях еластичного типу часто називають методом оцінки жорсткості артерій. Але чому ШППХ може бути методом діагностики стану судинної стінки? І як взагалі ці поняття взаємопов’язані? Щоб це зрозуміти, розглянемо на прикладі моделей із використанням основних законів фізики, причому всі швидкісні показники зобразимо схематично за допомогою векторів (рис. 3).
У нас є дві артерії: одна більш еластична (рис. 3А), інша — більш жорстка (рис. 3Б). Припустимо, сила скорочення серця — константа, а тому вихідний вектор швидкості однаковий. Проте частина кінетичної енергії буде йти у бік судинної стінки. Якщо судина еластична, то ця енергія буде витрачатися на її розтягнення і формування пульсової хвилі, а отже, результуючий вектор буде коротший і ШППХ буде меншою. Якщо судина більш жорстка, то енергії витрачається менше, результуючий вектор буде довшим, а отже, і ШППХ буде вищою. А тому чим вище швидкість пульсової хвилі, тим більш жорсткою є стінка артерії. Також слід зазначити, що зростання ШППХ в артеріях еластичного типу є показником субклінічного ураження органа-мішені артерій, що, як правило, виникає найпершим. Проте цей стан оборотний. Швидкість пульсової хвилі в артеріях еластичного типу починає знижуватися після 6 місяців регулярного прийому ефективної антигіпертензивної терапії при умові повноцінного контролю артеріального тиску (АТ). А тому починати оцінювати динаміку цього показника більш раціонально не раніше ніж через півроку після початку лікування.
Інша методика — це методика контурного аналізу пульсової хвилі. Тобто метод, що дозволяє за контуром пульсового сигналу проводити розрахунки основних параметрів гемодинаміки в аорті неінвазивно. На рис. 4 наведено контур пульсового сигналу, а також зображено основні параметри, які можна розраховувати шляхом такого аналізу.
Отриманий контур пульсового сигналу насправді дуже нагадує сфігмограму. Тут також можна побачити зубець А, зубець В і дикротичну виїмку. Але це не зовсім вірно. Сфігмограма — це графічне зображення фаз змін тиску в середині аорти за даними катетеризації, хоча цей графік дуже схожий на контур пульсової хвилі. Контур, що використовується в даному випадку, — це графік коливання стінки аорти.
Але саме на цьому принципі і базується метод. У ХХ ст. із використанням сфігмографії та сфігмоманометрії Barnett та співавтори проводили одночасну реєстрацію хвиль зміни діаметра артерії та зміну тиску у ній (рис. 5). Виявилося, що коливання стінки артерії відбуваються майже однаково до фаз змін тиску, оскільки стінка артерії поводить себе як чисто пружній матеріал, майже не виявляючи гістерезису. А тому і контур обох хвиль абсолютно однаковий. Тобто, аби виміряти тиск в аорті, достатньо зареєструвати коливання її стінки без необхідності катетеризації самої аорти.
Тим не менш у реальних клінічних умовах записати коливання стінки аорти так само важко, як і виконати катетеризацію аорти та прямим методом виміряти тиск у ній. І тут на допомогу прийшло інше відкриття — ампліфікації пульсової хвилі (рис. 6).
Ампліфікація пульсової хвилі — це явище, суть якого полягає у тому, що чим далі від серця прямує пульсова хвиля, тим вищою стає її амплітуда. З точки зору фізіології, такий механізм можна пояснити тим, що в артеріях середнього калібру з’являється велика кількість гладком’язових клітин, що забезпечують активне скорочення стінки артерій. Процес поширення пульсової хвилі із пасивного перетворюється на активний, а тому і амплітуда контуру пульсового сигналу стає вищою. Явище ампліфікації пульсової хвилі також було покладено в основу методології неінвазивного вимірювання центрального АТ (ЦАТ). Адже, знаючи контур пульсового сигналу на артерії, де його не важко зареєструвати (радіальній або брахіальній), а також знаючи крок ампліфікації (розраховується автоматично за зростом пацієнта), величину ампліфікації (розраховується емпірично за віком пацієнта), можна змоделювати контур хвилі в аорті та розрахувати значення тиску у ній. Але варто зазначити, що ампліфікація пульсової хвилі більш виражена у молодих осіб. У молодих осіб високого зросту різниця між рівнями центрального і брахіального АТ може бути досить суттєвою, а тому, відповідно до сучасних рекомендацій із ведення хворих з АГ, у таких осіб потрібно вимірювати неінвазивно рівень центрального АТ з метою верифікації діагнозу та визначення тактики терапії. У людей похилого віку амплітуди всіх хвиль будуть майже однакові, а тому і рівень центрального тиску буде приблизно відповідати рівню брахіального АТ.
У цілому центральний систолічний АТ — це найперший і найважливіший показник, який можна –отримати за допомогою контурного аналізу пульсової хвилі. У багатьох дослідженнях було продемонстровано, що саме рівень центрального систолічного АТ більше пов’язаний із ураженням органів-мішеней [1] та погіршенням прогнозу у пацієнтів із АГ [2, 3]. На даний момент було встановлено, що рівень центрального АТ вище 125 мм рт.ст. асоціюється із погіршенням прогнозу у пацієнтів із АГ, а тому референтною нормою вважають рівень ЦАТ нижче за 125 мм рт.ст. Достовірних даних, які допомогли б визначити нижню границю норми ЦАТ, на сьогодні наведено мало.
Наступним також добре доведеним і важливим показником, що також можна розрахувати шляхом контурного аналізу пульсової хвилі, є індекс аугментації. Аугментація центрального тиску — це додаткове зростання рівня АТ в аорті при поверненні відбитої від периферії хвилі пульсу. Пульсова хвиля, утворившись в систолу, прямує до периферії і там в місцях зменшення калібру та розгалуження артерій відбивається і повертається в аорту. Якщо відбита хвиля встигає повернутися у систолу, вона підвищує рівень центрального АТ. Пульсова хвиля повертається у систолу також при підвищенні тонусу периферичних артерій, коли діаметр артерій стає меншим, а точка відбиття пульсової хвилі наближається до серця. На практиці використовують індекс аугментації пульсової хвилі, що виражається у відсотках та демонструє, яка частка у підвищенні ЦАТ належить відбитій хвилі. Нормативні показники індексу аугментації залежать від віку [4–6], що наведено в табл. 1.
У ході виконання наукових або популяційних досліджень також визначають і тривалість викиду, що розраховується за даними контурного аналізу пульсової хвилі та виражається у відсотках. Цей показник демонструє тривалість систолічної частини пульсового сигналу до моменту настання аугментації. Нормативні показники [7] наведено у табл. 2.
Дуже цікавим, але мало доведеним і менш уживаним є такий показник, як субендокардіальний індекс життєздатності — параметр, що демонструє гемодинамічну ефективність діастоли в плані забез-печення коронарного кровообігу. Для його розрахунку використовують площу понад кривою пульсового сигналу, з якого розраховують співвідношення частин систоли та діастоли. Причому чим вище цей показник, тим краще забезпечення коронарного кровотоку в діастолу. Нормальним вважається показник індексу від 130 до 200 %.
Багато приладів надають додаткові параметри контурного аналізу. Але вони, як правило, не використовуються на практиці, проте можуть допомогти краще зрозуміти рівень гемодинамічних порушень у, наприклад, наукових дослі–дженнях.
На сьогодні на ринку представлено багато апаратів, що використовуються для оцінки жорсткості артерій і вимірювання центрального АТ. Кожен із них має як переваги, так і недоліки, які варто розглянути окремо.
1. Система SphygmoCor, AtCor, Австралія. Цей прилад для реєстрації контура пульсового сигналу використовує методику апланаційної тонометрії, тобто датчик реєструє зміну тиску на нього при проходженні пульсової хвилі, у той час як артерія притиснена до кістки. У цьому приладі у датчик вбудовано п’єзоелемент, подібний до того, який використовується для апаратів ультразвукової діагностики. А тому він є одним із найбільш дорогих. Використання такої технології забезпечує надзвичайно високу якість контурного аналізу пульсової хвилі, і на сьогодні, за даними міжнародного метааналізу, цей прилад визнано золотим стандартом вимірювання рівня АТ в аорті.
2. Система Complior, Alam, Франція. Діагностичне дослідження в даному випадку також базується на основі методу апланаційної тонометрії, але замість п’єзодатчиків розробники використали еластичні мембрани. При цьому усі три датчики встановлюються одночасно і реєструють хвилі пульсу також одночасно. Такий спосіб є найбільш оптимальним для оцінки швидкісних параметрів пульсової хвилі, а тому, за даними того ж метааналізу, цей прилад було визнано золотим стандартом вимірювання жорсткості артерій.
3. Система для амбулаторного моніторування АТ, вимірювання центрального АТ та жорсткості артерій Mobil-O-Graph, I.E.M. GmbH, Німеччина. Даний прилад реєструє хвилі пульсу шляхом оцінки осциляцій на брахіальній артерії, що реєструються під час звичайного манжеткового вимірювання АТ. Система має доволі зрозумілий інтерфейс та, окрім стандартних показників добового моніторування, дозволяє оцінити середньодобовий (а також денний і нічний) центральний АТ, індекс аугментації, ШППХ та ступінь резистентності периферичних артерій.
4. Система для амбулаторного моніторування АТ, вимірювання центрального АТ та жорсткості артерій BpLab (МнСДП), ООО «Петр Телегин», Росія. Як і попередня, ця система також доповнює стандартні показники добового моніторування АТ даними контурного та швидкісного аналізу пульсової хвилі. Особливості даного приладу полягають у тому, що в експертному режимі звіту система дозволяє оцінити ще низку необхідних клінічних параметрів, як, наприклад, дані хронобіологічного аналізу, ранкової динаміки АТ та багато іншого.
5. Система для офісного вимірювання центрального артеріального АТ та жорсткості артерій ВАТ 41-2 на базі програмного забезпечення «Аріада+». На сьогодні цей апарат є найбільш дешевим і доступним в Україні, його було сконструйовано на базі стандартної системи для моніторування добового АТ, при цьому розробникам вдалося підвищити чутливість датчиків удвічі. Клінічне дослідження валідації приладу проводилося на базі відділу симптоматичних гіпертензій ДУ «ННЦ «Інститут кардіології ім. акад. М.Д. Стражеска», результати його були опубліковані раніше в журналі «Артеріальна гіпертензія». Однак програмне забезпечення «Аріада+» дозволяє лише офісне вимірювання цих параметрів. Добове моніторування центрального АТ та жорсткості на даний момент ще не розроблено.
6. Апарат для оцінки індексу CAVI, VaSera 1500, Fukuda Denshi, Японія. Окремо слід розглянути такий метод вимірювання еластичності судин, як Cardio Ankle Vascular Index, або індекс CAVI. Цей показник також дозволяє оцінити жорсткість судин, але його принципова відмінність від ШППХ полягає у тому, що на відміну від нього у алгоритмі обчислення CAVI-індексу не використовується рівень брахіального АТ. І тому отриманий показник дозволяє оцінити стан артерій більш об’єктивно. На сьогодні методика широко використовується у клінічній практиці Японії, у Європі прилад використовують у великих популяційних дослідженнях.
Тепер розглянемо додаткові методики, які також дозволяють оцінити жорсткість артерій, але в силу високої вартості або надзвичайної складності не набули широкого визнання у науковій і медичній спільноті. Перший — це метод ультразвукового відстеження зміни діаметра артерій. Перші роботи з цього приводу датуються 2009 роком. За майже 9 років існування даної методики можна підбити певні підсумки: метод не увійшов до клінічної практики, більш того, має досить слабку доказову базу, а тому не може витіснити еталонний метод оцінки жорсткості судин.
Наступна методика відносно нова і викликає певний інтерес у світової спільноти — оцінка жорсткості артерій за допомогою 4D-фазової контрастної магнітно-резонансної томографії (МРТ). Але, без сумнівів, використовувати МРТ суто для оцінки жорсткості судин недоцільно. Таким аналізом доповнюють стандартну МРТ для більш детальної діагностики стану пацієнта. Взагалі це надзвичайно потужна і цікава методика, що дозволяє оцінити структуру різних об’єктів. Але надзвичайно висока вартість обстеження поки що є основним бар’єром до широкого впровадження методу у практичну діяльність як у Європі, так і в Україні.
Отже, як можна зрозуміти, новітні методики дійсно необхідні в сучасній клінічній практиці. Проте кожен із доступних нині приладів має як сильні сторони, так і певні недоліки. А тому робити вибір на користь кожного окремого апарата варто, лише виходячи із власних потреб і напрямку діяльності клініки. Наводимо табл. 3, у якій представлено порівняльну характеристику всіх приладів, про які говорилося вище.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Roman M.J., Devereux R.B., Kizer J.R. et al. Central pressure more strongly relates to vascular disease and outcome than does brachial pressure: the Strong Heart Study // Hypertension. — 2007 Jul. — № 50(1). — Р. 197-203.
2. Roman M.J., Devereux R.B., Kizer J.R. et al. High central pulse pressure is independently associated with adverse cardiovascular outcome the strong heart study // J. Am. Coll. Cardiol. — 2009 Oct 27. — № 54(18). — Р. 1730-4.
3. Morgan T., Lauri J., Bertram D. et al. Effect of different antihypertensive drug classes on central aortic pressure // Am. J. Hypertens. — 2004 Feb. — № 17(2). — Р. 118-23.
4. Wilkinson I.B., MacCallum H., Flint L. et al. The influence of heart rate on augmentation index and central arterial pressure in humans // J. Physiol. — 2000 May 15. — № 525 (Pt. 1). — Р. 263-70.
5. Wilkinson I.B., Cockcroft J.R., Webb D.J. Pulse wave analysis and arterial stiffness // J. Cardiovasc. Pharmacol. — 1998. — № 32(Suppl. 3). — S33-7.
6. Wilkinson I.B., Fuchs S.A., Jansen I.M. et al. Reprodu-cibility of pulse wave velocity and augmentation index measured by pulse wave analysis // J. Hypertens. — 1998 Dec. — № 16(12, Pt. 2). — Р. 2079-84.
7. Weissler A.M., Harris L.C., White G.D. Left ventricular ejection time index in man // J. Appl. Physiol. — 1963 Sep. — № 18. — Р. 919-23.

/55-1.jpg)
/55.2.jpg)
/56-1.jpg)
/56-2.jpg)
/57-1.jpg)
/57-2.jpg)
/58-1.jpg)
/59-1.jpg)