Вступ
За останнє десятиріччя відмічається неухильне зростання частоти алергічної патології, від якої нині страждає близько 15–25 % дитячої популяції [1, 4–6]. Спостерігаються значне її помолодшання й тенденція до почастішання тяжких клінічних форм, резистентних до традиційних методів лікування.
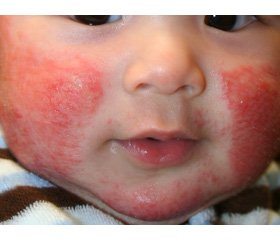
У дітей раннього віку найчастіше зустрічається атопічний дерматит (АД) як прояв харчової алергії. З віком спектр сенсибілізації розширюється за рахунок побутових, пилкових, грибкових та епідермальних алергенів, що клінічно проявляється ураженням респіраторного тракту.
Зростання захворюваності на АД у всьому світі пов’язане з несприятливим впливом багатьох факторів сучасної цивілізації.
Поширеність патології в розвинутих країнах Західної Європи серед дітей віком до 14 років становить 10–20 %. Серед дітей в європейських країнах, які народились до 1960 року, поширеність АД становила від 1,4 до 3,1 %, у період 1960–1970 рр. — 3,8–8,8 %, а після 1970 року зросла до 20,4 % [7, 13].
Дебют захворювання найчастіше має місце в ранньому дитячому віці. У дітей АД вперше проявляється до 6 місяців у 45 % випадків, протягом першого року життя — у 60 % і до 5 років — у 85 % випадків [2, 4, 13].
За даними офіційної статистики, частота атопічного дерматиту в Україні становить 3–10 на 1000 дітей, однак результати досліджень за стандартизованою міжнародною програмою ISAAC (International Study of Asthma and Allergies in Childhood) перевищують зазначені показники в 5–10 разів [1].
Ураховуючи той факт, що атопічний дерматит та сенсибілізація до харчових продуктів є невід’ємною частиною та стартом атопічного маршу, до клінічних ознак якого відносять також алергічний риніт та бронхіальну астму, адекватне лікування даної патології заслуговує на особливу увагу.
Мультифакторний патогенез, варіабельність перебігу АД вимагають комплексного підходу до лікування.
АД характеризується клінічними проявами з боку багатьох органів і систем, зокрема ураження шлунково-кишкового тракту (ШКТ) спостерігається в 52 % хворих, респіраторні симптоми — у 32 % [2, 4].
Клінічна маніфестація ураження ШКТ відбувається вже на першому році життя у вигляді кишкових кольок, зригувань, блювоти, метеоризму, не-оформлених випорожнень [6].
Велике значення мають патологічні зміни гепатобіліарної системи, які призводять до порушення розщеплення харчових компонентів у процесі травлення, що додатково сприяє сенсибілізації [3, 8].
Урсодезоксихолева кислота (УДК) — це третинна гідрофільна нетоксична жовчна кислота, частка якої становить приблизно 3 % від загального пулу жовчних кислот людини, що має надзвичайно широкий спектр лікувальних ефектів. У разі призначення УДК у дозі 13–15 мг/кг/добу вона стає основним складовим компонентом жовчі (48 %), викликає не тільки кількісні, але і якісні її зміни, зумовлюючи реалізацію низки лікувальних властивостей препарату. Накопичені на сьогодні дані дають змогу згрупувати ефекти препарату таким чином: антихолестатичний (пригнічення надходження токсичних жовчних кислот у жовч за рахунок конкурентного захвату рецепторами у здухвинній кишці та стимуляції екзоцитозу в гепатоцитах); холеретичний (індукція бікарбонатного холерезу, що підсилює виведення гідрофобних жовчних кислот до кишечника); цитопротекторний (відновлення структури гепатоцитів за рахунок «вбудовування» УДК у фосфоліпідний шар клітинної мембрани, що забезпечує її стабілізацію й підвищує стійкість до пошкоджуючого впливу токсинів); гіпохолестеринемічний (зниження всмоктування холестерину в кишечнику, його синтезу в печінці та екскреції в жовч); літолітичний (зниження літогенності жовчі внаслідок формування рідких кристалів із молекулами холестерину, запобігання утворенню та розщепленню холестеринових каменів); імуномодулюючий, антиапоптичний; антифібротичний та антиоксидантний [8, 9, 11].
Тому застосування препарату з гепатопротекторною, холеретичною, дезінтоксикаційною дією в комплексній терапії АД є патогенетично обґрунтованим.
Метою роботи було вивчити ефективність удосконаленої за рахунок введення суспензії урсодео-ксихолевої кислоти (Укрлів) комплексної терапії в дітей раннього віку з поширеною формою атопічного дерматиту.
Матеріали і методи
Вивчення ефективності удосконаленої терапії проводилось у формі відкритого дослідження з включенням 45 пацієнтів віком від 6 місяців до 3 років, які перебували на обстеженні та лікуванні у відділенні проблем харчування та соматичних захворювань дітей раннього віку ДУ «Інститут педіатрії, акушерства і гінекології НАМН України» або були виписані з клініки та знаходились під амбулаторним спостереженням.
Пацієнти взяли участь у дослідженні після отримання письмової інформованої згоди обох батьків.
Методом простої рандомізації діти були розділені на дві групи. Пацієнти основної та контрольної груп були ідентичні за статтю, віком та тяжкістю захворювання й отримували базисну терапію, яка включала: елімінаційну дієту (суміш з екстенсивним гідролізом білка в разі алергії до білка коров’ячого молока), антигістамінний препарат L-цет сироп (у дозі 2,5 мл/добу дітям 6–12 місяців, 5 мл/добу — 1–3 років), замісну ферментотерапію (лактаза) при грудному вигодовуванні в разі недостатності лактази, топічні глюкокортикоїди, зволожуючі засоби.
Основну групу становили 25 дітей, які у складі комплексної терапії атопічного дерматиту приймали препарат урсодеоксихолевої кислоти (Укрлів) у дозі 10 мг/кг 1 раз на добу (5 мл суспензії містить урсодеоксихолевої кислоти 250 мг) упродовж 21 дня. Контрольну групу становили 20 дітей, які отримували стандартну терапію без включення в схему лікування препарату урсодеоксихолевої кислоти чи інших засобів з гепатопротекторною дією.
З метою вивчення ефективності лікування атопічного дерматиту на фоні включення в схеми терапії суспензії УДК була проведена комплексна оцінка основних клінічних та параклінічних показників у динаміці на початку і в кінці прийому препаратів.
Клінічна ефективність комплексу із застосуванням суспензії УДК оцінювали в динаміці за інтенсивністю клінічних проявів із боку шкіри (площа ураження, інтенсивність свербежу), гастроінтестинальних проявів (кишкових кольок, метеоризму, зригувань), показників ультразвукового дослідження гепатобіліарної системи.
Комплексне обстеження хворих включало:
— загальноклінічне обстеження з оцінкою алергологічного (сімейного та індивідуального анамнезу), визначення наявності зв’язку між вживанням продукту харчування та виникненням гастроінтестинальних, шкірних та респіраторних симптомів анкетним методом;
— визначення рівнів загального IgE та алергенспецифічних IgE до харчових алергенів методом імуноферментного аналізу (ІФА);
— УЗД органів черевної порожнини.
Для визначення тяжкості шкірних алергічних реакцій застосовували систему бального оцінювання ступеня тяжкості АД — SCORAD (scoring of atopic dermatitis) [2].
Результати отриманих даних обробляли статистично. Вірогідність різниць оцінювали за допомогою t-критерію Стьюдента та методом кутового перетворення Фішера. Різницю вважали вірогідною при р < 0,05.
Обробку отриманих результатів проводили загальноприйнятими математичними методами варіаційної статистики.
Усі пацієнти основної групи отримали повний курс лікування. Випадків дострокового вибування пацієнтів із дослідження не було.
Результати і обговорення
Відповідно до критеріїв залучення в дослідження всі 45 дітей (24 хлопчики та 21 дівчинка) народились доношеними, із нормальними масо-ростовими показниками. Більшість із них (32; 71,1 %) були прикладені до грудей матері в першу годину життя. П’ятеро дітей (11,1 %) народились від ускладнених вагітностей, перебіг пологів був обтяженим у 4 випадках (8,9 %), 9 (20,0 %) дітей народились шляхом кесарева розтину.
Обтяжений сімейний алергологічний анамнез відмічений у 2/3 дітей з АД, у 20 (44,4 %) — по материнській лінії, у 9 (20,0 %) — по лінії батька, у 6 (13,3 %) дітей обидва батьки мали алергічні захворювання.
Дебют АД у дітей обох груп спостереження виникав у перші 3 місяці життя на фоні вживання сумішей на основі коров’ячого молока або після введення прикорму. У дітей на грудному вигодовуванні поява клінічних симптомів АД стартувала на фоні вживання матір’ю-годувальницею продуктів харчування з алергенними властивостями (коров’ячого молока, яєць, курятини, червоних та помаранчевих овочів та фруктів).
Усі обстежені діти мали АД середньої тяжкості та тяжкої форми, яка характеризувалась хронічним рецидивним перебігом, із переважанням еритематозно-сквамозних форм середньої тяжкості та тяжких (сухість, лущення, еритема, екскоріації) та вираженим свербежем у 100 % малюків, в 11 (24,4 %) дітей із ділянками мокнуття.
Середній показник тяжкості АД за шкалою SCORAD на момент початку дослідження становив 78,77 ± 3,19 бала.
У 37 (82,2 %) дітей мали місце гастроінтестинальні прояви: зригування — у 22 (48,8 %), абдомінальний больовий синдром — у 36 (80,0 %), метеоризм — в 11 (24,4 %), неоформлені випорожнення — у 29 (64,4 %), запори — у 5 (11,1 %) дітей.
З метою визначення причинних факторів розвитку захворювання всім дітям із гастроінтестинальними та шкірними проявами харчової алергії було проведене імунологічне дослідження, яке включало визначення рівнів загального IgE, алергенспецифічних IgE-антитіл до харчових, побутових, пилкових алергенів методом імуноферментного аналізу (ІФА).
У 38 (84,4 %) малюків з АД виявлена сенсибілізація до харчових алергенів: у 22 (48,8 %) — до білків коров’ячого молока, 11 (24,4 %) дітей мали сенсибілізацію до яєчного білка, у 12 (26,7 %) виявлена сенсибілізація до алергену пшеничного борошна. Шістнадцять (35,5 %) обстежених мали сенсибілізацію до двох та більше алергенів.
Рівень загального IgE сироватки крові визначали в 38 (84,4 %) пацієнтів, підвищення його концентрації понад 2–3 норм виявлено лише в 25 (55,5 %) обстежених, 13 (28,8 %) дітей мали нормальні його показники, середнє значення загального IgE становило 68,6 МО/мл при референтних значеннях (< 45 МО/мл).
Аналіз параклінічних даних дітей з АД показав зміни з боку червоної крові у вигляді гіпохромної анемії та незначної еозинофілії в 34 (75 %) обстежених.
При інструментальному ультразвуковому дослідженні органів черевної порожнини в усіх обстежених дітей виявлено функціональні зміни з боку гепатобіліарної системи й підшлункової залози: дифузне підвищення ехогенності паренхіми печінки, помірне ущільнення стінок внутрішньопечінкових жовчних ходів і судин системи портальної вени, збільшення розмірів підшлункової залози, зниження ехогенності паренхіми, збільшення розмірів селезінки та помірне ущільнення стінок судин.
Обстеження дітей в динаміці лікування показало, що призначення пацієнтам препарату урсодеоксихолевої кислоти в суспензії у складі комплексної терапії АД (основна група) сприяє більш значному та швидкому зменшенню клінічних симптомів, як шкірних, так і гастроінтестинальних, порівняно з групою дітей, які його не отримували (контрольна група), що свідчить про виражений терапевтичний ефект даного лікувального засобу.
У процесі спостереження за дітьми основної групи на фоні лікування виявлено регресію шкірних висипань та значне зменшення інтенсивності свербежу, що підтверджено зниженням середнього показника індексу SCORAD у 2,3 раза (із 80,27 ± 2,97 до 35,27 ± 2,54 бала). У 20 пацієнтів групи контролю, які отримували традиційну терапію, індекс SCORAD до лікування становив 77,27 ± 3,41 бала, після курсу терапії він знизився лише до 49,6 ± 4,5 бала (в 1,56 раза) (табл. 1). Таким чином, в основній групі спостереження відмічене вірогідне зниження індексу SCORAD порівняно з контрольною групою в динаміці лікування (p = 0,01).
%201/53-1.jpg)
У дітей обох груп спостереження відмічена позитивна динаміка гастроінтестинальних симптомів, однак серед обстежуваних основної групи наприкінці дослідження вірогідно нижчим був відсоток дітей з абдомінальним больовим синдромом, зригуваннями або блюванням, неоформленими випорожненнями, порушенням сну на відміну від пацієнтів групи контролю, у якій спостерігалось вірогідне зменшення лише абдомінального больового синдрому (табл. 2).
У всіх обстежених дітей середньодобова прибавка маси тіла відповідала віковій нормі.
В основній групі відмічено також покращання сну. При опитуванні матерів основної групи 19 (76,0 %) із них на початку дослідження відмічали порушення характеру сну дітей через виражений свербіж шкіри. Після проведеного лікування в більшості дітей основної групи сон нормалізувався, а дітей із порушеннями сну було тільки 3 (12,2 %), у той час як у групі контролю порушення сну зберігались у 35,0 % дітей.
За результатами УЗД органів черевної порожнини виявлені позитивні зміни на фоні проведеної терапії у вигляді зменшення розмірів печінки та нормалізації ехогенності її паренхіми.
Індивідуальна переносимість суспензії УДК була доброю в усіх пацієнтів основної групи спостереження.
У процесі виконання дослідження не було відмічено алергічних або інших негативних реакцій на прийом суспензії УДК, у тому числі алергічних реакцій або посилення клінічної симптоматики захворювання в дітей з АД, що свідчить про безпеку застосування суспензії УДК у цієї категорії дітей.
Висновки
1. Прийом суспензії урсодеоксихолевої кислоти (Укрлів) у складі комплексної терапії атопічного дерматиту середньої тяжкості та тяжкої форми в дітей раннього віку сприяв позитивній клінічній динаміці як шкірних, так і гастроінтестинальних проявів, що виражалось зменшенням площі ураження шкіри, інтенсивності свербежу, нормалізацією сну та регресією больового абдомінального синдрому, зменшенням частоти зригувань.
2. Призначення суспензії урсодеоксихолевої кислоти (Укрлів) дітям раннього віку з атопічним дерматитом у дозі 10 мг/кг/добу протягом 21 дня не викликало розвитку побічних реакцій, що свідчить про безпеку застосування суспензії УДК у цієї категорії дітей.
3. Проведене клінічне дослідження дозволяє рекомендувати включення суспензії урсодеоксихолевої кислоти в комплексну терапію атопічного дерматиту в дітей перших років
життя.
Конфлікт інтересів. Не заявлений.

%201/53-1.jpg)
%201/54-1.jpg)