Статтю опубліковано на с. 86-92
Стаття є фрагментом науково-дослідної роботи «Пошук шляхів ранньої діагностики природжених вад розвитку, асоційованих із недиференційованою дисплазією сполучної тканини».
Вступ
Проблема природжених вад розвитку органів сечовидільної системи (ПВР ОСС) у дітей раннього віку стає все більш актуальною у зв’язку зі щорічним зростанням кількості хворих з ускладненим перебігом захворювань ОСС [4]. Особливо гостро це питання постало перед дитячими нефрологами та урологами, які спостерігають гетерогенність перебігу захворювань ОСС. Це спонукало до чіткого виділення в дитячій нефрології окремого напрямку — нефрології раннього дитинства, яка, по суті, є нефроурологією [11].
Однією з найбільш поширених ПВР ОСС у дітей раннього віку є міхурово-сечовідний рефлюкс (МСР) [10].
У наш час спостерігається тенденція до збільшення кількості мікроаномалій з боку різних органів і систем, зумовлених особливостями будови сполучної тканини [5]. Ці зміни проявляються комплексом фенотипових ознак і трактуються як недиференційована дисплазія сполучної тканини (НДСТ) [6].
Синдром дисплазії сполучної тканини (ДСТ) був відокремлений як самостійна нозологічна форма наприкінці XX ст. ДСТ прийнято розподіляти на диференційовані дисплазії сполучної тканини (ДДСТ) та недиференційовані дисплазії сполучної тканини. ДДСТ характеризуються певним типом успадкування та чіткою клінічною картиною, зокрема це синдроми Марфана, Елерса — Данлоса та ін. НДСТ діагностують, коли в пацієнта набір клінічних ознак не вкладається в жодне спадкове моногенне захворювання [1].
У практичній діяльності частіше доводиться стикатися з недиференційованими формами ДСТ — генетично гетерогенною групою захворювань мультифакторної природи з прогредієнтним перебігом, в основі яких лежать порушення синтезу, розпаду чи морфогенезу компонентів позаклітинного матриксу, що виникає в період раннього ембріогенезу чи постнатально під впливом несприятливих факторів оточуючого середовища й може виявлятися в різні періоди життя [6].
Після народження дитини з ПВР ОСС, зокрема з МСР, у клінічному аспекті одним із питань, що потребує своєчасного вирішення, є безпосередня оцінка того, наскільки вада відповідає НДСТ, тобто наскільки остання порушує функціональний стан паренхіми нирок.
Вчені-урологи С.А. Байдін, Л.Б. Меновщикова, а також ряд інших авторів вказують, що одним із провідних патогенетичних факторів порушення функції нирок при МСР, асоційованому з НДСТ, є гіпоксія, яку викликають як гемодинамічні порушення, закономірно наявні при НДСТ, так і порушення тканинного дихання [13].
У літературі є повідомлення про швидкий розвиток склерозування ниркової тканини у дітей раннього віку при МСР, асоційованому з НДСТ, і особливо за наявності запального процесу ниркової паренхіми [12]. Відомо, що МСР зумовлює низку патологічних процесів у нирці, кінцевим результатом яких є ремоделювання тубулоінтерстиціальної тканини, що стає передумовою нефросклерозу [12].
Проте чутливість екскреторної урографії як способу рентгенологічної оцінки стану функціонуючої паренхіми при нефросклерозі дуже низька [12].
Ультразвукове дослідження (УЗД) широко використовується у дітей, однак дозволяє вловлювати склеротичні зміни в нирках тільки на пізніх етапах формування нефросклерозу [17]. Радіоізотопні методи діагностики дозволяють визначити ступінь та обсяг функціонуючої паренхіми за індексом інтегрального захвату радіофармпрепарату [16]. Проте високий ступінь променевого ушкодження інших органів, висока вартість та великі розміри датчика обмежують використання даного способу для діагностики рубцевих змін у паренхімі нирок дітей раннього віку.
Вищезазначене вимагає пошуку скринінгових високочутливих специфічних методів діагностики та прогнозування нефросклеротичних змін при НДСТ у дітей раннього віку з МСР.
Для розуміння діагностичної цінності тестів із позицій доказової медицини Р. Флетчер і співавт. [15] запропонували оригінальну чотирипільну таблицю, що дає змогу визначати відношення між результатами тестування та правильним діагнозом.
Існує два мнемонічних правила, що суттєво допомагають у використанні даних про чутливість і специфічність діагностичного тесту, а саме:
SnNout — мнемонічне правило, що стверджує таке: ознака, тест або симптом, які мають високу чутливість (high Sensitivity test), при негативному їх результаті виключають наявність захворювання (Negative result rules out);
SpPin — мнемонічне правило, що стверджує таке: ознака, тест або симптом, які мають високу специфічність (high Specificity test), при позитивному їх результаті підтверджують наявність захворювання (Positive result rules in).
Оптимальні тести відповідають критеріям, наведеним у табл. 1 [15].
Для того, щоб оцінити якість тесту для певної хвороби, тобто ефективності лабораторних тестів, варто користуватися такими мірами, як чутливість і специфічність [15]. Чутливість тесту — це ймовірність того, що у позитивного пацієнта буде позитивний тест. Якщо в усіх пацієнтів із певною хворобою тест дає позитивний результат, тоді чутливість тесту буде 100 %. Тест із високою чутливістю є корисним, тому що виключає діагноз, оскільки надає мало помилково негативних результатів.
Специфічність тестів — це ймовірність того, що здоровий пацієнт отримає негативні результати тесту. Якщо всі пацієнти, які не мають певної хвороби, отримують негативні тести, специфічність тесту становить 100 %. Високоспецифічний тест корисний для підтвердження діагнозу, оскільки цей тест надає дуже мало помилково позитивних результатів.
Для визначення чутливості та специфічності тесту щодо певної хвороби його необхідно порівняти із золотим стандартом — процедурою, що визначає справжній стан пацієнта.
У літературі є повідомлення, що результати клінічного обстеження та стандартного комплексу досліджень функціонального стану нирок, проведеного у дітей з МСР, так звані тести золотого стандарту, не виявили в них порушення функціонального стану паренхіми та виражених ознак нефросклерозу [7, 8]. Тому виникла необхідність впровадження точних, чутливих, а також неінвазивних методів динамічної оцінки функціонального стану ниркової паренхіми.
Отже, мета дослідження — встановлення референтних значень показників функціонального стану паренхіми нирок у здорових дітей раннього віку та оцінка їх інформативності й діагностичної цінності у дітей раннього віку з МСР.
Матеріали та методи
З метою оцінки результатів дослідження біологічних маркерів ушкодження паренхіми нирок у дітей із МСР були обстежені 50 дітей з одно- або двобічним МСР ІІ–ІV ст., асоційованих із НДСТ, що було підтверджено наявністю у їх сечі оксипроліну. Референтну групу становили 40 соматично здорових дітей.
Визначались такі маркери тканинної гіпоксії паренхіми: тест на АКЗС за методикою Е.О. Юр’євої [2] та добова екскреція солей у сечі за методикою Ю.Є. Вельтищева [2].
Досліджувались маркери морфофункціонального стану цитомембран ниркового епітелію: проба на кальцифікацію — наявність полярних ліпідів (ПЛ) у сечі та тест на наявність продуктів перекисного окислення ліпідів (ПОЛ) у сечі за методикою Е.О. Юр’євої [14].
Маркерами функціонального стану проксимальних канальців вважали тести на уринолізис: проби на наявність білка, гіпераміноацидурію, проба за Сулковичем, проба Гайнеса, що проводились за методикою І.І. Гребешевої [14].
Визначали маркери функціонального стану сполучної тканини паренхіми нирок, зокрема вміст креатиніну та глікозоаміногліканів у добовій сечі за методом Ю.Є. Вельтищева та А.А. Ананенко [2].
З метою максимального наближення клініко-лабораторних результатів у дітей референтної конт–рольної групи до загальнопопуляційних для відбору дітей був використаний рандомізований метод випадкової вибірки [9].
Чутливість, специфічність та ефективність діагностичного лабораторного тесту визначали за чотирипільною таблицею, приклад якої наведений у табл. 2 [15].
Характеристики діагностичного тесту в чотирипільній таблиці такі:
Se — чутливість;
Sр — специфічність;
+PV — прогностична цінність позитивного результату тесту;
–PV — прогностична цінність негативного результату тесту;
+LR — відношення правдоподібності позитивного результату тесту;
–LR — відношення правдоподібності негативного результату тесту;
Р — поширеність захворювання.
При цьому для оцінки чутливості діагностичного тесту, що перевіряється, брали такі дані, наведені в табл. 3.
Визначали вірогідність відмінностей між середніми показниками. Для кожного порівняння було знайдено ймовірність (p) того, що різниця є вірогідною. Ймовірність (p) для більшості вибірок не перевищувала 0,01. За допомогою таблиці «Значення нормального інтегралу ймовірностей в межах ± t» та відповідно до величини коефіцієнта Стьюдента знаходили значення ймовірності (p) [3].
Обговорення результатів
Результати дослідження обраних маркерів ушкодження паренхіми нирок у соматично здорових дітей референтної групи подані в табл. 4.
/86-92/89-1.jpg)
/86-92/89-2.jpg)
Ефективність діагностичних тестів найпоказовіше характеризує прогностичну цінність результату діагностичного дослідження та відношення правдоподібності, що об’єднують інформацію про чутливість і специфічність [15]. У зв’язку з цим було обчислено прогностичну цінність позитивного результату тесту — ймовірність наявності хвороби за позитивного результату (+PV) та прогностичну цінність негативного результату тесту — ймовірність відсутності хвороби за негативного результату (–PV). Визначалось також відношення правдоподібності позитивного результату тесту в осіб із захворюванням до ймовірності цього результату в осіб без цього захворювання (+LR), а також відношення правдоподібності негативного результату тесту –(–LR) як відношення ймовірності мати негативний результат тесту в осіб із захворюванням до ймовірності цього результату в осіб без захворювання згідно з формулами, які включають чутливість, специфічність і поширеність хвороб (Р) кожного тесту, що вивчався у пацієнтів із МСР. Приклад оцінки результатів діагностичної ефективності тесту на антикристалутворюючу здатність сечі (АКЗС) до оксалатів кальцію в дітей раннього віку з міхурово-мисковим рефлексом наведений у табл. 5.
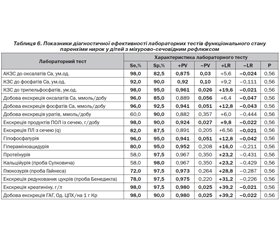
Показники діагностичної ефективності всіх лабораторних тестів функціонального стану паренхіми нирок у дітей із МСР наведені у табл. 6.
Отже, за даними Se та Sр, наведеними у табл. 6, тести, обрані для характеристики функціонального стану паренхіми нирок у дітей із МСР, мають в основному високу (АКЗС до оксалатів Ca, АКЗС до фосфатів Ca, АКЗС до трипельфосфатів, добова екскреція оксалатів Ca, добова екскреція фосфатів Ca, екскреція продуктів ПОЛ із сечею, гіпофосфатурія, екскреція креатиніну, добова екскреція ГАГ) та середньовисоку (екскреція ПЛ із сечею, гіпер–аміноацидурія, глюкозурія та екскреція редукованих цукрів) чутливість при високій специфічності в межах 82,5–98,0 %.
Величина прогностичної цінності як позитивних (+PV), так і негативних (–PV) результатів обраних тестів у дітей із МСР підтвердила ефективність діагностування тканинної гіпоксії, процесів мембранодеструкції, тубулярної дисфункції та наявність дисфункції сполучної тканини паренхіми нирок, оскільки вона коливалась в межах 0,875–0,980 для +PV та 0,025–0,350 для –PV (табл. 6).
Відношення правдоподібностей для позитивних результатів діагностичного тесту +LR показало, що тести екскреції креатиніну з добовою сечею та добова екскреція з сечею ГАГ з високою ймовірністю діагностують наявність дисфункції сполучної тканини паренхіми нирок у хворого, якщо в нього отримані дані про зниження екскреції креатиніну (+LR = 39,2) та підвищення екскреції ГАГ (+LR = 39,2) з сечею (табл. 6).
Такі тести як АКЗС до трипельфосфатів та добова екскреція фосфатів Ca мають цілком задовільну здатність діагностувати наявність тканинної гіпоксії паренхіми нирок у дітей із МСР (+LR = +19,6 та +12,8 відповідно). Тести АКЗС до оксалатів Ca –
(–LR = –0,024) із задовільною вірогідністю та добова екскреція оксалатів Ca (–LR = –0,047) і добова екскреція фосфатів Ca (–LR = –0,043) з високою ймовірністю діагностують відсутність тканинної гіпоксії у дитини з МСР, якщо в неї не було виявлено відхилень у цих показниках. Отже, обрані для характеристики наявності тканинної гіпоксії паренхіми нирок тести мають високу ймовірність діагностувати як наявність тканинної гіпоксії, так і її відсутність.
Такі тести як екскреція продуктів ПОЛ з сечею (+LR = +9,8; –LR = –0,022) та екскреція ПЛ із сечею (+LR = +6,56; –LR = –0,021) мають середню здатність діагностувати наявність мембранопатологічного процесу в паренхімі нирок у дітей із МСР, проте особливо високоймовірно відкидають наявність мембранодеструкції клітин ниркового епітелію у дітей із негативним результатом (табл. 6).
Комплекс тестів уринолізису цілком задовільно діагностує наявність дисфункції проксимальних канальців нефронів при позитивному результаті (+LR від +12,8 до +31,2), а тест на гіпофосфатурію ще й здатний задовільно заперечувати наявність порушення функції проксимальних відділів нефронів за відсутності гіпофосфатурії (–LR = –0,042).
Отже, обраний комплекс тестів продемонстрував високу чутливість, специфічність та ефективність діагностики порушень функціонального стану і склеротичних змін у паренхімі нирок в дітей із МСР.
Відомо, що чим більша +LR, тим вища чутливість тесту при позитивних результатах встановити наявність хвороби [15]. Обрані тести продемонстрували їх задовільну здатність розпізнавати наявність порушення функціонального стану паренхіми нирок у групах дітей раннього віку з МСР, оскільки цифри +LR для всіх тестів перебували у межах +5,14…+35,00.
Відповідно, чим менша –LR, тим вища чутливість тесту при негативних результатах виявити відсутність хвороби [15]. Обраний комплекс тестів продемонстрував задовільну здатність розпізнавати відсутність захворювання в дітей із МСР, оскільки в основному величини –LR коливались в межах –0,016...–0,340 (табл. 6).
Отже, в той час як тести, що належать до золотого стандарту діагностики порушення функціонального стану та наявності процесів склерозування паренхіми нирок, не відзначали цих порушень в обстежених дітей із МСР, обраний комплекс тестів продемонстрував високу чутливість, специфічність, прогностичну цінність та ефективність діагностики ранніх порушень функціонального стану і розвитку склеротичних змін у паренхімі нирок у дітей із МСР, асоційованого з НДСТ.
Висновки
1. Доведена висока чутливість, специфічність, прогностична цінність та ефективність діагностики ранніх порушень функціонального стану та дисфункції сполучної тканини паренхімі нирок, асоційованих із НДСТ за показниками АКЗС до оксалатів Са, фосфатів і трипельфосфатів, добової екскреції оксалатів Са, фосфатів Са та уратів, добової екскреції продуктів ПОЛ і ПЛ, результату дослідження тестів уринолізису, вмісту у добовій сечі креатиніну та глікозаміногліканів.
2. Отримані результати дослідження біомаркерів функціонального стану паренхіми нирок у дітей референтної групи можна використовувати як нормативні регіональні показники.
Список литературы
1. Багдасарова І.В. Захворювання органів сечової системи у дітей та синдром дисплазії сполучної тканини / І.В. Багдасарова, Т.В. Буднік, А.В. Малахова // Новости медицины и фармации. Нефрология. — 2009. — № 297. — С. 38-39.
2. Биохимическое исследование мочи у детей: Метод. рекомендации [Текст] / Ю.Е. Вельтищев, А.А. Ананенко, Г.М. Титов [и др.] — М., 1979. — 51 с.
3. Боровиков, В. Statistica: искусство анализа данных на компьютере. Для профессионалов [Текст] / В. Боровиков. — СПб.: Питер, 2001. — 656 с.
4. Динамика заболеваемости и распространенности заболеваний мочевыводящей системы у детей г. Екатеринбург и Свердловской области / В.Л. Зеленцова, В.И. Шилко, Р.Г. Бабина, Е.Б. Николаева // Педиатрия. — 2003. — № 2. — С. 31-36.
5. Земцовский Э.В. Диагностика и лечение дисплазии соединительной ткани [Текст] / Э.В. Земцовский // Мед. вестник. — 2006. — № 11. — С. 11-14.
6. Кадурина Т.И. Дисплазия соединительной ткани: Руководство для врачей [Текст] / Т.И. Кадурина, В.Н. Горбунова. — СПб.: Элби СПб., 2009. — 714 с.
7. Кенс К.А. Неінвазивні маркери порушення функції нирок у дітей раннього віку з міхурово-сечовідним рефлюксом в динаміці хірургічного та метаболічного лікування [Текст]: Автореф. дис… канд. мед. наук: спец. 14.01.06 / К.А. Кенс; Державна установа «Інститут урології НАМН України». — К., 2012. — 23 с.
8. Лакомова Д.Ю. Ранняя диагностика и прогнозирование развития нефросклероза у детей с пузырно-мочеточниковым рефлюксом [Текст]: Автореф. дис… канд. мед. наук: спец. 14.01.23; 14.03.03 / Д.Ю. Лакомова; Саратовский медицинский университет им. В.И. Разумовского. — Саратов: б.и., 2011. — 26 с.
9. Мальцев В.И. Методология проведения клинических исследований [Текст] / В.И. Мальцев, Т.К. Ефимцева, Д.Ю. Белоусов // Український медичний часопис. — 2001. — № 5. — С. 49-65.
10. Наказ МОЗ України від 29.12.2003 № 624 «Про затвердження Протоколів лікування дітей зі спеціальності «Дитяча урологія».
11. Папаян А.В. Клиническая нефрология детского возраста / А.В. Папаян, Н.Д. Савенкова. — СПб.: Сотис, 1997. — 718 с.
12. Патогенетические основы и современные возможности ранней діагностики нефросклероза у детей с пузырно-мочеточниковым рефлюксом / Д.А. Морозов, В.В. Моррисон, О.Л. Морозова, Д.Ю. Лакомова // Саратовский научно-медицинский журнал. — 2011. — Т. 7, № 1. — С. 151-157.
13. Перекисное окисление липидов и метаболизм оксида азота у больных хронической болезнью почек в динамике лечения [Текст] / И.И. Топчий, А.Н. Кириенко, Т.Н. Бондарь [и др.] // Український журнал нефрології та діалізу. — 2012. — Т. 33, № 1(33). — С. 3-8.
14. Скрининг-тесты в педиатрии [Текст] // Под ред. И.И. Гребешевой. — К., 1985. — 30 с.
15. Флетчер Р. Клиническая эпидемиология. Основы доказательной медицины [Текст] / Флетчер Р., Флетчер С., Вагнер Е. / Пер. с англ. под общ. ред. С.Е. Бащинского, С.Ю. Варшавского. — М.: Медиа Сфера, 1998. — 347 с.
16. Хворостов И.Н. Тактика лечения пузырно-мочеточникового рефлюкса у детей [Текст] / И.Н. Хворостов, С.Н. Зоркин, И.Е. Смирнов // Бюллетень Волгоградского научного центра РАМН. — 2009. — № 4. — С. 30-33.
17. Gallo F. Ureteropelvic Junction obstruction: Which is the best treatment today? [Text] / F. Gallo, M. Schenone, C. Giberti // J. Laparoendoscopic advanced surgical techniques. — 2009. — Vol. 19(5). — P. 657-662.

/86-92/88.jpg)
/86-92/88-2.jpg)
/86-92/89-1.jpg)
/86-92/89-2.jpg)
/86-92/90-1.jpg)
/86-92/90-2.jpg)