Статья опубликована на с. 14-17 (Укр.)
Грип — це гостре вірусне захворювання, що передається повітряно-крапельним шляхом і є найбільш частим інфекційним захворюванням у вагітних. Вірус грипу проникає через дихальні шляхи, уражає циліндричний епітелій респіраторного тракту, особливо трахеї. Підвищення проникності судинної стінки спричиняє порушення мікроциркуляції та геморагічні ускладнення (петехіальну висипку на шкірі та слизовій оболонці ротової порожнини, крововиливи в склери та кон’юнктиву, рідше — кровохаркання, носові кровотечі, геморагічну пневмонію). Грип знижує імунологічну резистентність і тим самим провокує загострення хронічних захворювань (ревматизм, пієлонефрит, холецистит тощо).
Пацієнтка становить загрозу щодо зараження грипом оточуючих від перших годин захворювання до стихання катаральних явищ (упродовж 5–7 діб). При ускладненні грипу пневмонією вірус зникає на 10–14-й день і пізніше, а при розмноженні збудника в носоглотці можлива поява епідеміологічно небезпечної безсимптомної форми хвороби [3, 4].
На грип та інші гострі респіраторні вірусні інфекції (ГРВІ) в Україні щорічно хворіє від 10 до 25 % населення. Грип посідає друге місце у структурі інфекційних хвороб, поступаючись лише сумарній кількості гострих вірусних інфекцій дихальних шляхів. Віруси грипу вражають різні органи та системи й у 5 % випадків спричиняють тяжкі, гіпертоксичні форми захворювання. Практично всі епідемії грипу супроводжуються розвитком ускладнень у вигляді пневмоній, синуситів, отитів, менінгітів, гострої серцево-судинної патології, що призводить до підвищення смертності, особливо в групах ризику [1, 2, 4]. Це стосується й вагітних, оскільки в них частіше діагностують тяжкі та ускладнені форми грипу, пневмонії [6, 7].
Найбільш частими ускладненнями грипу є пневмонії (74,6 %) [15, 16]. Смертність від грипозної пневмонії становить 30 % від загальної смертності, 90 % від смертності від грипу й респіраторних вірусних інфекцій. Пневмонія, що ускладнює перебіг грипу, може розвинутися в будь-якому періоді захворювання на грип [13, 14]. Однак в осіб молодого віку в 60 % випадків переважають ранні вірусні пневмонії, що виникають на 1–5-й день від початку захворювання, зазвичай при вираженому катаральному синдромі й загальній інтоксикації, що значно ускладнюють своєчасну діагностику цих ускладнень [13, 14]. Вірусно-бактеріальна пневмонія виявляється в половини всіх хворих, госпіталізованих з грипом, переважно тяжкої й середньотяжкої форми.
Проблема грипу розглядається сучасною наукою як глобальна: за даними ВООЗ, у світі щорічно на грип та інші гострі вірусні інфекції респіраторного тракту хворіють від 3 до 5 млн людей, помирають від грипу та його ускладнень від 20 до 40 тисяч [13]. У період епідемій збільшується летальність не тільки від вірус-асоційованих хвороб, але й від неінфекційних захворювань, 70 % померлих — особи старшого віку [9, 10].
Сьогодні гостро виникла чергова проблема грипу, викликаного вірусом грипу А (H1N1) (свинячого грипу), який може набирати розмахів пандемії та є інфекцією, що раптово виникає й пояснюється переходом відомого збудника на нового хазяїна.
Вірус грипу свиней H1N1 — А/Каліфорнія/04/2009 (штам H1N1/Каліф) — з’явився в Мексиці у березні 2009 р., зміг інфікувати людей і передаватися контактним особам. Цей штам є потрійним реасортантом і містить гени, що кодують гемаглютинін і білки NP і NS, характерні для класичного штаму вірусу грипу свиней, гени, що кодують нейрамінідазу й білок М — від євроазіатської лінії вірусу грипу свиней, гени, що кодують білки РВ2 і РА — від вірусу грипу птахів, і ген, що кодує білок РВ1 — від вірусу грипу людини [5, 11].
За антигенної специфічності штам H1N1/Каліф сильно відрізняється від вірусу грипу людини H1N1, штам А/Брісбейн/59/2007, що циркулював серед людей у сезонних епідеміях грипу в останні роки. Антитіла до штаму H1N1/Каліф у реакції затримки гемаглютинації майже не реагували зі штамом H1N1/Брісбейн, так само як антитіла до штаму H1N1/Брісбейн — зі штамом H1N1/Каліф [5, 8].
Зимовий період є найбільш сприятливим для поширення різних штамів вірусу грипу. Не став винятком і 2016 рік. Саме зима 2016 року ознаменована активним поширенням найбільш небезпечного штаму, іменованого каліфорнійським, або свинячим, грипом.
Грип та інші гострі респіраторні вірусні інфекції досить часто зустрічаються в період вагітності. У вагітних грип становить реальну небезпеку як для майбутньої матері, так і для плода. Повідомляється (Трифонов И., 2007), що фізіологічні зміни в організмі, які відбуваються при вагітності, сприяють ризику розвитку тяжких ускладнень при виникненні респіраторного захворювання незалежно від його збудника. Отже, вагітна жінка більш вразлива до респіраторних патогенів, у тому числі вірусів. У вагітних грипозна інфекція може різко знижувати резистентність організму, порушувати функції ендокринної та імунної систем, що сприяє активізації існуючих латентних хвороб, а також підвищувати ризик захворювання на інші гострі респіраторні вірусні інфекції під час вагітності та після пологів.
За час спалаху епідемії 2016 р. у нашому закладі всього проліковано 349 хворих на ГРВІ та грип, з них підтверджено грип лабораторно (вірусологічно) в 43 вагітних жінок різного віку та терміну гестації. З них грип А (Н1N1) було підтверджено у 28 вагітних, грип А — у 8, грип В — у 7.
Незважаючи на існування ефективної вакцини, вибір методів лікування грипу зараз досить обмежений. Антивірусна терапія є найважливішою складовою комплексного лікування грипу. Безпечна й ефективна терапія грипозної інфекції є серйозною проблемою, що в умовах нової пандемії, пов’язаної з вірусом грипу A (H1N1), стоїть особливо гостро [12].
Наприклад, гідрохлориди амантадину й ремантадину — препарати, ефективні на ранній стадії грипу А, не діють на віруси грипу В і можуть сприяти розвитку вірусної резистентності в осіб, які вже отримували ці препарати. Крім того, обидва препарати можуть викликати небажані явища з боку центральної нервової системи й шлунково-кишкового тракту. Озельтамівіру карбоксилат — потужний специфічний інгібітор нейрамінідази вірусу грипу — пригнічує реплікацію широкого спектра вірусів грипу А і В in vitro. Озельтамівіру фосфат (озельтамівір) — проліки озельтамівіру карбоксилату, він являє собою етиловий ефір, при пероральному прийомі якого досягається стійка концентрація активної речовини в плазмі.
Вірус грипу A (H1N1) swl чутливий до інгібіторів нейрамінідази — озельтамівіру й занамівіру [1, 2]. Однак застосування таких препаратів у нашій країні обмежене їх високою вартістю.
Інгавірин® — новий оригінальний вітчизняний хіміопрепарат, дозволений до застосування при грипі у дорослих в 2008 р. на підставі результатів досліджень. Основною діючою речовиною даного препарату є імідазолілетанамід пентандіової кислоти (вітаглутам), завдяки чому препарат чинить противірусну дію, ефективний щодо вірусів грипу типу А та В, аденовірусної інфекції. В експерименті in vitro та in vivo ефективно пригнічує репродукцію та цитопатичну дію вірусів грипу типу А та В, аденовірусів. Противірусний механізм дії полягає в пригніченні репродукції вірусу на етапі ядерної фази, що забезпечує затримку міграції заново синтезованого NP вірусу з цитоплазми в ядро, чим і викликає підвищення вмісту інтерферону в крові до фізіологічної норми, стимулює й нормалізує знижену α-інтерферон-продукуючу здатність лейкоцитів крові, стимулює γ-інтерферон-продукуючу здатність лейкоцитів. Викликає генерацію цитотоксичних лімфоцитів і підвищує вміст NK-Т-клітин, що мають високу кілерну активність щодо трансформованих вірусами клітин і визначену противірусну активність.
Протизапальна дія обумовлена пригніченням продукції ключових протизапальних цитокінів (TNF-α, IL-1β і IL-6) за рахунок зниження активності мієлопероксидази.
Терапевтична ефективність при грипі проявляється в скороченні періоду гарячки, зменшенні інтоксикації (головний біль, слабкість, запаморочення), катаральних явищ, зниженні числа ускладнень і тривалості захворювання в цілому. Проведені токсикологічні дослідження свідчать про низьку токсичність і високий профіль безпеки препарату (LD50 перевищує терапевтичну дозу більше ніж у 3000 разів). Встановлено, що препарат не має мутагенної й канцерогенної дії, не впливає на репродуктивну функцію, не має імунотоксичних і алергізуючих властивостей, не чинить місцевої подразнювальної дії.
З огляду на вищенаведене підставою для клінічного застосування Інгавірину® при грипі A (H1N1) стала його противірусна активність щодо цього збудника, показана в дослідженнях in vitro [2, 8].
Мета дослідження: порівняти ефективність та переносимість Інгавірину® і озельтамівіру (Таміфлю®, рекомендованого Всесвітньою організацією охорони здоров’я для лікування пацієнтів, інфікованих вірусом пандемічного грипу H1N1) у вагітних жінок для подальшого впровадження необхідного лікування в клінічну практику.
Матеріали й методи дослідження
Для досягнення мети під нашим наглядом проведено клінічні випробування препарату Інгавірин® та Таміфлю® у вигляді таблеток у вагітних жінок, хворих на ГРВІ, та всіх пацієнток з верифікованим діагнозом «грип».
Дослідження проводилось на базі Київського міського центру репродуктивної та перинатальної медицини. Госпіталізація відбувалася в інфекційне акушерське відділення та відділення патології першої половини вагітності.
Усім хворим, які надходили з явищами ГРВІ, проведено комплексне обстеження, яке передбачало оцінку їх клінічного стану: виконувався чіткий збір епіданамнезу, анамнезу життя та захворювання, скарг, зовнішній, бімануальний огляд, проводились загальноклінічні дослідження (загальний аналіз крові з лейкоцитарною формулою, коагулограма, біохімічний аналіз крові, загальний аналіз сечі, аналізи виділень із піхви), жінки обстежувались вірусологічно, вимірювалась сатурація, проводилася аускультація легень.
Усі вагітні з явищами ГРВІ оглядалися лікарем-інфекціоністом та анестезіологом (вихідні дні, вечірні та нічні години).
До дослідження було залучено 100 вагітних жінок, яких було розподілено на дві клінічно та статистично рівні групи, які отримували необхідну симптоматичну терапію (дезінтоксикаційну, жарознижуючу, знеболюючу, спрямовану на збереження вагітності, антиоксидантну, муколітичну, вітамінотерапію). Основну групу становили 50 жінок, яким призначався препарат Інгавірин® по 1 таблетці на добу впродовж 5 днів. Контрольну групу становили 50 жінок, яким призначався препарат Таміфлю® по 1 таблетці двічі на добу впродовж 5 днів. Проводилось динамічне клініко-лабораторне спостереження за досліджуваними з постійним моніторингом стану плода за допомогою ультразвукового дослідження та кардіотокографії після 24 тижнів вагітності (протягом проведеного лікування та після нього).
Контроль лікування проводили через 2 дні, 5 днів та 2 тижні від початку лікування (у разі виписки зі стаціонару раніше від зазначеного терміну з пацієнтами було обговорено чіткий регламент щодо обов’язкової явки для проведення необхідних діагностичних заходів в амбулаторних умовах з визначенням усіх необхідних даних).
Отримані цифрові дані оброблені методом варіаційної статистики за допомогою програми Microsoft Excel із застосуванням парного критерію Стьюдента.
Результати та їх обговорення
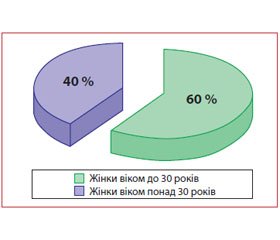
Досліджувані групи були подібні за віком, соматичним та акушерським анамнезом. Вік обстежених жінок коливався від 18 до 40 років. Більшість хворих (60 %) була віком до 30 років (рис. 1).
Усі жінки, які увійшли до груп дослідження, знаходилися на різних термінах гестації й розподілялися таким чином: І триместр — 18 жінок основної групи і 15 жінок — контрольної; ІІ триместр — 18 вагітних основної групи, 10 — контрольної групи; ІІІ триместр — 14 вагітних основної групи, 25 — контрольної (рис. 2).
Слід зазначити, що на етапі госпіталізації 70 % жінок було доставлено в лікувальний заклад каретою швидкої допомоги, а решта, 30 %, звернулися за медичною допомогою самостійно чи за направленням дільничного акушера-гінеколога жіночої консультації або дільничного терапевта. Тривалість захворювання коливалася в межах від 1 до 5 днів (рис. 3).
При госпіталізації пацієнтки скаржилися на загальну слабкість, підвищення температури тіла, головний біль, дертя в горлі, кашель, нежить, сльозотечу (дані наведено в табл. 1).
Під час госпіталізації досліджуваним проводили необхідний клініко-лабораторний огляд. Для оцінки повноти поставленої нами мети дослідження як важливі клініко-лабораторні показники прийнято параметри сатурації (SpO2), аускультації легень, загального аналізу крові з лейкоцитарною формулою.
У 100 досліджуваних вагітних з даною патологією параметри сатурації не опускалися нижче за відмітку 95 %. Але слід відмітити, що в 9 жінок основної групи, що становить 18 %, параметри сатурації коливалися в межах 98–99 %, а також у 19 жінок (38 %) контрольної групи. У межах 97–98 % параметри сатурації відмічалися у 16 (32 %) вагітних основної групи й у 7 (14 %) жінок контрольної групи, SpO2 в межах 96–97 % визначалася у 25 (50 %) досліджуваних основної групи та у 24 (48 %) — контрольної групи.
Під час госпіталізації спостерігалася така картина при аускультації легень: везикулярне дихання було в 15 і 13 жінок основної та контрольної груп, що становить 30 та 26 % відповідно; везикулярне дихання з жорстким відтінком вислуховувалося у 12 (24 %) пацієнток основної групи та 19 (38 %) пацієнток контрольної групи; жорстке дихання було наявним у 23 вагітних основної групи та 18 — контрольної, 46 та 36 % відповідно.
Беручи до уваги показники загального аналізу крові, слід зазначити, що в усіх жінок обох досліджуваних груп відмічався лейкоцитоз зі зсувом лейкоцитарної формули вліво.
Після призначення лікування нами було отримано такі результати (табл. 2).
Після проведення динамічного спостереження нами було відмічено нормалізацію SpO2 на фоні призначеної терапії в усіх жінок основної групи на 2-гу — 3-тю добу, у жінок контрольної групи нормалізація параметрів сатурації відмічалася на 3-тю — 5-ту добу лікування.
Аускультативна картина легень змінювалася таким чином: в основній групі у 19 жінок (38 %) везикулярне дихання з жорстким відтінком вислуховувалося з 2-ї до 5-ї доби, жорсткий відтінок зовсім зникав і лише у 2 вагітних (4 %) зберігався до 8 діб, у контрольній групі аускультативна картина змінювалася аналогічним чином у 29 (58 %) досліджуваних та 3 (6 %) вагітних відповідно.
Беручи до уваги показники загального аналізу крові, слід зазначити, що зсув лейкоцитарної формули вліво нівелювався вже на 3-тю — 4-ту добу як в основній, так і в контрольній групах, хоча підвищення лейкоцитів у крові трималося до 5–7-ї доби.
Слід зазначити, що при аналізі стану плода патологічних станів, які б супроводжували його внутрішньоутробну життєдіяльність, не відмічалося в жодній досліджуваній групі.
Слід також відмітити наявність негативних реакцій, що проявлялися блюванням, у 9 жінок контрольної групи після прийому озельтамівіру, що становить 18 %, в основній групі жодних негативних реакцій не відмічалося.
Висновки
Результати проведеного дослідження свідчать про високу ефективність озельтамівіру в лікуванні ГРВІ та грипу. Застосування препарату в ранні строки хвороби призводить до зниження температури тіла, зменшення тривалості основних симптомів захворювання (лихоманки, головного болю, загальної слабкості, кашлю, трахеїту, риніту) і зниження інфекційного титру вірусу. Отримані дані узгоджуються з результатами мультицентрового дослідження й дозволяють рекомендувати озельтамівір як препарат вибору для лікування хворих на грип.
Проте проведене дослідження клінічної ефективності Інгавірину® показало, що застосування досліджуваного препарату в ранні терміни грипозної інфекції (перші 24–36 год) призводить до статистично вірогідного зменшення тривалості гарячкового періоду й зниження вираженості симптомів інтоксикації.
На тлі терапії Інгавірином® в дозі 90 мг 1 раз на добу спостерігається вірогідне зниження вираженості симптомів ураження верхніх дихальних шляхів, а також їх тривалості.
Слід зазначити відсутність розвитку бактеріальних ускладнень грипозної інфекції серед пацієнтів, які приймали Інгавірин®.
Отримані результати відображають клінічно вірогідне зниження тяжкості захворювання на тлі терапії Інгавірином®, що підтверджується даними вірусологічних досліджень щодо зниження інфекційних титрів у процесі лікування.
Порівняльний аналіз результатів лікування Інгавірином® і Таміфлю® показує, що їх ефективність при грипі в цілому порівнянна, однак відсутність ускладнень в групі Інгавірину®, а також менша тривалість таких значущих симптомів, як лихоманка, кашель, можуть свідчити про кращий лікувальний ефект Інгавірину®.
Відзначено добру переносимість і безпеку Інгавірину®. Проведений комплекс лабораторних досліджень дозволяє зробити висновок про те, що приймати Інгавірин® необхідно в дозі 90 мг/добу впродовж 5 діб. Курсова доза 450 мг не впливає на функцію печінки і нирок, не викликає змін у складі крові.
Отже, результати проведеного дослідження свідчать про те, що Інгавірин® є ефективним лікарським препаратом при лікуванні грипу у дорослих та забезпечує високу комплаєнтність хворих з рекомендованим режимом терапії. Важливим є те, що препарат можна застосовувати під час вагітності у всіх триместрах і в період лактації.
Ще однією важливою особливістю цього препарату є його доступність завдяки ціновій політиці компанії-виробника, що є економічно вигідним для пацієнтів, а також препарат дуже зручний у прийомі (необхідна лише одна таблетка на добу).
Загалом ці два препарати майже однакові за своєю ефективністю, добре зарекомендували себе під час епідемії грипу у 2016 році, що дозволяє призначати їх як базисну терапію при грипі та ГРВІ.
Слід також зазначити, що незначні побічні дії контрольного препарату мали симптоматичний характер, не потребували відміни лікування й повністю зникли після закінчення курсу лікування.
Результати проведених клінічних досліджень дають підставу рекомендувати обидва лікарські препарати як ефективні й безпечні противірусні засоби для лікування грипу.

/16_u.jpg)
/16_u2.jpg)
/16_u3.jpg)