Журнал «» 2 (34) 2014
Вернуться к номеру
Нужны ли споры на тему: лучше сартаны или ингибиторы АПФ? (часть 1)
Авторы: Радченко А.Д. - ГУ «ННЦ «Институт кардиологии имени акад. Н.Д. Стражеско» НАМН Украины, г. Киев
Рубрики: Семейная медицина/Терапия, Кардиология
Разделы: Медицинское образование
Версия для печати
Данная статья является первой частью обзора данных литературы о механизме действия и эффективности блокаторов рецепторов ангиотензина II (БРА) в снижении артериального давления и предупреждении поражения органов-мишеней. Проводится сопоставление с действием ингибиторов ангиотензинпревращающего фермента (иАПФ). Делаются выводы, что существенной разницы, которая имела бы клиническое значение, между БРА и иАПФ нет.
Представлена стаття є першою частиною огляду даних літератури про механізм дії та ефективність блокаторів рецепторів ангіотензину ІІ (БРА) в зниженні артеріального тиску та попередженні ураження органів-мішеней. Проводиться зіставлення із дією інгібіторів ангіотензинперетворюючого ферменту (іАПФ). Зроблено висновки, що клінічно значущих відмінностей між БРА та іАПФ немає.
This article is the first part of the review of the literature data on the mechanism of action and efficacy of angiotensin receptor blockers II (ARBs) in reducing blood pressure and preventing end-organ damage. A comparison with the action of angiotensin-converting enzyme (ACE) inhibitors is being carried out. The authors concluded that the significant difference, that would have clinical significance between ARBs and ACE inhibitors, hasn’t been found.
ингибиторы ангиотензинпревращающего фермента, сартаны, эффективность, безопасность.
інгібітори ангіотензинперетворюючого ферменту, сартани, ефективність, безпека.
inhibitors of angiotensin-converting enzyme, sartans, efficiency, safety.
Статья опубликована на с. 97-111
В спорах рождается истина,
а она, в свою очередь, рождает споры.
Автор неизвестен
Сколько существуют различные препараты, блокирующие ренин-ангиотензиновую систему (РАС), столько длятся споры о преимуществах одних и недостатках других. Первыми появились и стали использоваться в клинической практике ингибиторы ангио-тензинпревращающего фермента (иАПФ). Затем в 1994 году на рынке появился лозартан — первый блокатор рецепторов ангиотензина II (БРА). С появлением нового класса антигипертензивных препаратов связывали особые надежды, так как считалось, что БРА лучше, чем иАПФ, подавляют эффекты ангиотензина II. Это объяснялось тем, что иАПФ блокируют только основной путь образования ангиотензина II (он может образовываться и другими путями), а БРА блокируют рецепторы к ангиотензину II и тем самым — его действие вне зависимости от того, каким путем произошло образование ангиотензина II. Иными словами, БРА призваны были в большей степени блокировать РАС, чем иАПФ. Кроме того, появились данные, что с течением времени происходит «ускользание» действия иАПФ из-за увеличения образования ангиотензина II другими путями. Все это плюс хорошая переносимость БРА привело к тому, что появились многочисленные исследования, показавшие, что БРА эффективно снижают артериальное давление (АД) [15, 49, 113], улучшают симптоматику при сердечной недостаточности (СН) [16, 18, 21, 32, 67, 68, 73, 88–91], уменьшают прогрессирование поражения почек при сахарном диабете [9, 50, 51, 85, 72, 114], частоту развития инсульта [15, 62, 63, 92, 94], новых случаев сахарного диабета [62, 104] и пароксизмов фибрилляции предсердий [15, 49].
Наряду с данными о положительном влиянии БРА появились свидетельства, что не все так хорошо. Так, в экспериментальных исследованиях было показано, что блокада рецепторов ангиотензина II 1-го типа может приводить к стимуляции рецепторов ангиотензина II 2-го типа, что влечет за собой, кроме позитивных, ряд возможных отрицательных эффектов, которые, в свою очередь, могут иметь клинически проявляющиеся последствия [3, 7, 20, 52, 60, 69, 108]. В некоторых клинических исследованиях появились указания на то, что терапия БРА сопряжена с увеличением риска развития инфаркта миокарда (ИМ) [33, 49]. В нескольких метаанaлизах также было подтверждено, что БРА увеличивают вероятность развития ИМ [98, 99, 100] и практически не влияют на смертность [99]. В ответ стали появляться многочисленные публикации, указывающие на обратное — отсутствие отрицательного влияния БРА на частоту развития ИМ.
Фактически с 2004 года и до настоящего времени ведущие специалисты в области кардиологии считали своим долгом высказать свое мнение или провести свой метаанализ по оценке влияния БРА на частоту развития ИМ и других сердечно-сосудистых осложнений. Более того, в 2010 г. появился метаанализ, утверждающий, что БРА увеличивают риск возникновения рака [96], и за ним тут же последовал метаанализ, опровергающий эти данные [12]. Несмотря на результаты прямого сравнения эффективности иАПФ и БРА у пациентов высокого риска [26, 103], в котором оба класса антигипертензивных препаратов оказались эффективными в предупреждении кардиоваскулярных событий без достоверной разницы между ними, ряд исследователей продолжают проводить новые метаанализы для пациентов высокого риска. Данная статья является, с одной стороны, обзором этих публикаций, с другой — попыткой объяснить читателю, что не все так бесспорно, как утверждают некоторые исследователи, и что в любом анализе всегда можно найти «подводные камни», которые ставят под сомнение его результаты. Поэтому надо стараться максимально критично относиться к любой публикации, особенно если результаты основываются не на прямых рандомизированных сравнительных исследованиях, а на ретроспективных наблюдениях, когортных исследованиях или метаанализах.
Что говорят рекомендации по поводу использования иАПФ и БРА?
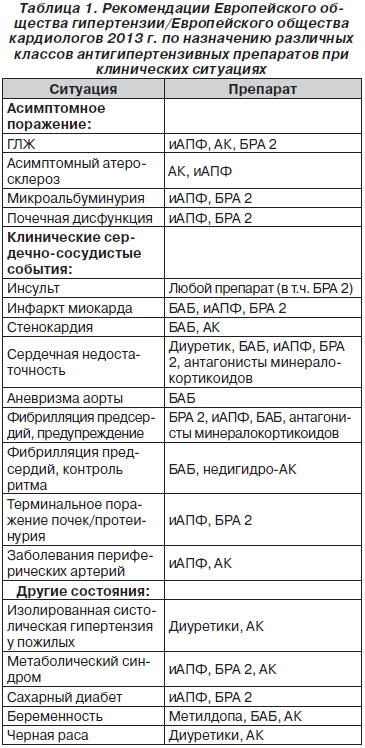
Рекомендации говорят, что основной эффект всех антигипертензивных препаратов связан со снижением АД per se, и выделяют пять классов, которые подходят для начала терапии: бета-блокаторы, диуретики, иАПФ, БРА, антагонисты кальция [1, 2]. В приказе МЗ Украины № 384 от 24.05.2012 «Настанова та клінічний протокол надання медичної допомоги «Артеріальна гіпертензія» указывается, что порядок перечисления лекарственных препаратов не означает приоритетность их применения [1]. Таким образом, на фактически законодательном уровне подтверждается, что разницы между иАПФ и БРА в лечении АГ нет и что врачи могут сами выбирать, что назначать. В европейских рекомендациях также есть оговорка, согласно которой в определенных ситуациях предпочтение следует отдавать определенным классам антигипертензивных препаратов [2]. Они представлены в табл. 1.
Какова частота назначения иАПФ и БРА в мире?
Согласно данным KANTAR HEALTH National Health and Wellness survey 2010, которые были представлены на конгрессе Европейского общества гипертензии в Лондоне 29 апреля 2012 года профессором Х. Girerd, в Европе в среднем 23 % пациентов получают БРА и 28 % — иАПФ [31, 41]. Есть страны, например Франция, в которых доля БРА (24,9 %) значительно больше, чем иАПФ (9,7 %), а, к примеру, в Велико-британии — наоборот: доля иАПФ больше (35,5 против 19,4 %). Если оценить частоту использования БРА и иАПФ в виде монотерапии, то во Франции лидером являются БРА — 30 % назначений против 14 % [115]. Они же преобладают в составе фиксированных комбинаций и во Франции, и в Италии, и в Германии — более 50 % случаев.
В США частота использования БРА ниже, чем иАПФ, но если проследить динамику частоты их применения за период с 2000 по 2010 год, то можно отметить значительный рост использования БРА (с 10,9 до 22,2 %) по сравнению с иАПФ (с 25,5 до 33,3 %) [34]. При этом самыми назначаемыми БРА являются валсартан и лозартан, а иАПФ — лизиноприл и его комбинации.
В Украине же ситуация, которая сложилась с назначениями БРА, по данным SMD за январь 2013 г., явно не в пользу БРА — только 2,5 и 2,6 % от аптечных продаж антигипертензивных препаратов приходится на БРА и их комбинации (на иАПФ и их комбинации — 26,4 и 25,5 % соответственно). Иными словами, в нашей стране разговоры о том, что не следует назначать БРА, не имеют смысла — в отличие от других стран у нас их и так назначают редко.
Насколько различны механизмы действия иАПФ и БРА и их клиническое значение?
БРА и иАПФ — это разные классы антигипертензивных препаратов, которые, соответственно, имеют разные механизмы действия. Противники БРА часто основывают свои утверждения на результатах экспериментальных данных. Но среди экспериментальных данных есть как аргументы против БРА, так и аргументы за.
Аргументы против БРА. Блокада рецепторов ангио-тензина II 1-го типа приводит к тому, что содержание ангиотензина II увеличивается, и это влечет за собой стимуляцию рецепторов ангиотензина II 2-го типа, которая не уравновешивается стимуляцией рецепторов 1-го типа. Длительная стимуляция рецепторов ангиотензина II 2-го типа может запускать апоптоз, подавлять ангиогенез и уменьшать синтез фиброзной ткани, что потенциально способно приводить к подавлению роста коллатеральных сосудов в ответ на ишемию, истончению фиброзной оболочки атеросклеротической бляшки и повышению вероятности ее разрыва [3, 4, 6, 7, 11, 13, 20, 36, 44, 47, 52, 60, 106, 107]. Кроме того, существуют данные, указывающие на то, что стимуляция рецепторов 2-го типа сопряжена с развитием гипертрофии кардиомиоцитов, способствует поддержанию воспаления в почках [47, 59, 60, 112, 114, 116].
При проведении обследования 509 семей, проживающих в Объединенном Королевстве и имеющих в анамнезе раннее развитие ишемической болезни сердца (ИБС), была обнаружена связь между полиморфизмом гена рецепторов 2-го типа (–1332 G/A) и преждевременным развитием ИБС [5]. Это может означать, что преждевременное развитие ИБС связано с экспрессией рецепторов 2-го типа [112].
Помимо рецепторов 2-го типа были обнаружены также рецепторы ангиотензина II 4-го типа, которые связаны с высвобождением ингибитора активатора плазминогена — мощного ингибитора фибринолиза и предиктора развития смерти при трансмуральном ИМ [69]. В настоящее время нет данных, указывающих на то, что назначение БРА приводит к стимуляции рецепторов 4-го типа, однако имеются данные, демонстрирующие, что у инсулинрезистентных пациентов с АГ, принимавших гидрохлортиазид, лечение иАПФ приводило к снижению ингибитора активатора плазминогена, а лечение БРА сопровождалось его увеличением [69].
иАПФ отличаются от БРА способностью увеличивать содержание брадикинина, который ингибирует агрегацию тромбоцитов и циркуляцию ингибитора активатора плазминогена, способствует высвобождению простациклинов, NO и эндотелий-зависимого гиперполяризирующего фактора [106, 117]. Кроме того, брадикинин обладает кардиопротективным действием: ограничивает зону инфаркта, уменьшает вероятность возникновения аритмии, индуцированной ишемией. БРА практически не влияют на содержание кининов [30, 117].
В отличие от БРА для иАПФ показано влияние на функцию эндотелия через другие механизмы. Они способны изменять активность циклооксигеназы-2 (ЦОГ-2), что влечет за собой повышение уровня простациклина (PGI2) и простагландина Е2, не влияя на содержание тромбоксана А2 [53].
Аргументы в пользу использования БРА. Роль рецепторов 2-го типа до конца не изучена. Содержание этих рецепторов изменяется в процессе развития человека (при внутриутробном развитии их количество наибольшее), и при возникновении некоторых патологических состояний (после ИМ, инсульта) их содержание и активность в кардиомиоцитах или нейроцитах увеличиваются [48, 52, 57]. С этим связывают то, что, возможно, рецепторы 2-го типа являются фактором, который способствует росту и развитию. При экспериментальном ИМ у крыс БРА кандесартан и ирбесартан значимо ограничивали зону инфаркта и увеличивали экспрессию рецепторов 2-го типа [48]. При этом не было обнаружено, что недостаток кинина при лечении БРА каким-либо образом влиял на функцию миокарда (что противоречит приведенным выше утверждениям о положительном кардиопротективном действии кининов). Рецепторы 2-го типа в значительном количестве обнаружены в эндокринных клетках, и считается, что они ответственны за локальную циркуляцию и ангиогенез. Аналогично с рецепторами 2-го типа связывают усиление развития коллатеральных сосудов и повышение резистентности к гипоксии нервной ткани, что часто служит объяснением более выраженного церебропротекторного действия БРА [4, 14, 28, 46, 61]. Предварительное назначение кандесартана, но не рамиприла в субгипотензивных дозах приводило к значительному уменьшению зоны инфаркта мозга у крыс при окклюзии церебральных артерий [55].
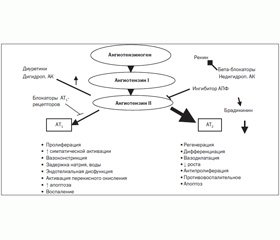
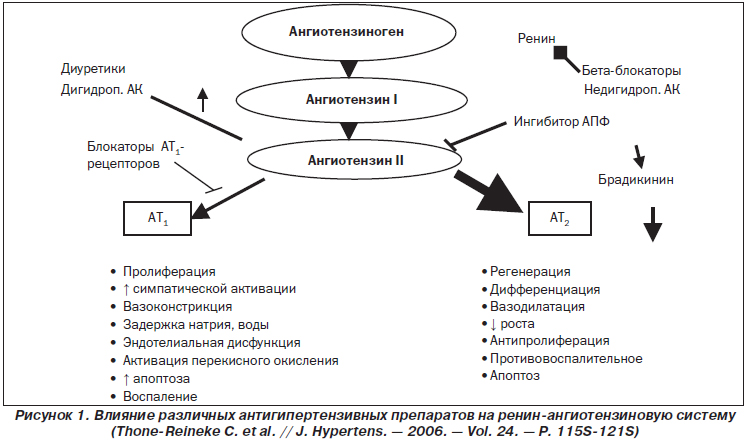
Существуют данные, которые указывают на то, что рецепторы 2-го типа способны отстрочить гибель нервной клетки. То есть их стимуляция не активирует (как указывалось выше), а замедляет апоптоз [7, 20]. В 80-х годах даже возникла теория Fournier, согласно которой ангиотензин II не является таким плохим (рис. 1), как часто о нем говорят [105]. Тогда заметили, что препараты, стимулирующие РАС (диуретики), были более эффективными в предупреждении инсульта, чем препараты, блокирующие РАС (бета-блокаторы). Дело в том, что ангиотензин II может связываться с рецепторами как 1-го, так и 2-го типа. Все плохое, что мы знаем о данном пептиде, опосредуется именно через рецепторы 1-го типа. Активация же рецепторов 2-го типа, наоборот, влечет за собой противоположное действие. Предполагается, что при обычных условиях они обеспечивают вазодилатацию, способствуют высвобождению NO, стимулируют диурез и натрийурез, обладают антипролиферативным действием [57, 59, 82, 106]. В ряде экспериментальных исследований было показано, что рецепторы 2-го типа ингибируют гипертрофические процессы в коронарных артериях, предупреждают их ремоделирование [4]. В обычном состоянии эти рецепторы не активны, но когда случается катастрофа (ишемия), они активируются, и если дать им возможность связаться с ангиотензином II, то последний будет оказывать защитное воздействие на клетку. Именно поэтому в ряде исследований препаратами с более выраженным нейропротекторным эффектом являются те, которые не влияют на содержание (или его увеличивают) ангиотензина II и/или не препятствуют его связыванию с рецепторами 2-го типа: диуретики, дигидропиридиновые антагонисты кальция, сартаны.
Таким образом, в настоящий момент существуют противоречивые экспериментальные данные касательно блокады рецепторов 1-го типа и стимуляции рецепторов 2-го типа, что не позволяет говорить о значимом преимуществе иАПФ и вредном влиянии БРА и экстраполировать эти данные для объяснения их клинического эффекта. Большинство экспериментальных исследований проведено на животных, и их данные нельзя в полной мере переносить на людей — хотя бы по той причине, что количество типов рецепторов ангиотензина II у животных и человека различно. Очень часто оказывается, что экспериментальные данные не подтверждаются при клинических исследованиях. Так, оказалось, что метформин и феноформин, препараты одного класса и фармакологического действия, при клинических исследованиях имели различное влияние на частоту развития ацидоза. Аналогично не все глитазоны нашли свое применение в клинике. Обеспечение двойной блокады при совместном назначении иАПФ и БРА, с точки зрения эксперимента, было бы оптимальным (нет «феномена ускользания», полная блокада РАС, положительные эффекты иАПФ) [107] и, казалось, решило бы все проблемы, но исследование ONTARGET [103] показало, что такая комбинация была сопряжена с увеличением необходимости проведения гемодиализа/вероятности повышения уровня креатинина в 2 раза/смерти — на 9 % (P = 0,037).
Есть ли разница в снижении АД между иАПФ и БРА?
Часто практические врачи, объясняя редкие назначения сартанов, говорят об их слабом антигипертензивном эффекте, хотя данные многих исследований и существующие руководства указывают на одинаковую антигипертензивную эффективность всех препаратов первой линии лечения АГ. Так, согласно данным метаанализа F. Messerli с соавторами (рис. 2), который основывался на результатах наблюдений за степенью снижения среднесуточного (не офисного!) САД и ДАД, существенной разницы между эффективностью иАПФ и БРА обнаружено не было [70]. Более того, БРА оказались даже намного более эффективными, чем тиазидные диуретики. Во французском исследовании FLASH [35], в которое включались пациенты, получавшие монотерапию различными классами антигипертензивных препаратов, частота достижения целевого АД, по данным домашнего самомониторирования (не офисного измерения!), была самой высокой на фоне приема БРА: 73 % — группа сартанов, 68 % — группа антагонистов кальция, 52 % — группа бета-блокаторов, 47 % — группа иАПФ. То есть монотерапия БРА была почти в два раза эффективнее монотерапии иАПФ.
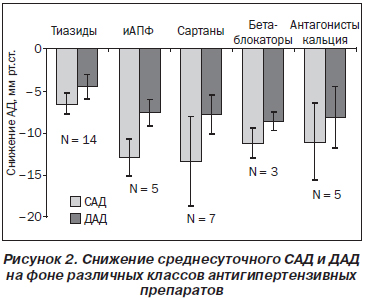
Особенностью всех сартанов является то, что они обладают продолжительностью действия 24 часа и более [24]. Поэтому их удобно назначать один раз в сутки, пропуск времени приема не сопровождается существенным повышением АД. Кроме того, так называемое соотношение «корыто — пик» (степень снижения АД к моменту приема следующей дозы/степень снижения АД на момент максимального действия) для всех сартанов составляет более 70 %. Согласно правилам, утвержденным FDA, в настоящее время для регистрации антигипертензивного препарата необходимо, чтобы его соотношение «корыто — пик» было не менее 50 % — только в этом случае препарат считается безопасным для длительного применения. Но если мы посмотрим на величину этого показателя для различных иАПФ (рис. 3), мы увидим, что у ряда из них она составляет менее 50 % [118]. Однако мы продолжаем их использовать, так как большинство иАПФ были зарегистрированы FDA в то время, когда данное правило еще не было введено.

Различаются ли между собой различные БРА по антигипертензивной эффективности? В литературе можно найти противоречивые данные, которые превозносят одни сартаны перед другими. В частности, говорят, что БРА имеют различное сродство к рецепторам АТ 1-го типа и с этим связаны их преимущества: меньше побочных эффектов, возможность оставлять большее количество свободных АТ2-рецепторов. Согласно одним авторам, наибольшим сродством к рецепторам АТ 1-го типа отличается валсартан, согласно другим — олмесартан [17, 22, 37, 71]. Но никто при этом не доказал, что меньшее сродство означает меньшую антигипертензивную эффективность или меньшее предупреждение кардиоваскулярных событий.
Часто большая степень снижения АД приписывается олмесартану. Но при этом есть результаты исследований, которые свидетельствуют о том, что валсартан сильнее. Так, M. Destro с соавторами показали, что валсартан 160 мг лучше, чем олмесартан 20 мг, снижает среднесуточное САД и ДАД — 15,7/12,2 против 14,6/11,2 мм рт.ст. (Р < 0,05 для ДАД) [19], а С. Calvo с соавторами отметили значительно большую антигипертензивную эффективность валсартана 160 мг по сравнению с телмисартаном 80 мг — 18,6/12,1 против 10,8/8,4 мм рт.ст. (Р < 0,05 для САД и для ДАД) [10]. Основным недостатком большинства подобных исследований является малая выборка пациентов. Многоцентровых же наблюдений по сравнению степени снижения АД между различными сартанами не было, как не было и исследований по сравнению их влияния на частоту возникновения кардиоваскулярных событий.
Имеет ли значение время назначения иАПФ и БРА? В последние годы популярным становится учение об оптимальном времени приема различных, в том числе антигипертензивных, препаратов — хронотерапия. Имеются доказательства того, что и для ингибиторов АПФ, и для БРА иногда более эффективным оказывается прием препаратов на ночь [38, 39, 97]. Более того, существуют исследования, указывающие на то, что даже использование фиксированных комбинаций блокаторов РАС с диуретиками лучше назначать на ночь [97]. Это вызывает некоторое удивление, учитывая, что в состав данной комбинации входит диуретик, который, как правило, назначают утром из-за возможного мочегонного эффекта. Но оказывается, что мочегонный эффект длится первые 3–4 суток, а затем он значительно ослабевает и остается только антигипертензивный эффект. В исследовании R. Hermida с соавторами выбрали две группы пациентов с АГ, которые были рандомизированы получать валсартан + гидрохлортиазид 160/12,5 мг утром или вечером на протяжении 12 недель, затем время приема изменялось на противоположное, и пациент наблюдался еще 12 недель. Оказалось, что и утреннее, и ночное назначение комбинации обеспечивало одинаковое снижение среднесуточного АД. Однако лучший контроль ночного САД (Δ 20,1 против 16 мм рт.ст.) и ПАД (Δ 6,5 против 4 мм рт.ст.), большее снижение доли пациентов non-dipper (с 59 до 23 %), большая доля пациентов, достигших нормализации среднесуточного АД (55 против 40 %, Р = 0,037), были в группе лиц, получавших валсартан + гидрохлортиазид вечером. Диуретический эффект был выражен лишь на протяжении первых 3–4 дней.
Медленное развитие антигипертензивного эффекта БРА — это недостаток? Еще одним возражением практических врачей против назначения БРА является их медленное начало действия. Особенно это беспокоит врачей стационаров, так как за две недели пребывания пациента в отделении нужно успеть нормализовать уровень АД, в противном случае пациент останется недовольным. При этом понятие эффекта первой дозы и начало действия часто путаются. Как правило, чем больше продолжительность действия антигипертензивного препарата, тем реже встречается снижение АД при приеме первой дозы. Последнее расценивается как побочный эффект, которого максимально стараются избежать. Частота встречаемости транзиторного снижения АД на фоне блокаторов РАС в среднем составляет 2,5 % (на фоне иАПФ с продолжительностью действия менее 24 часов эта величина может быть выше). Поэтому в целях безопасности часто советуют рекомендовать пациентам первый прием антигипертензивного препарата в офисе врача. При этом обязательно нужно исключать прочие причины снижения АД: другие гипотензивные препараты, потерю жидкости (особенно на фоне петлевых диуретиков), cтеноз почечных артерий, кардиальные заболевания (инфаркт миокарда, сердечная недостаточность, аритмия), неврогенные заболевания (болезнь Паркинсона), печеночную недостаточность, сепсис, кровотечение.
После эффекта первой дозы, как правило, АД повышается и начинает стабильно снижаться спустя какое-то время. Максимальный антигипертензивный эффект развивается при выходе препарата на плато действия. Для различных классов и их представителей это плато действия возникает через различные промежутки времени. Так, от бета-адреноблокаторов снижения АД можно ожидать уже на 2–7-е сутки (для небиволола — через 14 дней). Для антагонистов кальция длительного действия время достижения плато составляет 7–14 дней, для тиазидных и тиазидоподобных диуретиков — от 3 дней (собственно диуретический эффект) до 4 недель (антигипертензивный эффект), для иАПФ и сартанов — от 10 дней до 4 недель. Таким образом, чтобы оценить антигипертензивный эффект препарата, необходимо подождать. В большинстве рандомизированных исследований, в том числе и с БРА, и с иАПФ, протоколы так и составлялись — титрация дозы производилась после выхода назначенной дозы препарата на плато.
К сожалению, ни одно руководство не дает ответа на вопрос, как быстро следует достигнуть целевого уровня АД. Единственное, что мы имеем, — это исследование VALUE, которое продемонстрировало, что раннее (на протяжении уже первого месяца лечения) снижение САД на 10 мм рт.ст. и более сопряжено с лучшим прогнозом по сравнению с более поздним снижением АД [113]. Резонно было бы предположить, что у пациентов высокого/очень высокого риска сердечно-сосудистых осложнений АД необходимо снижать раньше, чем у пациентов умеренного и низкого риска. Так, например, если предположить, что у пациента очень высокого риска вероятность возникновения осложнений на протяжении следующих 10 лет составляет 50 %, то на протяжении одного месяца — 0,4 %. А это означает, что у одного из 250 больных, у которых АД не снизили, возможно возникновение осложнения. Как же быть тогда с ожиданием выхода на плато через месяц? Согласно данным анализа D. Lasserson c соавторами, в среднем у всех антигипертензивных препаратов пик действия определяется на 4-й неделе, но 50 % от максимального эффекта можно ожидать уже на 1-й неделе лечения (рис. 4) [58]. Иными словами, если приблизительно к 1-й неделе САД снизилось на 10 мм рт.ст., то на 4-й неделе можно ожидать снижения как минимум на 20 мм рт.ст. Если этого достаточно для достижения целевого показателя, то лечение можно продолжать, если нет, то возможны варианты: или увеличить дозу, или добавить другой антигипертензивный препарат.
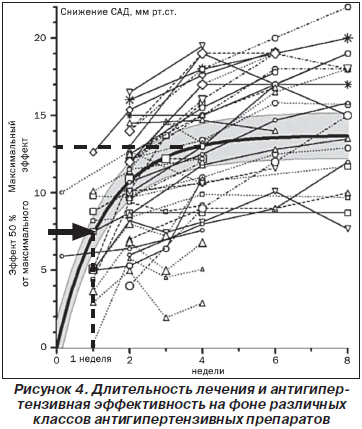
Большинство руководств рекомендуют использовать комбинированную терапию как стартовую для всех пациентов с уровнем АД ≥ 160/100 мм рт.ст. или высокого/очень высокого риска. Поэтому у таких пациентов нет необходимости долго ждать выхода на плато, нужно сразу использовать возможности комбинации. Для улучшения приверженности пациента к лечению, особенно при первичном назначении терапии, лучше использовать фиксированные комбинации (чтобы не пугать пациента сразу большим количеством таблеток). Это подтверждено украинскими рекомендациями по диагностике и лечению АГ, утвержденными приказом МЗ № 384 от 24.05.2012, в которых указано, что для пациентов со 2-й и 3-й степенью повышения АД или пациентов высокого/очень высокого риска терапию рациональнее начинать с фиксированной комбинации [1]. Среди фиксированных комбинаций, имеющих в своем составе сартаны, наиболее часто используемыми являются комбинации «БРА + диуретик». Компания «КРКА Украина» (Словения) на рынке Украины предлагает две такие комбинации — «лозартан ++ гидрохлортиазид» и «валсартан + гидрохлортиазид» в различных дозировках — 50/12,5 мг (лориста-Н), 100/12,5 мг (лориста-Н 100), 100/25 мг (лориста-НД) и 160/12,5 мг (вальсакор-Н), 160/25 мг (вальсакор-НД), 320/12,5 (вальсакор-Н 320), 320/25 мг (вальсакор-НД 320) соответственно, что значительно облегчает индивидуальный подбор терапии.
В основе более выраженного эффекта при использовании сразу двух антигипертензивных препаратов лежит следующий принцип. Как правило, в популяции существуют колебания в ответе на назначение антигипертензивного препарата. Так, одни пациенты отвечают на назначение блокаторов РАС значительным снижением АД, а другие — незначительным (рис. 5). При этом у одних пациентов увеличение дозы сопровождается значительным увеличением антигипертензивного эффекта, а у других антигипертензивный эффект увеличивается не так значительно. Амплитуда колебаний ответа различна для различных классов. Чем она меньше, тем большая вероятность того, что, назначив данный препарат, вы получите хорошее снижение АД у большинства пациентов.
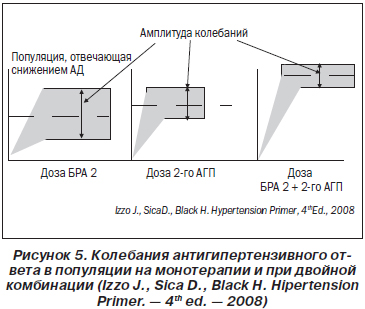
Такой маленькой амплитудой обладает клонидин. Почти все пациенты реагируют на его прием снижением АД. Далее по возрастанию следуют антагонисты кальция, диуретики, бета-адреноблокаторы = иАПФ = БРА. При назначении двух классов антигипертензивных препаратов (рис. 5) амплитуда колебаний ответа значительно уменьшается, а это значит, что значительно большее количество пациентов ответят снижением АД. Кроме того, это снижение будет более значительным, чем при использовании монотерапии. Так, известно, что блокаторы РАС менее эффективны в снижении АД у пациентов пожилого возраста или афроамериканцев в силу низкой активности у них РАС. В исследовании B. Everett с соавторами было показано, что использование комбинации валсартана с гидрохлортиазидом увеличивало степень снижения АД более чем в два раза по сравнению с монотерапией у вышеуказанной категории больных [23].
Таким образом, не существует разницы между иАПФ и БРА по степени снижения АД. Все БРА в отличие от некоторых иАПФ имеют продолжительность действия более 24 часов и соотношение «корыто — пик» более 70 %, что позволяет назначать их один раз в сутки и обеспечивает плавный стойкий антигипертензивный эффект. У пациентов высокого/очень высокого риска или с уровнем САД/ДАД ≥ 160/100 мм рт.ст. рекомендовано начинать лечение с назначения фиксированных комбинаций. Для увеличения эффективности комбинации «блокатор РАС (иАПФ или БРА) + диуретик», особенно у пациентов с недостаточным снижением АД в ночное время и высоким подъемом утреннего АД, может быть рекомендовано ее вечернее назначение.
Возможности влияния иАПФ и БРА на поражение органов-мишеней
Как правило, большинство исследователей говорят о том, что нет существенной разницы между влиянием иАПФ и БРА на органы-мишени. И те, и другие способны вызывать регресс гипертрофии левого желудочка (ГЛЖ), протеинурии, улучшать эластичность артерий. Однако есть единичные указания на то, что разница существует.
Влияние на ГЛЖ. В одном из последних метаанализов, посвященных оценке регресса ГЛЖ на фоне различных классов антигипертензивных препаратов (рис. 6), говорится, что уменьшение индекса массы миокарда во многом зависит от снижения АД [25]. При одинаковом эффективном контроле АД не имеет значения, принимает пациент диуретики, антагонисты кальция, иАПФ или нет, — в любом случае будет регресс гипертрофии. Однако существует достоверная разница между группами лиц, получавших и не получавших БРА. При одинаковом контроле АД на фоне БРА достоверно в большей степени уменьшилась величина индекса массы миокарда, чем на фоне другой антигипертензивной терапии, что говорит о возможном АД-независимом действии БРА на миокард. С другой стороны, бета-адреноблокаторы достоверно уступали во влиянии на гипертрофию другим классам антигипертензивных препаратов.
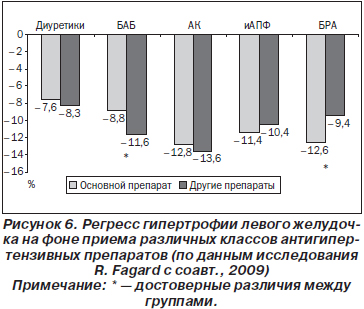
Возможно, именно с таким выраженным положительным влиянием БРА на ГЛЖ связана их эффективность в предупреждении пароксизмов фибрилляции предсердий. Согласно последним рекомендациям Европейского общества кардиологов/Европейского общества гипертензии 2013 г., БРА являются препаратами выбора у пациентов с АГ и пароксизмальной/персистирующей формой фибрилляции предсердий (табл. 1). Это связано с тем, что в двух больших исследованиях было продемонстрировано достоверное снижение частоты пароксизмов фибрилляции предсердий: на 33 % при использовании лозартана (исследование LIFE) у больных с АГ и ЭКГ-признаками ГЛЖ [111] и на 37 % при использовании валсартана (исследование Val-HeFT) у больных с клиническими признаками сердечной недостаточности [65]. Cледует отметить, что данный эффект отмечался только у пациентов с нарушенной внутрисердечной гемодинамикой (на фоне ГЛЖ или систолической/диастолической дисфункции). В других исследованиях, в которых валсартан или ирбесартан назначали всем подряд больным с фибрилляцией предсердий в анамнезе (исследования GISSI-AF и ACTIVE) без учета наличия ГЛЖ или признаков сердечной недостаточности, не было получено достоверного влияния БРА на частоту возникновения пароксизмов фибрилляции предсердий [101]. В подисследовании LIFE при проведении ЭхоКГ было подтверждено, что связь между регрессом ГЛЖ и уменьшением частоты пароксизмов фибрилляции предсердий опосредуется значимым уменьшением размеров левого предсердия (за счет улучшения диастолической функции левого желудочка при регрессе ГЛЖ).
В недавнем обсервационном датском исследовании, которое опубликовано в декабре 2013 г. в журнале European Heart Journal, было показано, что назначение иАПФ или БРА пациентам с АГ без СН, ИБС, сахарного диабета или нарушений функции шитовидной железы ассоциируется с уменьшением частоты пароксизмов фибрилляции предсердий по сравнению с назначением монотерапии бета-блокаторами и диуретиками [66]. В этом анализе сопоставили группу гипертензивных пациентов без истории фибрилляции предсердий, получавших монотерапию иАПФ, с группами монотерапии бета-блокаторами (n = 48 658), диуретиками (n = 69 630), антагонистами кальция (n = 57 646) и БРА (n = 20 158). Затем сопоставили группы монотерапии БРА с группами монотерапии бета-блокаторами (n = 20 566), диуретиками (n = 20 832), антагонистами кальция (n = 20 232)и иАПФ (n = 20 158). Оказалось, что по сравнению с бета-блокаторами и диуретиками иАПФ/БРА уменьшали вероятность возникновения фибрилляции предсердий на 88/90 и 49/57 % соответственно. По сравнению с антагонистами кальция достоверной разницы не было. При этом БРА обеспечивали достоверное снижение частоты фибрилляции предсердий на 32 % даже по сравнению с иАПФ.
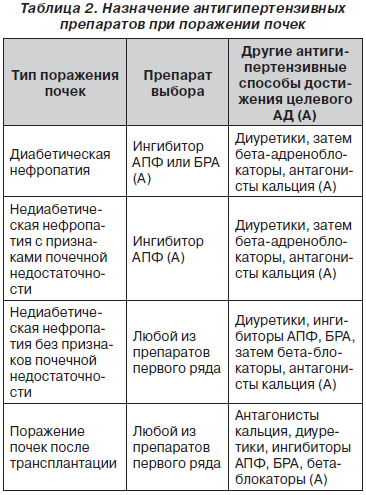
Влияние на почки. Поражение почек определяется снижением скорости клубочковой фильтрации (СКФ) и/или наличием протеинурии (микроальбуминурии — 30–300 мг/сут, макроальбуминурии ≥ 300 мг/сут). Согласно рекомендациям Национальной фундации почек 2002 г. (National Kidney Foundation), антигипертензивные препараты при хроническом заболевании почек назначаются следующим образом (табл. 2): при диабетическом поражении — блокаторы РАС (или иАПФ, или БРА), при недиабетическом поражении без признаков почечной недостаточности — любые антигипертензивные препараты, при недиабетическом поражении с признаками хронической почечной недостаточности — иАПФ (в случае непереносимости БРА); после трансплантации почек — любые антигипертензивные препараты (нет доказательств преимущества каких-либо классов) [42]. В последующих рекомендациях по лечению диабетической нефропатии говорится, что при сахарном диабете 1-го типа преимущества имеют иАПФ (большинство исследований проводилось именно с этими блокаторами РАС), при сахарном диабете 2-го типа и наличии микроальбуминурии врач может назначить или иАПФ, или БРА, при наличии макроальбуминурии предпочтение следует отдавать БРА [51]. В более поздних рекомендациях National Kidney foundation 2012 г. по лечению АГ при поражении почек на первом месте стоят БРА [50]. Это обусловлено большим количеством исследований, в которых БРА назначались пациентам с сахарным диабетом 2-го типа и протеинурией. Практически для каждого представителя класса сартанов существуют доказательства уменьшения протеинурии (регресс микроальбуминурии, предупреждение перехода микроальбуминурии в макроальбуминурию) [100], а согласно данным исследования LIFE, уменьшение протеинурии на этапе «один год от начала лечения» сопряжено с достоверным уменьшением риска развития кардиоваскулярных осложнений [43]. Первые данные об эффективности БРА при диабетической нефропатии были получены для лозартана (исследование RENAAL) и ирбесартана (исследование IDNT) в 2001 году. Назначение этих препаратов по сравнению с плацебо и амлодипином (исследование IDNT) замедляло прогрессирование поражения почек, которое определялось как удвоение уровня креатинина или развитие терминальной стадии почечной недостаточности. Затем появились результаты исследования MARVAL, в котором валсартан по сравнению с амлодипином при одинаковом снижении АД обеспечивал более выраженное уменьшение протеинурии [110], причем положительное влияние валсартана на протеинурию было отмечено как у нормотензивных, так и у гипертензивных пациентов, что позволило рекомендовать назначение БРА пациентам с сахарным диабетом и протеинурией независимо от наличия у них повышенного АД.
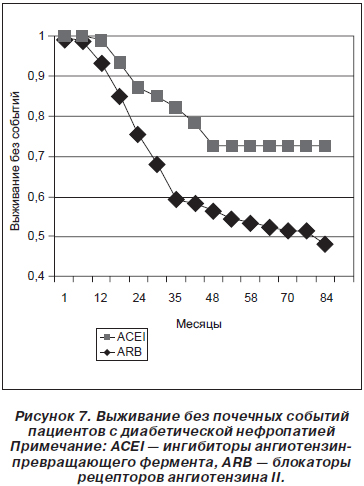
В исследовании N. Robles с соавторами был проведен ретроспективный анализ выживания пациентов с диабетической нефропатией без почечных событий в зависимости от базовой терапии — на основе или иАПФ, или БРА [93]. Оказалось, что на фоне БРА выживание было достоверно лучшим (рис. 7).
При недиабетической нефропатии, как указывалось выше, преимущество имеет назначение иАПФ. Однако в случае непереносимости иАПФ нужно назначать БРА, так как есть данные отдельных исследований, продемонстрировавших их эффективность у данной категории пациентов [45, 76]. Так, в исследовании T. Ishimitsu c cоавторами при одинаковом контроле АД на фоне плацебо уровень креатинина за год значительно вырос — с 1,9 ± 0,5 до 2,3 ± 0,8 мг/дл (p < 0,001), а на фоне валсартана он достоверно не изменился (2,1 ± 0,6 и 2,2 ± 0,9 мг/дл соответственно), и протеинурия значительно уменьшилась [45].
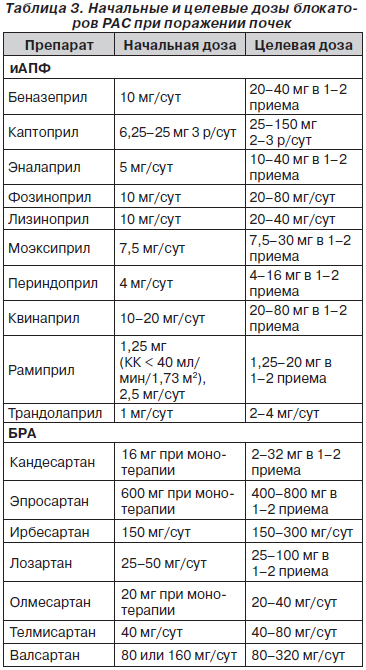
При лечении пациентов с поражением почек всегда необходимо помнить о правилах назначения блокаторов РАС, одним из которых является использование целевых доз (табл. 3). В большинстве исследований с применением препаратов этих классов был продемонстрирован дозозависимый эффект на протеинурию. Необходимо также помнить, что все БРА выводятся в основном с печенью. Поэтому их безопасно назначать при нарушенной функции почек и следует соблюдать осторожность при желчекаменной болезни и печеночной недостаточности.
Cогласно данным одного из последних проспективных когортных исследований, и иАПФ, и БРА могут снизить риск диализа у пациентов с хроническим поражением почек [40, 83]. В это исследование было включено 28 497 пациентов с первичным диагнозом V стадии хронического заболевания почек (ХЗП), с гипертензией и анемией. Пациентов разделили на группы — принимавших (n = 14 117) или не принимавших (n = 14 380) иАПФ или БРА. По истечении периода наблюдения, составившего в среднем 7 месяцев, 70,7 % изучаемой популяции нуждались в проведении длительного диализа, а 20 % умерли до того, как им потребовался длительный диализ. Применение ингибиторов АПФ или блокаторов рецепторов ангиотензина II было связано с более низким риском необходимости длительного диализа (HR = 0,94, ДИ 0,91–0,97) и комбинированным риском длительного диализа или смерти (HR = 0,94, ДИ 0,92–0,97). У пациентов, которым были назначены иАПФ или БРА, отмечался более высокий уровень развития госпитализаций по поводу гиперкалиемии по сравнению с непринимавшими (9,2 % против 6,7 %, р < 0,001), но это не влияло на риск смерти от гиперкалиемии до диализа (HR = 1,03, ДИ 0,92–1,16). Результаты не различались в зависимости от вида монотерапии — иАПФ или БРА. По оценкам иcследователей, каждый год прием иАПФ/БРА может защитить 5,5 % пациентов, пребывающих на поздних стадиях ХЗП, от необходимости начала длительного диализа, и прекращение терапии блокаторами РАС может ускорить начало терминальной стадии почечной болезни.
Еще недавно велись активные споры о возможности применения комбинации иАПФ и БРА у пациентов с поражением почек. В одних исследованиях показано, что в ситуациях, когда АД хорошо контролируется, а протеинурия продолжает нарастать, данная комбинация эффективна [56, 64, 72, 109]. В рандомизированном сравнительном исследовании ONTARGET назначение такой комбинации было сопряжено с увеличением частоты осложнений (гиперкалиемии, гипотонии, почечных событий) и не приводило к улучшению исходов заболевания у пациентов высокого риска. В конце 2013 г. появились также сообщения о досрочном окончании исследования VА-NEPHRON-D, в котором принимали участие пациенты с диабетической нефропатией, рандомизированные получать или лозартан, или комбинацию «лозартан + лизиноприл» [29]. Не было установлено достоверной разницы в частоте кардиоваскулярных событий между группами лечения, а частота гиперкалиемии и острого ухудшения функции почек была выше в группе комбинации. Поэтому в настоящее время использование такой комбинации считается неоправданным и не рекомендуется.
Влияние на сосуды. Согласно рекомендациям Европейского общества гипертензии/Европейского общества кардиологов 2013 г. (табл. 1), при наличии признаков асимптомного атеросклероза преимущества в назначении имеют иАПФ и антагонисты кальция. Однако это не означает, что сартаны невозможно применять при этих состояниях. Так, в исследовании LIFE было показано, что назначение лозартана приводило к достоверному по сравнению с атенололом уменьшению толщины комплекса интима-медиа у пациентов с АГ и ГЛЖ [27, 79].
Это также было продемонстрировано и для других БРА: телмисартана [75], кандесартана [81], валсартана [54, 78], ирбесартана [74].
Кроме того, были получены данные, что представитель БРА валсартан способствует замедлению развития коронарного атеросклероза [86, 87]. Так, в исследовании VALVACE в группе пациентов, получавших валсартан, наблюдалось значительно меньше рестенозов после стентирования, чем в группе иАПФ (рамиприл, каптоприл, эналаприл). Особенно это было выражено у пациентов с острым коронарным синдромом и при наличии сахарного диабета. Позднее это подтвердилось в исследовании Т. Okaka с соавторами, в котором вероятность рестенозов после установки металлических стентов составила 14,5 % в группе валсартана и 27,8 % в группе контроля (Р = 0,024) [77]. При назначении валсартана пациентам с установленными элютинг-стентами разницы с группой сравнения в количестве рестенозов через 8 месяцев наблюдения не было, однако количество новых поражений коронарных артерий было меньшим в группе валсартана, что доказывает антиатеросклеротический эффект БРА [83].
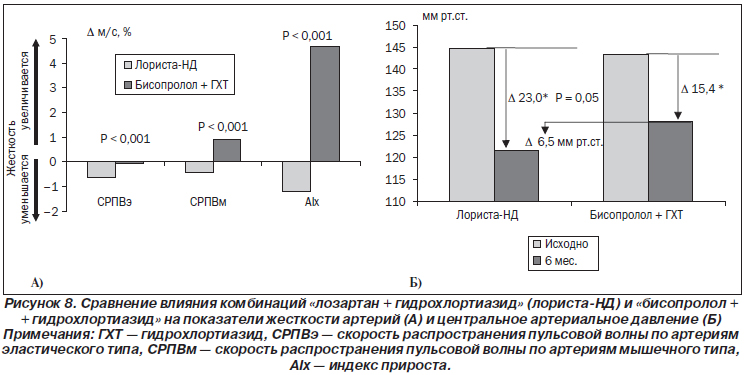
Согласно данным метаанализа, назначение любых антигипертензивных препаратов способствует уменьшению жесткости артерий из-за снижения АД [80]. Однако степень этого положительного влияния может быть разной для различных классов или даже для представителей одного и того же класса (например, бета-адреноблокаторы с вазодилатирующим эффектом и без него). При сопоставлении, которое проводилось в исследовании на базе отделения симптоматических гипертензий ГУ «ННЦ «Институт кардиологии имени академика Н.Д. Стражеско» НАМНУ, динамики скорости распространения пульсовой волны (характеризует жесткость артерий) на фоне лечения различными классами антигипертензивных препаратов (сартаны, иАПФ, антагонисты кальция) было выявлено, что через 6 месяцев лечения во всех группах наблюдалось достоверное снижение изучаемого показателя. Однако на фоне БРА это происходило значительно быстрее — уже на 3-м месяце лечения. В дальнейшем нами было проведено сравнение эффективности двух комбинаций — «лозартан 100 мг + гидрохлортиазид 25 мг» (лориста-НД производства компании КРКА, Словения) и «бисопролол 10 мг (конкор производства компании «Никомед», Германия) + гидрохлортиазид 25 мг (гипотиазид производства компании «Санофи-Авентис», Франция)». При одинаковом снижении офисного и среднесуточного АД комбинация «БРА + диуретик» обеспечивала более выраженное снижение центрального САД и достоверно большую динамику скорости распространения пульсовой волны, чем комбинация «бета-блокатор + диуретик» (рис. 8). При этом негативное влияние бисопролола на скорость распространения пульсовой волны и индекс прироста и недостаточное снижение центрального САД во многом объясняются значительным замедлением ЧСС. В то же время снижение ЧСС на фоне лечения лозартаном не сопровождалось негативным влиянием.
В исследовании EXPLOR сравнивали две группы — получавших терапию комбинациями «амлодипин + валсартан» и «амлодипин + атенолол» [8]. Оказалось, что снижение скорости распространения пульсовой волны наблюдалось в обеих группах, однако в группе атенолола оно зависело от степени снижения ЧСС и АД. В группе же валсартана положительное влияние на жесткость не зависело от степени снижения ЧСС и АД.
Таким образом, к настоящему моменту не существует данных, говорящих о том, что БРА или иАПФ обладают преимуществами, которые имели бы клиническое значение, в механизме действия, снижении АД или предупреждении поражения органов-мишеней. В следующей части данной статьи будут рассмотрены вопросы сравнения эффективности БРА и иАПФ в предупреждении кардиоваскулярных событий и сравнения безопасности использования данных классов антигипертензивных препаратов.

1. Настанова та клінічний протокол надання медичної допомоги «Артеріальна гіпертензія». Наказ МОЗ України № 384 від 24.05.2012. — Київ, 2012. — 107 с.
2. 2013 ESH/ESC Guidelines for the management of arterial hypertension TheTask Force for the management ofarterial hypertension of the European Society ofHypertension (ESH) and of the European Society of Cardiology (ESC) // Journal of Hypertension. — 2013. — Vol. 31. — P. 1281-1357.
3. Akishita M., Horiuchi M., Yamada H. et al. Inflammation influences vascular remodeling through AT2 expression and signaling // Physiol Genom. — 2000. — Vol. 2. — P. 13-20.
4. Akishita M., Iwai M., Wu L. et al. Inhibitory effect of angiotensin II type 2 receptor on coronary arterial remodelling after aortic banding in mice // Circulation. — 2000. — Vol. 102. — P. 1684-1689.
5. Alfakih K., Lawrance R.A., Maqbool A. et al. The clinical significance of a common, functional, X-linked angiotensin II type 2-receptor gene polymorphism (–1332 G/A) in a cohort of 509 families with premature coronary artery disease // Eur. Heart J. — 2005. — Vol. 26. — P. 584-589.
6. Benndorf R., Boger R.H., Ergun S. et al. Angiotensin II type 2 receptor inhibits vascular endothelial growth factor-induced migration and in vitro tube formation of human endothelial cells // Circ. Res. — 2003. — Vol. 93. — P. 438-447.
7. Benneti M., Macdonald K., Chan S. et al. Cooperative interactions between RB and p53 regulate cell proliferation, cell senescence, and apoptosis in human vascular smooth muscle cells from atherosclerotic plaques // Cir. Res. — 1998. — Vol. 82. — P. 704-712.
8. Boutouyrie P., Beaussier H., Achouba A., Laurent S. for the EXPLOR trialist. Destiffening effect of valsartan and atenolol: influence of heart rate and blood pressure // J. Hypertens. — 2014. — Vol. 32. — P.108-114.
9. Brenner B., Cooper M., de Zeeuw D. et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy // N. Engl. J. Med. — 2001. — Vol. 345. — P. 861-869.
10. Calvo C., Termida I., Ayala D.E. Effects of telmisartan 80 mg and valsartan 160 mg on ambulatory blood pressure in patients with essential hypertension // J. Hypertens. — 2004. — Vol. 22. — P. 837-846.
11. Cao Z., Dean R., Wu L. et al. Role of angiotensin receptor subtypes in mesenteric vascular proliferation and hypertrophy // Hypertension. — 1999. — Vol. 34. — P. 408-414.
12. Connolly S., Yusuf S., Swedberg K. et al. Effects of telmisartan, irbesartan, valsartan, candesartan, and losartan on cancers in 15 trials enrolling 138 769 individuals // J. Hypertension. — 2011. — Vol. 29 (4). — P. 623-635.
13. D’Amore A., Black M.J., Thomas W.G. The angiotensin II type 2 receptor causes constitutive growth of cardiomyocytes and does not antagonize angiotensin II type 1 receptor-mediated hypertrophy // Hypertension. — 2005. — Vol. 46. — P. 1347-1354.
14. Dai W., Funk A., Herdegen T. et al. Blockade of central angiotensin AT1 receptors improves neurological outcome and reduces expression of AP-1 transcription factors after focal brain ischemia in rats // Stroke. — 1999. — Vol. 30. — P. 2391-2399.
15. Dahlof B., Devereux R.B., Kjeldsen S.E. et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol // Lancet. — 2002. — Vol. 359. — P. 995-1003.
16. Dalby A., McMurray J. VALIANT trial results support use of valsartan in acute myocardial infarction // Cardiovasc Journal of South Africa. — 2003. — e-publication 5 December 2 — P. 1-3 (www.cvjsa.co.za).
17. de Gasparo M., Whitebread S. Binding of valsartan to mammalian angiotensin AT1 receptors // Regul. Pept. — 1995. — Vol. 59. — P. 303-311.
18. Demers C., McMurray J.J., Swedberg K. et al. Impact of candesartan on nonfatal myocardial infarction and cardiovascular death in patients with heart failure // JAMA. — 2005. —Vol. 294. — P. 1794-1798.
19. Destro M., Scabrosetti R., Vanasia A., Mugellini A. Comparative effi cacy of valsartan and olmesartan in mild-to-moderate hypertension: results of 24-hour ambulatory blood pressure monitoring // Adv. Ther. — 2005. — Vol. 22, № 1. — P. 32-43.
20. Diap Q., Li J., Schiffrin E. In vivo study of AT1 and AT2 angiotensin receptors in apoptosis in rat blood vessels // Hypertension. — 1999. — Vol. 34. — P. 617-624.
21. Dickstein K., Kjekshus J. Effects of losartan and captopril on mortality and morbidity in high-risk patients after acute myocardial infarction: the OPTIMAAL randomised trial: Optimal Trial in Myocardial Infarction with Angiotensin II Antagonist Losartan // Lancet. — 2002. — Vol. 360. — P. 752-760.
22. Edwards R.M., Aiyar N., Ohlstein E.H. et al. Pharmacological characterization of the nonpeptide angiotensin II receptor antagonist, SK&F 108566 // J. Pharmacol. Exp. Ther. — 1992. — Vol. 260. — P. 175-181.
23. Everett B.M., Glynn R.J., Danielson E. et al. Combination therapy versus monotherapy as initial treatment for stage 2 hypertension: a prespecified subgroup analysis of a community-based, randomized, open-label trial // Clin. Ther. — 2008. — Vol. 30. — P. 661-672.
24. Fabia M.J., Abdilla N., Oltra R., Fernandez C., Redon J. Antihypertensive activity of angiotensin II AT1 receptor antagonists: A systematic review of studies with 24 h ambulatory blood pressure monitoring // J. Hypertens. — 2007. — Vol. 25. — P. 1327-1336.
25. Fagard R., Celis H., Thijs L., Wouters S. Regression of Left Ventricular Mass by Antihypertensive Treatment A Meta-Analysis of Randomized Comparative Studies // Hypertension. — 2009. — Vol. 54. — P. 1084-1091.
26. Fitchett D. Results of the ONTARGET and TRANSCEND studies: an update and discussion // Vascular Health and Risk Management. — 2009. — Vol. 5. — P. 21-29.
27. Fossum E., Olsen M., Hцieggen A. et al. Long-Term Effects of a Losartan-Compared With an Atenolol-Based Treatment Regimen on Carotid Artery Plaque Development in Hypertensive Patients With Left Ventricular Hypertrophy: ICARUS, a LIFE Substudy // J. Clin. Hypertens. — 2006. — Vol. 8. — P. 169-173.
28. Fournier A., Achard J., Boutitie F. et al. Is the angiotensin II type 2 receptor cerebroprotective? // Curr. Hypertens. Rep. — 2004. — Vol. 6. — P. 182-189.
29. Fried L., Emanuele N., M.D., Zhang J. et al. Combined Angiotensin Inhibition for the Treatment of Diabetic Nephropathy // N. Engl. J. Med. — 2013. — Vol. 369. — P. 1892-1903.
30. Galliant S., Busche S., Raizada M. et al. The angiotensin II type 2 receptor: an enigma with multiple variations // Am. J. Physiol. Endocrinol. Metab. — 2000. — Vol. 278. —P. 357-374.
31. Girerd X., Mourad J., Vaisse B. et al. Estimation of the number of patients treated for hypertension, diabetes or hyperlipidemia in France (Flash Study 2002) // Arch. Mal. Coeur Vaiss. — 2003. — Vol. 96. — P. 750-753.
32. Granger B.B., Swedberg K., Ekman I. et al. Adherence to candesartan and placebo and outcomes in chronic heart failure in the CHARM programme: double-blind, randomised, controlled clinical trial // Lancet. — 2005. — Vol. 366. — P. 2011.
33. Granger B., McMurray J.J., Yusuf S. et al. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function intolerant to angiotensin-converting-enzyme inhibitors: the CHARM-Alternative trial // Lancet. — 2003. — Vol. 362. — P. 772-776.
34. Gu Q., Burt V., Dillon C., Yoon S. Trends in Antihypertensive Medication Use and Blood Pressure Control Among United States Adults With Hypertension: The National Health and Nutrition Examination Survey, 2001 to 2010 // Circulation. — 2012. — Vol. 126. — P. 2105-2114.
35. Hannon O., Laroche P., Vidal J.S. et al. Assessment of antihypertensive monotherapies effectiveness by home blood pressure self-measurement in hypertensive patients // Ann. Cardiol. Angeiol. (Paris). — 2012. — Vol. 61 (3). — P. 218-23.
36. Haulica I., Walther Bild W., Serban D. Review: Angiotensin Peptides and their Pleiotropic Actions // J. Renin Angiotensin Aldosterone Syst. — 2005. — Vol. 6. — P. 121-131.
37. Herbert J.-M., Delisee C., Dol F. et al. Effect of SR 47436, a novel angiotensin II AT1 receptor antagonist, on human vascular smooth muscle cells in vitro // Eur. J. Pharmacol. — 1994. — Vol. 251. — P. 143-50.
38. Hermida R.C., Ayala D.E., Calvo C. Optimal timing for antihypertensive dosing: focus on valsartan // Ther. Clin. Risk Manag. — 2007. — Vol. 3(1). — P. 119-131.
39. Hermida R.C., Smolensky M.H. Chronotherapy of hypertension // Curr. Opin. Nephrol. Hypertens. — 2004. — Vol. 13(5). — P. 501-505.
40. Hsu T.-W., Jia-Sin Liu, Szu-Chun Hung et al. Renoprotective Effect of Renin-Angiotensin-Aldosterone System Blockade in Patients With Predialysis Advanced Chronic Kidney Disease, Hypertension, and Anemia // JAMA Intern. Med. — 2014. — Vol. 174(3). — P. 347-354.
41. http://www.kantarhealth.com
42. http://www.kidney.org/professionals/KDOQI/guidelines_bp/index.htm
43. Ibsen H., Olsen M.H., Wachtell K. et al. Reduction in albuminuria translates to reduction in cardiovascular events in hypertensive patients: a LIFE study // Hypertension. — 2005. — Vol. 45. — P. 198-202.
44. Ichihara S., Senbonmatsu T., Price E. Jr. et al. Angiotensin II type 2 receptor is essential for left ventricular hypertrophy and cardiac fibrosis in chronic angiotensin II-induced hypertension // Circulation. — 2001. — Vol. 104. — P. 346-351.
45. Ishimitsu T., Kakeda T., Akashiba A. et al. Effects of valsartan on the progression of chronic renal insufficiency in patients with nondiabetic renal diseases // Hypertension Research. — 2005. — Vol. 28. — P. 865-870.
46. Iwai M., Liu H., Chen R. et al. Possible inhibition of focal cerebral ischemia by angiotensin II type 2 receptor stimulation // Circulation. — 2004. — Vol. 110. — P.843-848
47. Jцhren O., Dendorfer A., Dominiak P. Review Cardiovascular and renal function of angiotensin II type-2 receptors // Cardiovascular Research. — 2004. — Vol. 62. — P. 460-467.
48. Jugdutt B., Menon V. Upreg ulation of angiotensin II type 2 receptor and limitation of myocardial stunning by angiotensin II type 1 receptor blockers during reperfused myocardial infarction in the rat // J. Cardiovasc. Pharmacol. Ther. — 2003. — Vol. 8. — P. 217-26.
49. Julius S., Kjeldsen S.E., Weber M. et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial // Lancet. — 2004. — Vol. 363. — P. 2022-2031.
50. KDIGO Clinical Practice Guideline for the Management of Blood Pressure in Chronic Kidney Disease // Kidney international supplements. — 2012. — Vol. 2. — P. 337-414.
51. KDOQI Clinical Practice Guidelines and Clinical Practice Recommendations for Diabetes and Chronic Kidney Disease // Am. J. Kidney Disease. — 2007. — Vol. 49, Suppl. 2. — P. 1S-179S.
52. Kim M.P., Zhou M., Wahl L.M. Angiotensin II increases human monocyte matrix etalloproteinase-1 through the AT2 receptor and prostaglandin E2: implications for atherosclerotic plaque rupture // J. Leukoc. Biol. — 2005. — Vol. 78. — P. 195-201.
53. Kohlstedt K., Kellner R., Busse R., Fleming I. Signaling via the angiotensin-converting enzyme results in the phosphorylation of the nonmuscle myosin heavy chain IIA // Mol. Pharmacol. — 2006. —Vol. 69. — P. 19-26.
54. Kosch M., Levers A., Lang D. et al. A randomized, double-blind study of valsartan versus metoprolol on arterial distensibility and endothelial function in essential hypertension // Nephrol. Dial. Transplant. — 2008. — Vol. 23. — P. 2280-2285.
55. Krikov M., Thone-Reineke C., Mьller S., Villringer A., Unger T. Candesartan but not ramipril pretreatment improves outcome after stroke and stimulates neurotrophin BNDF/TrkB system in rats // Journal of Hypertension. — 2008. — Vol. 26. — P. 544-552.
56. Kunz R., Friedrich C., Wolbers, Mann J.F.E. Meta-analysis: Effect of Monotherapy and Combination Therapy With Inhibitors of the Renin-Angiotensin System on Proteinuria in Renal Disease // Ann. Intern. Med. — 2008. — Vol. 148. — P. 30-48.
57. Lange S., Wolf B., Schober K. et al. Chronic angiotensin II receptor blockade induces cardioprotection during ischemia by increased PKC-epsilon expression in the mouse heart // J. Cardiovasc. Pharmacol. — 2007. — Vol. 49. — P. 46-55.
58. Lasserson D., Buclin T., Glasziou P. How quickly should we titrate antihypertensive medication? Systematic review modelling blood pressure response from trial data // Heart. — 2011. — Vol. 97(21). — P. 1771-1775.
59. Lйvy B., Benessiano I.J., Henrion D. et al. Chronic blockade of AT2-subtype receptors prevents the effect of angiotensin II on the rat vascular structure // J. Clin. Invest. — 1996. — Vol. 98. — P. 418-425.
60. Lйvy B. Can Angiotensin II Type 2 Receptors Have Deleterious Effects in Cardiovascular Disease? Implications for Therapeutic Blockade of the Renin-Angiotensin System // Circulation. — 2004. — Vol. 109. — P. 8-13.
61. Li J., Culman J., Hortnagi H. et al. Angoitansin AT2 receptor protects against cerebral ischemia-induced neuronal injury // FASEB J. —2005. — Vol. 19. — P. 617-619.
62. Lindholm L.H., Ibsen H., Dahlof B. et al. Cardiovascular morbidity and mortality in patients with diabetes in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol // Lancet. — 2002. — Vol. 359. — P. 1004-1010.
63. Lithell H., Hansson L., Skoog I. et al. The Study on Cognition and Prognosis in the Elderly (SCOPE): principal results of a randomized double-blind intervention trial // J. Hypertens. — 2003. — Vol. 21. — P. 875-886.
64. MacKinnon M., Shurraw S., Akbari A., Knoll G.A., Jaffey J., Clark H.D. Combination therapy with an angiotensin receptor blocker and an ACE inhibitor in proteinuric renal disease: a systematic review of the efficacy and safety data // Am. J. Kidney Dis. — 2006. — Vol. 48. — Р. 8-20.
65. Maggioni A.P., Latini R., Carson P.E. et al. Valsartan reduces the incidence of atrial fibrillation in patients with heart failure: results from the Valsartan Heart Failure Trial (Val-HeFT) // Am. Heart J. — 2005. — Vol. 149. — P. 548-557.
66. Marott S.C., Nielsen S.F., Benn M., Nordestgaard B.G. Antihypertensive treatment and risk of atrial fibrillation: a nationwide study // Eur. Heart J. — 2014. — DOI: 10.1093/eurheartj/eht507. Abstrac.
67. McMurray J., Solomon S., Pieper K. et al. The effect of valsartan, captopril, or both on atherosclerotic events after acute myocardial infarction: an analysis of the Valsartan in Acute Myocardial Infarction Trial (VALIANT) // J. Am. Coll. Cardiol. — 2006. — Vol. 47. — P. 726 -733.
68. McMurray J.J., Ostergren J., Swedberg K. et al. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function taking angiotensin-converting-enzyme inhibitors: the CHARM-Added trial // Lancet. — 2003. — Vol. 362. — P. 767-771.
69. Mehta J.L., Li D.Y., Yang H., Raizada M.K. Angiotensin II and IV stimulate expression and release of plasminogen activator inhibitor-1 in cultured human coronary artery endothelial cells // J. Cardiovasc. Pharmacol. — 2002. — Vol. 39. — P. 789-794.
70. Messerli F. Antihypertensive Efficacy of Hydrochlorothiazide as Evaluated by Ambulatory Blood Pressure Monitoring. A meta-analysis of randomized trial // Am. Coll. Cardiol. — 2011. — Vol. 57. — P. 590-600.
71. Miura S., Saku K. Do all angiotensin II type 1 receptor blockers have the same beneficial effects? // Br. J. Pharmacol. — 2007. — Vol. 151(7). — P. 912-913.
72. Mogensen C.E., Neldam S., Tikkanen I. et al. Randomised controlled trial of dual blockade of renin-angiotensin system in patients with hypertension, microalbuminuria, and non-insulin dependent diabetes: the candesartan and lisinopril microalbuminuria (CALM) study // Br. Med. J. — 2000. — Vol. 321. — P. 1440-1444.
73. Mцller J., Dahlstrцm U., Gцtzsche O. et al. Effects of losartan and captopril on left ventricular systolic and diastolic function after acute myocardial infarction: results of the Optimal Trial in Myocardial Infarction with Angiotensin II Antagonist Losartan (OPTIMAAL) echocardiographic substudy // Am. Heart J. — 2004. — Vol. 147. — P. 494-501.
74. Mцrtsell D., Malmqvist K., Held C., Kahan T. Irbesartan reduces common carotid artery intima-media thickness in hypertensive patients when compared with atenolol: the Swedish Irbesartan Left Ventricular Hypertrophy Investigation versus Atenolol (SILVHIA) study // J. Intern. Med. — 2007. — Vol. 261. — P. 472-479.
75. Nakamura T., Inoue T., Suzuki T. et al. Comparison of renal and vascular protective effects between telmisartan and amlodipine in hypertensive patients with chronic kidney disease with mild renal insufficiency // Hypertens. Res. — 2008. — Vol. 31. — P. 841-850.
76. Nakao N., Yoshimura A., Morita H., Takada M., Kayano T., Ideura T. Combination treatment of angiotensin-II receptor blocker and angiotensin-converting-enzyme inhibitor in non-diabetic renal disease (COOPERATE): a randomised controlled trial // Lancet. — 2003. — Vol. 361. — P. 117-124.
77. Okaka T., Yamamoto H., Okimoto T. et al. Beneficial Effects of Valsartan on Target Lesion Revascularization After Percutaneous Coronary Interventions With Bare Metal Stent // Circulation Journal. — 2011. — Vol. 75. — P. 1641-1648.
78. Okura T., Watanabe S., Kurata M. et al. Long-term effects of angiotensin II receptor blockade with valsartan on carotid arterial stiffness and hemodynamic alterations in patients with essential hypertension // Clin. Exp. Hypertens. — 2008. — Vol. 30. — P. 415-422.
79. Olsen M.H., Wachtell K., Neland K. et al. Losartan but not atenolol reduce carotid artery hypertrophy in essential hypertension. A LIFE substudy // Blood Press. — 2005. — 14. — Р. 177-183.
80. Ong K., Delerme S., Pannier B. et al. Aortic stiffness is reduced beyond blood pressure lowering by short-term and long-term antihypertensive treatment: a meta-analysis of individual data in 294 patients // J. Hypertens. — 2011. — Vol. 29. — P. 1034-1132.
81. Ono H., Minatoguchi S., Watanabe K. et al. Candesartan decreases carotid intima-media thickness by enhancing nitric oxide and decreasing oxidative stress in patients with hypertension // Hypertens. Res. — 2008. — Vol. 31. — Р. 271-279.
82. Otsuka S., Sugano M., Makino N. et al. Interaction of mRNAs for angiotensin II type 1 and type 2 receptors to vascular remode-ling in spontaneously hypertensive rats // Hypertension. — 1998. — Vol. 32. — P. 467-472.
83. Park D., Yangsoo Jang, Ki-Bae Seung et al. Effect of valsartan on suppression of neointimal hyperplasia after drug-eluting stents and on regression of native plaque volume: the VAL-SUPPRESS randomized controlled trail // JACC. — 2011. — Vol. 57. — E. 1909.
84. Park M., Chi-yuan Hsu. An ACE in the Hole for Patients With Advanced Chronic Kidney Disease? // JAMA Intern. Med. — 2014. — Vol. 174(3). — P. 355-356.
85. Parving H., Lehnert H., Brochner-Mortensen J. et al. The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes // N. Engl. J. Med. — 2001. — Vol. 345. — P. 870-878.
86. Peters S., Gotting B., Trummel M. et al. Valsartan for prevention of restenosis after stenting of type B2/C lesions: the VAL-PREST trial // J. Invasive Cardiol. — 2001. — Vol. 13. — Р. 93-97.
87. Peters S., Trummel M., Meyners W. et al. Valsartan versus ACE inhibition after bare metal stent implantation—results of the VALVACE trial // Int. J. Cardiol. — 2005. — Vol. 98. — Р. 331-335
88. Pfeffer M.A., McMurray J.J., Velazquez E.J. et al. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both // N. Engl. J. Med. — 2003. — Vol. 349. — P. 1893-1906.
89. Pfeffer M.A., Swedberg K., Granger C.B. еt al. Effects of candesartan on mortality and morbidity in patients with chronic heart failure: the CHARM-Overall programme // Lancet. — 2003. — Vol. 362. — P. 759-766.
90. Pitt B., Poole-Wilson P.A., Segal R. et al. Effect of losartan compared with captopril on mortality in patients with symptomatic heart failure: randomised trial: the Losartan Heart Failure Survival Study ELITE II // Lancet. — 2000. — Vol. 355. — P. 1582-1587.
91. Pitt B., Segal R., Martinez F.A. et al. Randomised trial of losartan versus captopril in patients over 65 with heart failure (Evaluation of Losartan in the Elderly Study, ELITE) // Lancet. — 1997. — Vol. 349. — P. 747-752.
92. Rayner B. Comments. Telmisartan shown to reduce cardiovascular death, myocardial infarction and stroke in ACE-intolerant high-risk patients // Cardiovascular Journal of South Africa. — 2008, advance publication 10 September. — P. 1.
93. Robles N., Romero B., Fernandez-Carbonero E. Angiotensin-converting enzyme inhibitors versus angiotensin receptor blockers for diabetic nephropathy: a retrospective comparison // Journal of Renin-Angiotensin-Aldosterone System. — 2009. — Vol. 10. — P. 195.
94. Schrader J., Luders S., Kulschewski A. et al. Morbidity and Mortality After Stroke, Eprosartan Compared with Nitrendipine for Secondary Prevention: principal results of a prospective randomized controlled study (MOSES) // Stroke. — 2005. — Vol. 36. — P. 1218-1226.
95. Senbonmatsu T., Ichihara S., Price E. Jr, Gaffney F.A., Inagami T. Evidence for angiotensin II type 2 receptor-mediated cardiac myocyte enlargement during in vivo pressure overload // J. Clin. Invest. — 2000. — Vol.106. — P. R25-R29.
96. Sipahi I., Debanne S.M., Rowland D.Y., Simon D.I., Fang J.C. Angiotensin-receptor blockade and risk of cancer: meta-analysis of randomised controlled trials // Lancet Oncol. — 2010. — Vol. 11(7). — P. 627-636.
97. Smolensky M., Hermida R.C., Ayala D.E. et al. Administration-time-dependent effects of blood pressure-lowering medications: basis for the chronotherapy of hypertension // Blood Press Monit. — 2010. — Vol. 15. — P. 173-180.
98. Strauss M., Lonn E., Verma S. Is the jury out? Class specific differences on coronary outcomes with ACE-inhibitors and ARBs: insight from meta-analysis and The Blood Pressure Lowering Treatment Trialists’ Collaboration // European Heart Journal. — 2005. — Vol. 26. — P. 2351-2353.
99. Strauss M., Hall A. Angiotensin Receptor Blockers May Increase Risk of Myocardial Infarction: Unraveling the ARB-MI Paradox // Circulation. — 2006. —Vol. 114. — P. 838-854.
100. Strippoli G.F., Craig M., Deeks J.J., Schena F.P., Craig J.C. Effects of angiotensin converting enzyme inhibitors and angiotensin II receptor antagonists on mortality and renal outcomes in diabetic nephropathy: systematic review // BMJ. — 2004. — Vol. 9, 329. — P. 828.
101. The ACTIVE I Investigators Irbesartan in Patients with Atrial Fibrillation // N. Engl. J. Med. — 2011. — Vol. 364. — P. 928-938.
102. The Investigators. Valsartan for Prevention of Recurrent Atrial Fibrillation // N. Engl. J. Med. — 2009. — Vol. 360. — P. 1606-1617.
103. The ONTARGET Investigators. Telmisartan, Ramipril, or Both in Patients at High Risk for Vascular Events // New Engl. J. Med. — 2008. — Vol. 358. — P. 1547-59.
104. The Task force members. Guidelines in diabetes, prediabetes and cardiovascular disease: full text // Eur. Heart J. — doi:10.1093/eurheartj/ehl261
105. Thone-Reineke C., Steckelings U.M., Unger T. Angiotensin receptor blockers and cerebral protection in stroke // J. Hypertens. — 2006. — Vol. 24. — P. 115S-121S.
106. Unger T. Pharmacological properties of angiotensin II antagonists: examining all the therapeutic implications // J. Renin Angiotensin Aldosterone Syst. — 2001. — Vol. 2. — P. S4-7.
107. Unger T., Stoppelhaar M. Rationale for double renine-angiotensin-aldosterone system blockade // Am. J. Cardiol. — 2007. — Vol. 100. — P. 25-31.
108. Vacanti L. Could angiotensin receptor blockers and activation of At2 induce plaque rupture, rather than repair? // BMJ. — 2004. — rapid Response (23 Dec. 2004).
109. Van de Wall R., Veldhuisen D., van Gilst W., Voors A. Addition of an angiotensin receptor blocker to full-dose ACE-inhibition: controversial or common sense? // European Heart Journal. — 2005. — Vol. 26. — P. 2361-2367.
110. Viberti G. Microalbuminuria Reduction With Valsartan in Patients With Type 2 Diabetes Mellitus: A Blood Pressure — Independent Effect. Wheeldon and for the Microalbuminuria Reduction With VALsartan (MARVAL) Study Investigators // Circulation. — 2002. — Vol. 106. — P. 672-678.
111. Wachtell K., Lehto M., Gerdts E. et al. Angiotensin II receptor blockade reduces new-onset atrial fibrillation and subsequent stroke compared to atenolol. The Losartan Intervention For End point reduction in hypertension (LIFE) study // J. Am. Coll. Cardiol. — 2005. — Vol. 45(5). — P. 712-719.
112. Warnecke C., Mugrauer P., Surder D. et al. Intronic ANG II type 2 receptor gene polymorphism 1675 G/A modulates receptor protein expression but not mRNA splicing // Am. J. Physiol. Regul. Integr. Comp. Physiol. — 2005. — Vol. 289. — P. 1729-1735.
113. Weber M.A., Julius S., Kjeldsen S.E. et al. Blood pressure dependent and independent effects of antihypertensive treatment on clinical values in the VALUE trial // Lancet. — 2004. — Vol. 363. — P. 2047-2049.
114. Wolf G. The road not taken: role of angiotensin II type 2 receptor in pathophysiology // Nephrol. Dial. Transplant. — 2002. — Vol. 17. — P. 195-198.
115. www.comitehta.org
116. Yan X., Price R.L., Nakayama M. et al. Ventricular-specific expression of angiotensin II type 2 receptors causes dilated cardiomyopathy and heart failure in transgenic mice // Am. J. Physiol. Heart Circ. Physiol. — 2003. — Vol. 285. — P. 2179-2187.
117. Yang X., Liu Y., Mehta D. et al. Diminished cardioprotective response to inhibition of angiotensin-converting enzyme and angiotensin II type 1 receptor in B(2) kinin receptor gene knockout mice // Circ. Res. — 2001. — Vol. 88. — P. 1072-1079.
118. Zannad F., Matzinger A., Larche J. Trough/peak ratios of once daily angiotensin converting enzyme inhibitors and calcium antagonists // Am. J. Hypertens. — 1996. — Vol. 9(7). — P. 633-643.