Газета «Новости медицины и фармации» Антимикробная терапия (223) 2007 (тематический номер)
Вернуться к номеру
Нозокомиальная пневмония
Авторы: Р.С. КОЗЛОВ, проф., д.м.н., директор НИИ антимикробной химиотерапии ГОУ ВПО Смоленская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию, г. Смоленск
Рубрики: Пульмонология
Разделы: Справочник специалиста
Версия для печати
Введение
Нозокомиальная пневмония (НП) остается важнейшей проблемой современных многопрофильных стационаров. НП является 2-й по частоте среди всех нозокомиальных инфекций (13–18 %), а в отделениях реанимации и интенсивной терапии (ОРИТ) — самой частой нозокомиальной инфекцией (> 45 %).
Согласно большинству исследований, частота НП составляет 0,5–1 % от общего числа госпитализированных пациентов и 15–25 % от находящихся в ОРИТ. Особая категория НП у пациентов, находящихся на ИВЛ, — так называемая вентиляторассоциированная пневмония (ВАП) — развивается у 9–27 % от общего числа пациентов с интубацией трахеи.
Актуальность проблемы НП, помимо высокой частоты ее встречаемости, заключается в том, что она характеризуется высокой летальностью, которая может достигать 30–70 %. Однако столь высокие показатели могут быть обусловлены наличием у большого числа пациентов с НП тяжелых сопутствующих заболеваний, при этом определить так называемую атрибутивную летальность, т.е. непосредственно связанную с НП, бывает очень сложно. Тем не менее, согласно имеющимся данным, она среди пациентов с НП составляет от 10 до 50 %.
Принципиально важным является то, что адекватная начальная антибактериальная терапия (АБТ) позволяет как минимум в 2–2,5 раза снизить количество летальных исходов при НП. В свою очередь, неадекватное эмпирическое назначение антимикробных препаратов является достоверно установленным независимым фактором риска развития летального исхода.
Ведение пациентов с НП сопровождается большими экономическими затратами, поэтому своевременная адекватная АБТ приводит не только к снижению летальности, но и к повышению экономической эффективности лечения.
Учитывая актуальность проблемы НП, а также наблюдающийся рост устойчивости основных возбудителей НП, в марте 2005 г. под эгидой Минздравсоцразвития России, Российского респираторного общества, Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), Федерации анестезиологов и реаниматологов России группой экспертов под редакцией академика РАМН А.Г. Чучалина были разработаны национальные рекомендации «Нозокомиальная пневмония: практические рекомендации по диагностике, лечению, профилактике». Они были составлены с соблюдением принципов доказательной медицины и учетом российских особенностей резистентности возбудителей НП.
Данная публикация подготовлена на основе вышеупомянутых рекомендаций.
Определение и классификация
Согласно принятому определению, нозокомиальная (госпитальная, внутрибольничная) пневмония — это заболевание, характеризующееся появлением на рентгенограмме «свежих» очагово-инфильтративных изменений в легких спустя 48 ч и более после госпитализации в сочетании с клиническими данными, подтверждающими их инфекционную природу (новая волна лихорадки, гнойная мокрота или гнойное отделяемое трахеобронхиального дерева, лейкоцитоз и т.д.), при исключении инфекций, которые находились в инкубационном периоде на момент поступления больного в стационар.
В настоящее время наибольшей известностью пользуется классификация, в основе которой лежат сроки развития НП и наличие или отсутствие факторов риска, повышающих вероятность того, что НП вызвана полирезистентными (т.е. устойчивыми к 3 и более классам антибиотиков) возбудителями (ПРВ).
В соответствии с этой классификацией выделяют:
— раннюю НП, возникающую в течение первых 5 дней с момента госпитализации, для которой характерны возбудители, как правило, чувствительные к традиционно используемым антибиотикам, и имеющую более благоприятный прогноз;
— позднюю НП, развивающуюся не ранее 6-го дня госпитализации, которая характеризуется более высоким риском наличия ПРВ и менее благоприятным прогнозом.
Патогенез и факторы риска развития НП
Патогенез НП является многофакторным, причем эти факторы тесно взаимодействуют между собой. Как и в случаях любой пневмонии, обязательным условием развития НП является преодоление микроорганизмами защитных механизмов нижних отделов дыхательных путей.
Основным путем проникновения инфекции в нижние дыхательные пути является аспирация содержимого ротоглотки и содержащихся в ней микроорганизмов, являющихся потенциальными возбудителями НП. Аспирация секрета ротоглотки может наблюдаться у здоровых лиц, особенно во время сна. Однако частота ее су щественно возрастает при нарушении созна ния, расстройствах глотания, угнетении рвотного рефлекса, замедлении опорожнения желудка, угнетении двигательной активности ЖКТ.
Другими, менее значимыми в патогенезе НП путями попадания возбудителей являются аспирация нестерильного содер жимого пищевода или желудка, ингаляция микробного аэрозоля и гематогенное распространение из отдаленного очага инфекции. Клиницистам следует помнить, что колонизация в норме стерильного желудка микроорганизмами может наблюдаться в следующих ситуациях: ахлоргидрия/ги похлоргидрия, недостаточное питание/ голодание, энтеральное питание, прием лекарственных средств, повышающих рН желудочного содержимого (антациды, Н2-блокаторы, ингибиторы протонной помпы).
Наиболее распространенные факторы риска развития НП
1. Со стороны пациента:
— пожилой и старческий возраст (≥ 60 лет);
— курение;
— заболевания органов дыхания: хроническая обструктивная болезнь легких (ХОБЛ), дыхательная недостаточность, острый респираторный дистресс-синдром (ОРДС), грипп;
— сердечная недостаточность, сахарный диабет, почечная недостаточность, алкоголизм;
— недостаточное питание;
— кома;
— травмы головы, другие нейрохирургические состояния, политравма;
— ожоги;
— метаболический ацидоз;
— любой очаг инфекции в организме, являющийся потенциальным источником гематогенного распространения;
— плохая гигиена полости рта.
2. Связанные с медицинскими манипуляциями:
— длительная госпитализация;
— горизонтальное положение пациента на спине;
— интубация трахеи, повторные интубации, трахеостомия;
— искусственная вентиляция легких;
— медикаментозная терапия (седативные лекарственные средства, миорелаксанты, антациды, Н2-блокаторы, глюкокортикоиды, цитостатики и другая иммуносупрессивная терапия);
— длительные и сложные оперативные вмешательства (особенно на органах грудной клетки и брюшной полости);
— фибробронхоскопия;
— наличие желудочного зонда;
— энтеральное питание;
— использование венозных катетеров;
— перекрестное инфицирование.
Одним из наиболее значимых факторов риска развития НП является искусственная вентиляция легких. Доказано, что риск развития НП у пациентов, находящихся на ИВЛ, возрастает в 6–21 раз и что существует связь между частотой НП и длительностью механической вентиляции.
Клиническая и инструментальная диагностика
Несмотря на известные ограничения, клиническое обследование остается отправной точкой в диагностике НП. Ценность же дополнительных инструментальных методов исследования во многом определяется их способностью снижать частоту ложноположительных клинических диагнозов НП.
К формализованным диагностическим критериям НП следует отнести:
1. Появление на рентгенограмме «свежих» очагово-инфильтративных изменений в легких.
2. Два из приведенных ниже симптомов:
— лихорадка > 39,3 ºС;
— бронхиальная гиперсекреция;
— РаО2/FiО2 ≤ 240 мм рт.ст.
3. Два из приведенных ниже признаков:
— кашель, тахипноэ, локально выслушиваемая крепитация, влажные хрипы, бронхиальное дыхание;
— лейкопения (< 4,0 ´ 109/л) или лейкоцитоз (> 12,0 ´ 109/л), сдвиг лейкоцитарной формулы влево (> 10 %);
— гнойная мокрота/бронхиальный секрет (> 25 полиморфноядерных лейкоцитов в поле зрения при микроскопии с увеличением в 100 раз).
Однако в реальной практике указанные клинические, лабораторные и рентгенологические критерии диагностики НП оказываются не вполне надежными, особенно у пациентов, находящихся на ИВЛ. Сходную картину могут давать тромбоэмболия ветвей легочной артерии с развитием инфаркта легкого, ателектазы, лекарственные реакции, легочные кровотечения, ОРДС, а также некоторые сопутствующие сердечно-сосудистые и бронхолегочные заболевания.
Для оценки вероятности наличия у пациента НП также может использоваться шкала клинической оценки инфекции легких (CPIS), представленная в табл. 1. Общая сумма баллов ≥ 7 с высокой долей вероятности указывает на то, что определяемая у пациента клиническая симптоматика обусловлена инфекционным процессом в легких, а при показателе ≤ 6 диагноз НП является сомнительным. Шкала CPIS также может применяться для контроля динамики состояния пациента в процессе лечения и для принятия решения о необходимости изменения или возможности прекращения АБТ.
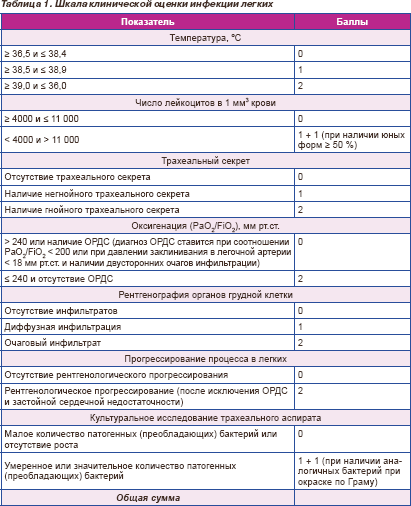
Всем пациентам должна быть выполнена рентгенография органов грудной клетки в передне-задней и боковой проекциях. Рентгенография дает возможность не только установить сам факт наличия очаговой инфильтрации легочной ткани (с определением ее локализации), но и оценить степень тяжести НП (мультилобарная инфильтрация, быстрое прогрессирование пневмонической инфильтрации, деструкция), а также выявить такое осложнение НП, как плеврит.
У всех пациентов должно быть проведено исследование газового состава артериальной крови или пульсоксиметрия.
Микробиологическая диагностика
Важнейшим этапом является установление этиологического диагноза НП.
Микробиологическое исследование крови является обязательным при обследовании пациента с подозрением на НП. До начала АБТ следует взять 2 образца венозной крови из 2 разных вен (предпочтительно в специальные флаконы для крови). При этом следует строго соблюдать правила асептики и обрабатывать место забора 70% этиловым спиртом, затем 1–2% раствором йода. У взрослых пациентов необходимо брать не менее 20 мл крови на каждый образец, что приводит к сущест венному повышению вероятности получения положительного результата. К сожалению, чувствительность этого метода < 25 %, а специфичность ограничивается тем, что у госпитализированных пациентов (особенно тяжелобольных) могут иметь место несколько источников бактериемии. Соответственно микроорганизмы, выделенные из крови, могут рассматриваться как возбудители НП лишь в тех случаях, если они обнаружены и при исследовании образцов из нижних дыхательных путей.
Несмотря на то, что исследование свободно откашливаемой мокроты (микроскопия окрашенных по Граму мазков, посев) у пациентов, не находящихся на ИВЛ, обладает низкой специфичностью (< 30 %), этот вид материала является основным в микробиологических лабораториях. Обязательной является оценка пригодности образца мокроты до проведения культурального исследования (> 25 нейтрофилов и < 10 эпителиальных клеток в поле зрения при микроскопии окрашенного по Граму мазка с увеличением в 100 раз).
Исследование трахеобронхиального сек рета (трахеального аспирата) является малоинформативным в связи с высоким риском контаминации материала.
У интубированных пациентов с подозрением на НП наиболее доступным способом получения материала для микробиологического исследования является эндотрахеальная аспирация (ЭТА). Основное значение микробиологического исследования эндотрахеального аспирата состоит в том, что отрицательный результат исследования позволяет исключить роль определенных видов возбудителей НП.
Современные инвазивные методы забора материала для количественного культурального исследования, такие как бронхоальвеолярный лаваж (БАЛ) и биопсия с помощью защищенных щеток (ЗЩ), которая предотвращает контаминацию микрофлорой верхних дыхательных путей, сравнимы по чувствительности и специфичности, однако ни один из них не может считаться золотым стандартом. Следует также отметить, что исследование с помощью защищенных щеток недоступно в России.
Диагностический торакоцентез показан только при наличии плеврального выпота c толщиной слоя свободно смещаемой жидкости на латерограмме > 10 мм или при тяжелом состоянии пациента прежде всего для дифференциальной диагностики эмпиемы плевры и парапневмонического выпота. Исследование плевральной жидкости должно включать определение содержания белка, глюкозы, уровня лактатдегидрогеназы, рН, изучение клеточного состава, окраску по Граму, окраску на кислотоустойчивость, микроскопию мазков с последующим культуральным исследованием.
Серологические исследования имеют ограниченную диагностическую ценность, не используются при обследовании пациентов с подозрением на НП и носят только эпидемиологическое значение, например при легионеллезной этиологии пневмонии.
Этиология НП
На этиологию НП оказывают влияние многочисленные факторы, связанные с состоянием пациента, основной патологией, сроком развития НП, профилем отделения, объемом и видом проводимой терапии и длительностью пребывания в стационаре.
При ранней НП у пациентов без предшествующей АБТ и факторов риска наличия ПРВ основными возбудителями являются S.pneumoniae, H.influenzae и грамотрицательные энтеробактерии.
Преобладающими возбудителями поздней НП, а также ВАП являются полирезистентные грамотрицательные микроорганизмы, такие как P.aeruginosa, E.coli, K.pneumoniae, Acinetobacter spp., а также грамположительные бактерии, включая метициллинорезистентные S.aureus (MRSA).
Более того, ПРВ могут играть этиологическую роль и при ранней НП. Факторами риска наличия ПРВ у этой категории пациентов являются:
— АБТ в предшествующие 90 дней (до госпитализации);
— высокая распространенность резистентности у основных возбудителей во внебольничных условиях или в конкретных отделениях стационаров;
— госпитализация в течение ≥ 2 дней за предшествующие 90 дней;
— пребывание в домах длительного ухода;
— проведение инфузионной терапии на дому;
— хронический диализ в течение предшествующих 30 дней;
— наличие члена семьи с заболеванием, вызванным ПРВ;
— наличие иммунодефицитного состояния, проводимая иммуносупрессивная терапия.
Анаэробы, легионеллы, вирусы и грибы являются редкими возбудителями НП. Следует подчеркнуть, что выделение некоторых микроорганизмов из мокроты или трахеобронхиального секрета (трахеального аспирата) скорее свидетельствует о контаминации материала, чем об их этиологической значимости. К микроорганизмам, которые не играют этиологической роли при НП у пациентов без иммунодефицитных состояний, относятся Streptococcus viridans, Enterococcus spp., коагулазонегативные стафилококки, Neisseria spp. и грибы.
Чувствительность к антибиотикам основных возбудителей НП
При выборе антибиотиков для эмпирической АБТ НП клиницисты должны ориентироваться на локальные данные по резистентности возбудителей в тех отделениях лечебного учреждения, где находятся пациенты с НП.
Важным является периодическое обновление этих данных, так как резистентность к антимикробным препаратам может изменяться со временем в зависимости от структуры и частоты их использования.
Для адекватного выбора антибиотиков важно знать о распространенности бета-лактамаз расширенного спектра (БЛРС). Несмотря на то, что практически все микроорганизмы семейства Enterobacteriaceae обладают способностью к выработке БЛРС, наиболее часто они встречается у E.coli и K.pneumoniae, являющихся основными возбудителями НП.
Согласно данным многоцентровых исследований, проводимых научно-методическим центром Федерального агентства по здравоохранению и социальному развитию по мониторингу антибиотикорезистентности и НИИ антимикробной химиотерапии ГОУ ВПО СГМА Росздрава, P.aeruginosa, являющаяся одним из основных возбудителей НП, характеризуется высокой резистентностью к антисинегнойным пенициллинам (пиперациллину, пиперациллину / тазобактаму), ципрофлоксацину. Наиболее активными in vitro в отношении синегнойной палочки являются цефепим, цефтазидим и карбапенемы (имипенем и меропенем), хотя и к этим препаратам отмечается наличие резистентности.
Необходимо отметить, что использование данных многоцентровых исследований резистентности основных возбудителей НП, учитывая значительные вариации в профилях резистентности не только в регионе, но и в пределах города и даже отдельного стационара, представляется не совсем целесообразным. Однако для России представленные выше данные являются наиболее адекватными, поскольку для того, чтобы ориентироваться на локальные данные, предоставляемые микробиологическими лабораториями стационаров, необходимо, чтобы исследования в них проводились с соблюдением правил качественной лабораторной практики (GLP), общепринятых стандартов и проведением контроля качества, что встречается пока еще достаточно редко.
Общие подходы к ведению пациентов с НП
Во всех случаях, когда имеется подозрение на НП, проводятся тщательный сбор анамнеза для выявления факторов риска развития НП, факторов риска наличия ПРВ и физикальное обследование.
На основании данных анамнеза, физикального обследования и других методов исследования можно оценить тяжесть течения заболевания для определения места лечения пациента (ОРИТ или соматическое отделение).
Критериями тяжелого течения НП являются:
— потребность в ИВЛ;
— многодолевое поражение или деструкция легочной ткани на рентгенограмме или быстрая отрицательная динамика;
— признаки тяжелого сепсиса или шока, потребность в вазопрессорах > 4 ч;
— АД сист. < 90 мм рт.ст. и/или АД диаст. < 60 мм рт.ст.;
— признаки острой почечной недо-статочности (диурез менее 20 мл/ч и/или креатинин крови > 177 мкмоль/л, и/или потребность в гемодиализе);
— ОРДС;
— выраженная гипоксемия (PaO2 < 60 мм рт.ст., SaO2 < 90 % или PaO2/FiO2 ≤ 240 мм рт.ст.);
— нарушение сознания.
Для оценки тяжести пневмонии и прогноза также можно использовать шкалы CPIS или APACHE II. Если НП расценена как тяжелая, то лечение пациентов целесообразно проводить в ОРИТ.
При уточнении нозологического диагноза НП следует немедленно начать эмпирическую АБТ, так как задержка назначения адекватного лечения сопровождается достоверным ухудшением прогноза и повышением летальности. До первого введения антибиотика необходимо взять материал для микробиологического исследования.
Диагностические мероприятия в процессе лечения НП будут определяться исходной степенью тяжести, динамикой состояния пациента в процессе лечения, наличием сопутствующей патологии.
Общий анализ крови выполняется регулярно с интервалом 2–4 дня; биохими ческий анализ крови при тяжелом течении НП — с интервалом 2–3 дня или по мере необходимости, при нетяжелом течении — через 5–7 дней при наличии изменений в первом анализе. Такие важные для оценки динамики НП показатели, как исследование газового состава артериальной крови или пульсоксиметрия, при тяжелой НП следует проводить ежедневно.
Повторное проведение микробиологического исследования мокроты у пациентов, не находящихся в ОРИТ, нецелесообразно; в случае неэффективности АБТ для уточнения этиологического диагноза показано использование более чувствительного способа получения материала — ЭТА или БАЛ.
Повторная рентгенография органов грудной клетки показана в случае ухудшения состояния или неэффективности АБТ по решению лечащего врача. В том случае, если лечение оказалось эффективным, контрольное рентгенологическое исследование проводится через 2–3 недели.
Антибактериальная терапия НП
На сегодняшний день является несомненным, что ключевым моментом, во многом определяющим исход лечения пациентов с НП, является незамедлительное назначение эффективной эмпирической АБТ. Результаты многочисленных исследований достоверно свидетельствуют, что при неадекватном выборе стартового режима АБТ его изменения в процессе лечения уже не могут благоприятно повлиять на показатели летальности при НП.
Выбор эмпирической терапии основан на существующих данных о наиболее вероятных возбудителях инфекции, спектр которых определяется с роком развития НП и наличием факторов риска ПРВ. Вторым моментом, который определяет выбор эмпирической АБТ, являются локальные данные по структуре антибиотикорезистентности наиболее часто встречающихся возбудителей НП.
Наиболее обоснованным представляется следующий подход к назначению АБТ (монотерапия или комбинация препаратов) в зависимости от сроков развития НП. При ранней НП, развившейся у пациентов без факторов риска, рекомендуется проведение монотерапии. При поздней НП или НП, развившейся у пациентов с факторами риска, более оправданным, по крайней мере, до идентификации возбудителя и определения его чувствительности, является использование комбинации антибиотиков.
Предлагаемые схемы эмпирической АБТ представлены в табл. 2 и 3.


В начале лечения большинство пациентов с НП должны получать антибиотики внутривенно. В дальнейшем у пациентов с клинической эффективностью терапии и без нарушения функции ЖКТ возмож но пероральное назначение препаратов, обладающих хорошей биодоступностью, — так называемая ступенчатая терапия.
Традиционно рекомендуемая длительность терапии НП составляла 14–21 день. Однако в настоящее время имеются доказательные данные, свидетельствующие о том, что при эффективной эмпирической АБТ, т.е. при положительной клинической динамике, ее длительность может быть сокращена до 7–8 дней.
Оценка эффективности АБТ и ее коррекция
Клиническая оценка эффективности базируется на динамике таких показателей, как лихорадка, количество и характер мокроты, лейкоцитоз или лейкопения, оксигенация крови, рентгенологическая картина, данные оценки состояния других органов и систем. Клиническое улучшение обычно отмечается через 48–72 ч после начала терапии, поэтому стартовую терапию НП в течение этого периода времени в большинстве случаев менять не следует. Исключение составляют случаи прогрессирующего ухудшения состояния или получение результатов микробиологического исследования, требующих изменения АБТ.
Рентгенография органов грудной клетки имеет ограниченную ценность при оценке динамики тяжелой НП, так как при этом часто отмечается первоначальное рентгенологическое ухудшение, особенно у пациентов с бактериемией или инфекцией, вызванной высоковирулентными микроорганизмами. Кроме того, у пожилых пациентов и лиц с сопутствующими заболеваниями (например, ХОБЛ) рентгенологическое разрешение значительно отстает от клинического улучшения. Рентгенологическими признаками ухудшения являются: поражение новых долей легкого, увеличение размера инфильтрата более чем на 50 % в течение 48 ч, появление очагов деструкции, наличие большого плеврального выпота.
Существенную помощь в клинической оценке динамики состояния пациента с НП может оказать использование шкалы CPIS.
При клинической неэффективности лечения НП или после получения результатов микробиологического исследования может потребоваться коррекция эмпирической АБТ. Однако микробиологические критерии, указывающие на необходимость изменения терапии, четко не определены. В связи с этим основным критерием для решения вопроса о необходимости / возможности изменения или прекращения АБТ является отсутствие / наличие клинического улучшения состояния пациента.
Коррекция терапии в виде перехода на антибиотики более узкого спектра может проводиться, если не выделены возбудители, против которых была направлена эмпирическая терапия (например, P.aeruginosa, Acinetobacter spp.), или в том случае, если выделенный возбудитель чувствителен к препаратам с более узким спектром активности (например, выделена E.coli, чувствительная к амоксициллину / клавуланату при эмпирическом назначении карбапенема).
Подобная тактика получила название деэскалации терапии. Основными проблемами в данном случае являются скорость получения результатов бактериологического исследования и оценка этиологической роли микроорганизмов, выделенных из нестерильных локусов, а также сложности с достоверным определением чувствительности.
Другим вариантом деэскалации терапии является назначение пациентам с поздней НП, с факторами риска наличия ПРВ и с ВАП стартовой АБТ, включающей 3 антибиотика, перекрывающих широкий спектр наиболее вероятных возбудителей, с последующей отменой отдельных препаратов на основании микробиологических данных.
Профилактика НП
Учитывая факторы риска и патогенез НП, профилактика должна включать в себя комплекс взаимосвязанных мероприятий организационно-технического и медицинского характера, снижающих вероятность контаминации и инфицирования, усиливающих противоинфекционную защиту пациентов, а также предотвращающих распространение полирезистентных штаммов. При этом относительно простые подходы и манипуляции способны существенно уменьшить риск развития НП.
1. Общие рекомендации:
— строгое выполнение мероприятий по инфекционному контролю, обучение персонала и соблюдение правил дезинфекции рук с использованием спиртосодержащих антисептиков для уменьшения риска перекрестного инфицирования;
— эпидемиологический надзор за инфекциями в ОРИТ для выявления и оценки распространенности ПРВ, а также своевременное и регулярное информирование клиницистов о полученных данных;
— обеспечение адекватного количества персонала в ОРИТ для повышения качества инфекционного контроля;
— приподнятое положение (30–45о) головного конца кровати пациента, особенно при проведении энтерального питания;
— предпочтительное использование энтерального питания, которое позволяет уменьшить риск развития осложнений, связанных с центральным венозным катетером, и предупредить атрофию слизистой оболочки кишечника, которая может повышать риск инфекции;
— тщательное наблюдение, ограниченное использование и своевременное удаление всех инвазивных устройств;
— эффективная программа контроля применения антибиотиков, основанная на локальных микробиологических и эпидемиологических данных, направленная на снижение риска колонизации и инфекции ПРВ.
2. Рекомендации по проведению интубации и ИВЛ:
— исключение случаев необоснованной интубации;
— неинвазивная вентиляция с положительным давлением с использованием лицевой маски или шлема может с успехом использоваться у некоторых пациентов с ХОБЛ и застойной сердечной недостаточностью;
— предпочтительное использование оротрахеальной интубации;
— давление в манжете интубационной трубки должно быть > 20 см вод.ст.;
— при проведении ИВЛ контролируемый объем не должен превышать 6 мл/кг, что позволяет уменьшить повреждение легких, особенно у пациентов с ОРДС;
— уменьшение длительности интубации и механической вентиляции с использованием протоколов по оптимизации применения седативных средств и быстрому отказу от ИВЛ;
— постоянная аспирация секрета из подсвязочного пространства.
3. Рекомендации по оборудованию для респираторной терапии:
— надлежащая дезинфекция и стерилизация оборудования для проведения респираторной терапии и бронхоскопов для уменьшения перекрестного инфицирования;
— удаление контаминированного конденсата из дыхательного контура;
— использование пассивных увлажнителей для снижения колонизации дыхательного контура. Замена дыхательных контуров не рекомендуется.
4. Применение антибиотиков и других лекарственных препаратов:
— профилактика НП путем проведения селективной деконтаминации кишечника не рекомендуется для рутинного использования и может применяться только у некоторых категорий пациентов (например, с травмой);
— применение хлоргексидина для уменьшения степени колонизации рото- глотки;
— рациональное назначение седативных препаратов, наркотических анальгетиков, миорелаксантов, что сокращает частоту развития НП за счет ограничения процесса транслокации микрофлоры в дыхательные пути;
— при наличии показаний для профилактики стрессовых язв рекомендуется назначение Н2-блокаторов (препараты выбора) или сукральфата.
