Газета «Новости медицины и фармации» Гастроэнтерология (434) 2012 (тематический номер)
Вернуться к номеру
Поражение органов системы пищеварения при саркоидозе
Авторы: Н.Е. Моногарова, д.м.н., доцент
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
В статье представлены эпидемиология, патогенез и клинические симптомы саркоидоза. Особое внимание уделено поражению саркоидозом желудочно-кишечного тракта и особенностям верификации диагноза. Приведены рекомендуемое обследование, порядок наблюдения за больным саркоидозом, а также препараты, применяющиеся в лечении.
Саркоидоз, гранулема, органы пищеварения.
Саркоидоз — хроническое мультисистемное заболевание неизвестной этиологии, характеризующееся скоплением Т-лимфоцитов и мононуклеарных фагоцитов, образованием неказеифицированнных эпителиоидных гранулем и нарушением нормальной архитектоники пораженного органа. Могут поражаться все органы, кроме надпочечников.
Распространенность системного саркоидоза 1–40/100 000, преимущественно наблюдается у афроамериканцев и лиц скандинавского происхождения, поражает в основном молодых людей в возрасте от 20 до 40 лет [1, 2]. Вовлечение желудочно-кишечного тракта (ЖКТ) у пациентов с системным саркоидозом является относительно редким, а в 60–90 % этих случаев гранулемы в печени могут быть найдены только при биопсии [2, 3]. Эксклюзивное участие печени без саркоидоза легких встречается еще реже, задокументировано только около 13 % пациентов с системным саркоидозом [3].
Введение
Саркоидоз является мультисистемным заболеванием, характеризующимся появлением неказеозных гранулем в пораженных органах, в том числе в коже, сердце, тканях нервной системы и суставах. Диагноз «саркоидоз», как правило, основан на наличии гранулемы по крайней мере в двух различных органах, грамнегативном окрашивании культуры микобактерий, отсутствии профессиональных воздействий или домашних токсинов, а также медикаментозного влияния. Поражение полых органов наблюдается редко. Вместо гранулем, характерных для саркоидоза, могут встречаться просто случайные гранулемы. Поражение лимфатических узлов может происходить по всему ходу желудочно-кишечного тракта. Желудок, в частности из всех органов ЖКТ, поражается наиболее часто, а тонкая кишка, наоборот, реже всего. Печень поражается относительно часто — от бессимптомных, случайно выявляемых гранулем при портальной гипертензии до характерных, ярко выраженных — при холестазах, как правило, с относительно сохраненной функцией органа. По сравнению с печенью при саркоидозе саркоидоз поджелудочной железы у пациентов с системным саркоидозом встречается редко и выявляется в основном при аутопсии [4–8]. Тем не менее, несмотря на то, что поджелудочная железа поражается крайне редко [9–23], в доступной литературе можно найти единичные случаи саркоидоза только в поджелудочной железе [24–26], поскольку основным симптомом, связанным с саркоидозом поджелудочной железы, является инфильтрация самой железы или ее протоков и, как результат, обструкция. Клиническая картина саркоидоза поджелудочной железы имеет общие симптомы и напоминает такие заболевания, как панкреатит или рак поджелудочной железы [27]. При компьютерной томографии (КТ) выявляется гепатоспленомегалия с лимфаденопатией — эти симптомы затухают при правильно проводимом лечении. Асцит, как правило, развивается из-за правожелудочковой сердечной недостаточности (из-за легочной гипертензии) или портальной гипертензии (билиарный цирроз). Редко экссудат при асците может появиться при поражении брюшины. Поджелудочная железа поражается редко, как правило, ее головка — выявляется узловое или диффузное поражение органа.
Патология и патогенез
При саркоидозе гистологически выявляют неказеозные гранулемы, хронический внутрипеченочный холестаз, прогрессивное уменьшение числа междольковых желчных протоков, перипортальный фиброз и в конечном итоге цирроз печени [29]. Биопсия печени показывает гранулематозный гепатит и фиброз. Часто обнаруживаются множественные неказеозные гранулемы, окруженные умеренными лимфоцитарными инфильтратами. В паренхиме печени наблюдается фиброз с узловым повреждением, предполагающим ранний цирроз. В гранулемах могут быть небольшие участки некроза. Гранулемы могут самостоятельно полностью разрешиться без остаточных повреждений, или в результате фиброза развивается бесклеточный шрам. Гранулемы могут быть разного возраста, так что более поздние поражения прилегают к рубцам, оставшимся после предыдущих поражений. Печеночные гранулемы чаще обнаруживаются у пациентов с саркоидозными изменениями паренхимы легких, чем у пациентов только с двусторонним грудным лимфаденитом.
Саркоидоз вызывает прогрессирующее заболевание печени с широким спектром гистологических особенностей, которые могут имитировать другие первичные заболевания печени [29]. Обнаруженные гистологические изменения классифицированы как холестатические, некрозно-воспалительные и сосудистые. Холестаз может быть внутрипеченочный или внепеченочный. У некоторых пациентов с внутрипеченочным холестазом поражения желчных протоков напоминают первичный билиарный цирроз печени [28], в то время как у других имеют структуру первичного склерозирующего холангита с перидуктальным фиброзом [30, 31]. У некоторых больных выявляется склероз общего желчного протока или сдавление печеночной вены вследствие лимфаденопатии [32, 33].
У небольшой части пациентов развивается портальная гипертензия, что связано с обструкцией воротной вены и развитием подпеченочной (пресинусоидальной) портальной гипертензии. У них могут развиваться артериовенозные шунты, что ведет к увеличению портального кровотока [34]. У всех пациентов с портальной гипертензией значительно выражены гепатомегалия и спленомегалия, у большинства из них имеется варикозное расширение вен пищевода, но тяжелая дисфункция печени встречается редко [35]. Варикозное расширение вен пищевода может развиваться и при отсутствии цирроза печени [36]. Тромбоз воротной вены — частое осложнение саркоидоза печени, возможно, из-за стаза мелких вен печени. Синдром Бадда — Киари может развиться из-за внешнего сдавления печеночных вен саркоидозной гранулемой, вызывая их сужение, венозный застой и последующий тромбоз [37].
Клинические проявления
Клинические проявления и течение саркоидоза многообразны. Нередко он протекает скрыто и спонтанно излечивается. Иногда болезнь сопровождается теми или иными симптомами, которые напоминают туберкулез, силикоз, лимфогранулематоз, ретикулез, рак и др. Саркоидоз поражает различные органы и системы. Все это, естественно, затрудняет своевременное и правильное распознавание заболевания, особенно при ограниченности методов диагностики и недостаточной осведомленности врачей различных специальностей о саркоидозе.
Пищевод при саркоидозе поражается редко. Дисфагия и потеря веса были отнесены к проявлениям нарушений моторики с нейропатией или миопатией или механической обструкции пищевода с инфильтрацией [38]. Гранулематозная инфильтрация стенок может являться следствием афтозного поражения [39], дивертикулитов [40], стриктур пищевода [41] или его утолщений, а также сужения дистального отдела пищевода [11-13]. Тракционные дивертикулы средней части пищевода могут возникать при гранулематозном воспалении лимфатических узлов средостения. Наиболее часто это состояние вызывают туберкулез и гистоплазмоз [38]. Гастроэнтерологи из клиники Мейо (Джексонвиль, Флорида, США) описали 48-летнего пациента, у которого развилась вторичная ахалазия вследствие саркоидоза пищевода [39]. В некоторых источниках показано, что сужение нижней части пищевода, выявленное при рентгенологическом исследовании, вызвано развитием саркоидоза в его дистальной части или поражением регионарных лимфатических узлов средостения [11, 12, 14]. Внутригрудной саркоидоз может сочетаться с опухолями пищевода и желудка, чем еще больше затрудняет диагностический процесс.
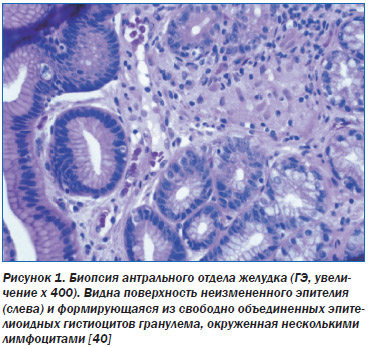
Желудок, особенно антральный его отдел, является самым часто поражаемым полым органом при саркоидозе. Однако, несмотря ни на что, могут встречаться случайные гранулемы при радиологически и эндоскопически нормальном желудке [15]. Наиболее известный симптом — боль в эпигастральной области, как правило, после еды. Также могут быть такие симптомы, как раннее насыщение, тошнота, рвота, потеря веса. Изъязвления слизистой могут вызвать кровотечения верхних отделов ЖКТ, иногда массивные [16, 17]. Иногда на слизистой можно выявить полипы, узелки или большие складки — как при болезни Менетрие. Они могут развиваться, вызывая сужение антрального отдела желудка и деформации, ведущие к желудочной обструкции и сужению двенадцатиперстной кишки [18, 19]. Изменения могут быть ошибочно приняты за рак желудка, хотя эндоскопическое ультразвуковое исследование может помочь в диагностике [20, 21]. У всех больных при гистологическом исследовании биоптатов обнаруживают неказеифицирующиеся эпителиоидноклеточные гранулемы.
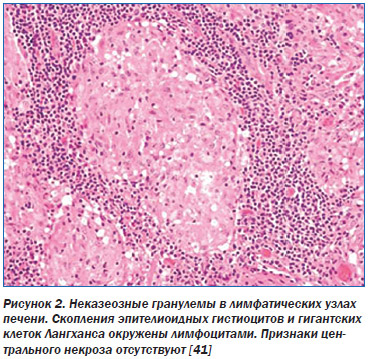
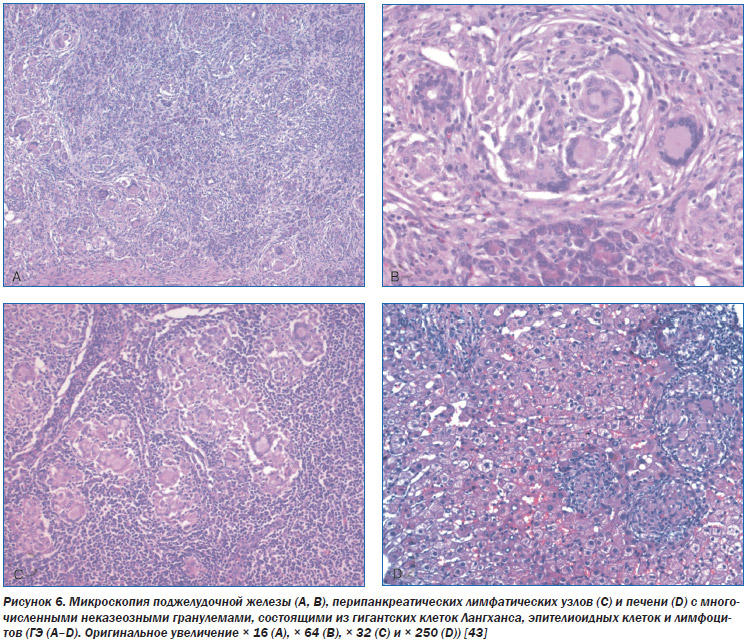
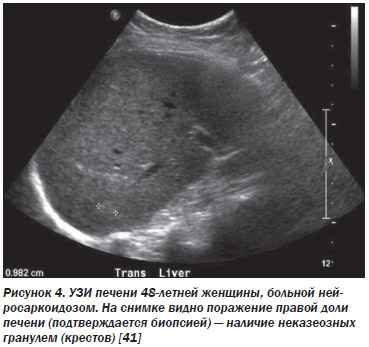
Саркоидоз печени относят к частой (66–80 % случаев поражения органов ЖКТ) локализации болезни, часто протекающей скрыто. Изменения в результатах лабораторных исследований состоят в гипергаммаглобулинемии, умеренном повышении активности щелочной фосфатазы сыворотки крови; изменения при визуализации крайне редки. Признаки саркоидоза печени можно обнаружить с помощью ультразвуковых исследований (рентгеновская компьютерная и магнитно-резонансная томографии — РКТ и МРТ), сканирования с галлием и технецием. Описаны множественные очаговые изменения пониженной плотности в печени и селезенки на РКТ органов брюшной полости даже при нормальной рентгенограмме органов грудной клетки. Саркоидоз печени дает ложноположительные результаты позитронно-эмиссионной томографии. МРТ-исследование не позволяет исключить злокачественную опухоль. Гепатопульмональный синдром, характеризующийся триадой из выраженной патологии печени, артериальной гипоксемии и внутрилегочной дилатации сосудов, при саркоидозе встречается редко. Саркоидоз печени только в 1 % случаев приводит к циррозу и портальной гипертензии. При лапароскопии можно видеть множественные узелки по поверхности печени или селезенки, биопсия которых выявляет неказеифицирующиеся эпителиоидноклеточные гранулемы, содержащие многоядерные гигантские клетки, что особенно часто обнаруживают в области ворот органа. Саркоидоз печени в биоптатах проявляется гистопатологически эпителиоидноклеточными, типичными неказеифицирующимися гранулемами, широко разбросанными по органу, с выраженной тенденцией к портальному или перипортальному расположению. В редких случаях саркоидоз печени осложняется портальной гипертензией или хроническим холестазом. Наряду с гранулемами гистологические изменения печени можно было разделить на три категории: холестатические, некрозно-воспалительные и сосудистые. В 21 % биоптатов выявляются признаки фиброза.
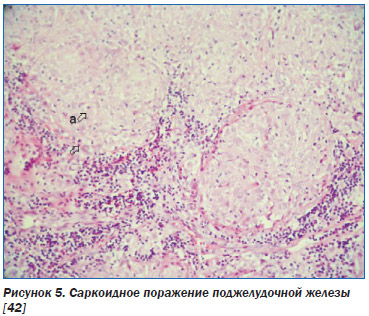
Поджелудочная железа поражается редко, однако изменения могут напоминать рак. 2/3 больных с саркоидозом поджелудочной железы имели боль в животе, а в 3/4 случаев имела место внутригрудная лимфаденопатия. Хронически повышенный уровень липазы может быть одним из первичных признаков, требующих исключения саркоидоза. При эндоскопическом ультразвуковом исследовании может быть обнаружен заметный железистый фиброз железы. У больного с системным саркоидозом при повышении в плазме уровня амилазы и липазы необходима оценка возможного поражения поджелудочной железы. На МРТ подтвержденный на тканевом уровне саркоидоз этого органа проявлялся множественными образованиями в поджелудочной железе с пониженной интенсивностью сигнала на Т1-взвешенном изображении, со средней интенсивностью сигнала на Т2-взвешенном изображении и снижением усиления в сравнении со здоровой поджелудочной железой после применения гадолиния. В отдельных случаях вследствие саркоидозной инфильтрации поджелудочной железы может развиться сахарный диабет.
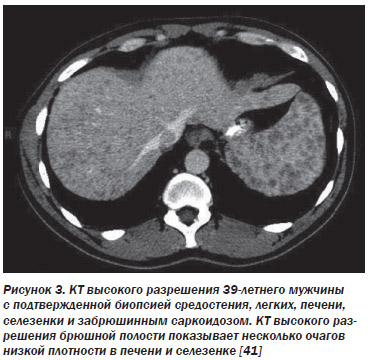
Сочетание саркоидоза с инсулинозависимым диабетом первого типа отмечается очень редко. Описан случай диабета 1-го типа у женщины, у которой клинические и биологические признаки саркоидоза возникли после ее первой беременности с рецидивом сразу после второй беременности. Диагноз саркоидоза был установлен на основании характерных кожных, суставных и легочных проявлений в сочетании с повышенным уровнем ангиотензинпревращающего фермента (АПФ) в плазме крови. Была установлена связь между диабетом 1-го типа и саркоидозом, как реципрокная между саркоидозом и беременностью. Кроме того, в данном случае имел место и семейный саркоидоз [44]. Острый панкреатит связан с воспалительным или вторичным процессом, который часто встречается при развитии гиперкальциемии у больных саркоидозом. Диагноз такого состояния труден, а этот тип панкреатита чувствителен к лечению глюкокортикостероидами [45].
Саркоидоз тонкой кишки — наименее распространенная форма саркоидоза. Пациенты страдают диареей, у них выявляются синдром мальабсорбции, энтеропатия с потерей белка, боли в области пупка или в эпигастрии, кровоизлияния в слизистую. Аналогичные симптомы могут быть при нарушении усвояемости фолиевой кислоты [46] или всасывания витамина В12 в подвздошной кишке при ахлоргидрии [26, 47]. Дифференцировать саркоидоз тонкого кишечника также нужно с целиакией [48]. Антиглиадиновые антитела обнаруживаются у 15–41 % пациентов с саркоидозом, из которых 1–4 % были эндомизиальными антителами [49, 50]. Возможно, имеет место параллельное развитие двух процессов — целиакии и саркоидоза — одновременно.
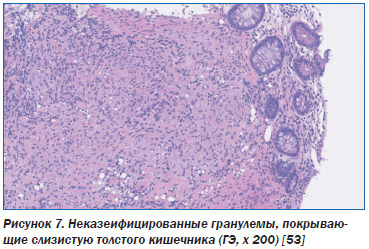
Толстый кишечник, хотя и редко поражается саркоидозом, однако имеет при этом множество гистологических проявлений, представленных множественными узелками, полипами, стенозом, обструктивными поражениями, афтозными кровоточащими эрозиями [8, 9, 51, 52]. Регионарная лимфаденопатия — наиболее частая причина кишечной непроходимости. Симптомами являются боли в животе более чем в 50 % случаев. Гистология обычно показывает неказеозные гранулемы с небольшим воспалением или формированием абсцесса.
Диагностика
Диагноз «саркоидоз печени» установить достаточно трудно, потому что при саркоидозе патогномоничные симптомы или функциональные расстройства в этом органе встречаются редко [54]. Саркоидоз печени в два раза чаще встречается у афроамериканцев, чем у белых [55]. Его клиническими проявлениями могут быть гепатоспленомегалия, повышение уровня ферментов печени, внутрипеченочный холестаз и портальная гипертензия как следствие цирроза печени в связи с давним внутрипеченочным холестазом [54].
Признаком поражения печени при саркоидозе может быть повышение уровня щелочной фосфатазы. Хотя саркоидоз печени и/или селезенки обычно протекает бессимптомно, а увеличение уровня ферментов печени может быть небольшим, по данным исследователей из Японии, методы визуализации (УЗИ брюшной полости, РКТ, МРТ и сканирование с галлием и технецием) могут легко выявить патологию. При лапароскопии можно видеть множественные узелки по поверхности печени или селезенки, биопсия которых выявляет неказеифицированные эпителиоидные гранулемы, содержащие многоядерные гигантские клетки, что особенно часто обнаруживают в области ворот органа [56].
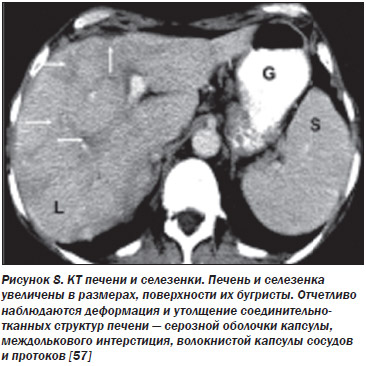
При УЗИ обычно выявляют множественные гипоэхогенные узлы, которые локализуются как в печени, так и в селезенке. У части больных проведение КТ-исследования позволяет не только подтвердить гепатолиенальные изменения, но и обнаружить мелкоочаговые изменения и инфильтраты в обоих легких с внутригрудной лимфаденопатией или без нее. На компьютерных томограммах, как правило, наблюдаются гепатомегалия, ровные или волнистые контуры, диффузная неоднородность паренхимы. При контрастировании в структуре печени могут определяться мелкие гиподенсные очаги. При саркоидозе в большинстве случаев выявляются также спленомегалия и увеличение лимфатических узлов в гепатодуоденальной связке, в воротах печени и селезенки, в перипанкреатической клетчатке. КТ-изменения при гранулематозных заболеваниях неспецифичны и требуют морфологической верификации.
Дифференциальная диагностика
Дифференциальную диагностику гранулематозного гастрита следует проводить с болезнью Крона, реакцией на инородное тело, туберкулезом и сифилисом [58, 59]. Саркоидоз толстой и подвздошной кишки также может имитировать болезнь Крона [60–62]. Сходство морфологического субстрата болезни Крона и саркоидоза (гранулематоз без очагов казеозного некроза) позволяет предполагать общие механизмы развития, обусловливающие возможность их сочетания. Установлено, что в формировании тканевого повреждения при этих заболеваниях участвуют одни и те же медиаторы, в том числе интерлейкин-2 и фактор некроза опухоли альфа. Неоднократно предпринимались попытки объединить саркоидоз и болезнь Крона единым этиологическим фактором (прежде всего инфицированием представителями рода Mycobacteria), однако результаты их оказались малоубедительными.
В пользу определенного сходства саркоидоза и болезни Крона свидетельствует и неоднократно обнаруживаемая при последней гиперкальциемия, механизм развития которой оказался близким к таковому при саркоидозе. I.C. Mitchell и соавт. [63] удалось воспроизвести реакцию Квейма, считающуюся относительно специфичной для саркоидоза, у мышей с воспалительным заболеванием кишечника, аналогичным болезни Крона. J.M. Smiejan и соавт. [64], сравнив особенности изменений параметров бронхоальвеолярного лаважа при саркоидозе и болезни Крона, констатировали их стереотипность: отмечено преобладание лимфоцитов в лаважной жидкости. Вместе с тем увеличение плазменной активности АПФ (характерный маркер активности саркоидоза) при болезни Крона не выявлено.
Клинические аргументы в пользу сходства саркоидоза и болезни Крона выглядят еще более убедительно. Среди них обращают на себя внимание общие внеорганные проявления, прежде всего узловатая эритема, часто наблюдающаяся как при саркоидозе, так и при болезни Крона. Четко продемонстрировано, что узловатая эритема может появляться значительно раньше первых специфичных признаков этих заболеваний. Выявляется общее отсутствие архитектурных искажений слизистой и острое ее воспаление. Саркоидоз обычно лучше реагирует на лечение кортикостероидами, чем болезнь Крона, часто с улучшением через несколько дней [65]. Редко саркоидоз сосуществует с болезнью Крона или неспецифическим язвенным колитом [66–69].
Подавляющее большинство исследователей отмечают положительную реакцию Квейма чаще при остром или подостро прогрессирующем саркоидозе, сопровождающемся узловатой эритемой и преимущественным поражением внутригрудных лимфатических узлов. Такую закономерность установили Hurley и Bartholomeusz [70] при анализе сводных данных о 1316 больных саркоидозом из 37 стран, которым в 1966–1969 гг. была произведена проба Квейма одним и тем же антигеном. Оказалось, что положительная реакция была в среднем у 53,5 % больных саркоидозом, причем чаще при подострой его форме (62,4 %), в I стадии заболевания (72,8 %) и при наличии узловатой эритемы (77,7 %).
На частоту и интенсивность реакции Квейма влияет лечение кортикостероидными гормонами. Угнетающее действие кортикостероидов наиболее отчетливо выявляется в тех случаях, когда антиген вводят в день приема гормонов. Оно выражено в меньшей степени при постановке пробы через 4–6 нед. после гормональной терапии. Это обстоятельство, а также крайне замедленное образование местной реакции и необходимость производить с целью диагностики не только однократно, но иногда и повторно биопсию кожи, на что не все больные охотно соглашаются, являются недостатками пробы Квейма.
Вместе с тем следует подчеркнуть, что проба Квейма оказывается иногда положительной при некоторых других заболеваниях. По данным Hurley и Bartholomeusz [70], она была сомнительной или положительной у 1,7 % из 722 больных с различными патологическими процессами, кроме саркоидоза. У некоторых больных на саркоидный антиген реагируют больные проказой, боррелиозом, гистоплазмозом, кокцидиоидным микозом, недавно вакцинированные БЦЖ и др.
Известно также, что при саркоидозе образуется местная реакция на внутрикожное введение суспензии ткани печени, селезенки, кожи, лимфатических узлов здоровых людей, коров, морских свинок, крыс, а также лиц, страдающих лейкемией. Эти данные свидетельствуют о том, что реакция Квейма приобретает определенное диагностическое и прогностическое значение лишь в сочетании с другими клинико-рентгенологическими и лабораторными методами исследования. Вместе с тем эти данные лишний раз свидетельствуют о том, что у больных саркоидозом отнюдь не подавлена полностью реактивность организма и что тенденция к анергии имеет более или менее избирательный характер. Но причины этого явления пока еще недостаточно изучены.
Рекомендуемое начальное обследование больного саркоидозом согласно международному соглашению
Анамнез (воздействие факторов окружающей среды и профессии, симптомы).
Физикальное обследование.
Прямая обзорная рентгенограмма органов грудной клетки.
Исследование функции дыхания: спирометрия и Dlco.
Клинический анализ крови: подсчет лейкоцитов и лейкоцитарной формулы, красная кровь, тромбоциты, СОЭ.
Содержание в сыворотке крови кальция, печеночных ферментов (АлАТ, АсАТ, ЩФ), креатинина, азота мочевины крови.
Общий анализ мочи.
Электрокардиограмма (ЭКГ).
Обследование офтальмолога.
Туберкулиновая проба Манту с двумя туберкулиновыми единицами (2 ТЕ) очищенного туберкулина (ППД-Л) в стандартном разведении для внутрикожного применения.
Алгоритм диагностики, порядок обследования и направления на госпитализацию больных саркоидозом [71] зависят от этапа обследования, преобладания поражения органов и систем.
1. Объем обследования при первичной диагностике саркоидоза: общий клинический анализ крови с лейкоцитарной формулой, общий анализ мочи, анализы крови на функциональные пробы печени (билирубин, АлАТ, АсАТ), уровень сахара, Са++, активность АПФ; прямая обзорная рентгенограмма органов грудной клетки, рентгеновская компьютерная томография высокого разрешения, бактериоскопия мокроты (индуцированной мокроты при отсутствии спонтанной мокроты) с окраской мазка по Цилю — Нильсену на кислотоустойчивые микобактерии (КУМ) не менее 3 раз, при возможности — бронхоальвеолярный лаваж в подсчетом клеток (расчет CD4/CD8); спирометрия с бронхолитиком, УЗИ печени, селезенки, почек, ЭКГ; консультация офтальмолога (с определением остроты зрении и осмотром глазного дна и переднего отрезка) — по месту жительства пациента, а также оценка диффузионной способности легких (многопрофильное ЛПУ или диагностический центр).
2. Объем исследований, проводимых при дифференциальной диагностике саркоидоза и туберкулеза в специализированном противотуберкулезном учреждении: проба Манту с 2 ТЕ, бактериоскопия мокроты (индуцированной мокроты при отсутствии спонтанной мокроты) на КУМ не менее 3 раз, посев мокроты на КУМ (не менее 3 образцов). По решению консилиума или ЦВКК РКПД больному могут быть проведены дополнительные исследования: РКТ, бронхоскопия с взятием образцов на КУМ, повторные анализы крови (общий клинический, Са++ крови, активность АПФ, СРБ и др.).
3. Рекомендуемый объем исследования больного при динамическом наблюдении по месту жительства: общий клинический анализ крови с лейкоформулой, общий анализ мочи, прямая обзорная рентгенограмма органов грудной клетки (при необходимости рентгеновская компьютерная томография высокого разрешения), спирометрия, оценка диффузионной способности легких, функциональные пробы печени (билирубин, АлАТ, АсАТ), УЗИ печени, селезенки, почек, ЭКГ; офтальмологическое обследование (глазное дно). Частота обследований и их объем определяются лечащим врачом в зависимости от активности саркоидоза (1, 3, 6 или 12 месяцев).
4. Показания для направления пациента с саркоидозом для неотложной госпитализации:
а) в пульмонологические (терапевтические) отделения:
— тяжелое течение саркоидоза и/или полиорганное поражение с развитием недостаточности органов и систем (дыхательной, сердечной, почечной недостаточности 2-й степени и более), сочетание легочного саркоидоза с поражением ЦНС, развитием блокад и аритмий сердца и поражением органа зрения;
— необходимость проведения терапии высокими дозами системных глюкокортикостероидов, цитостатиков, эфферентных методов терапии (плазмаферез, экстракорпоральная модификация лимфоцитов и др.);
б) кардиологические отделения:
— тяжелые аритмии и блокады у больных саркоидозом;
в) неврологические отделения:
— тяжелые поражения центральной и периферической нервной системы (фокусы в головном мозге, очаговый менингоэнцефалит, паралич лицевого нерва, периферическая нейропатия и другие);
г) торакальные хирургические отделения:
— необходимость проведения инвазивной диагностики (видеоторакоскопическая биопсия, трансбронхиальная и открытая биопсия легкого или ВГЛУ, других органов); бронхоскопия с биопсией; медиастиноскопия и др.;
— развитие спонтанного пневмоторакса на фоне сотового легкого (срочная госпитализация);
д) хирургические отделения неторакального профиля:
— необходимость биопсии печени, других органов брюшной полости, кожи, периферического лимфатического узла;
е) офтальмологические отделения:
— тяжелые формы поражения органа зрения с угрозой слепоты (увеиты, иридоциклиты).
Порядок наблюдения больного саркоидозом
1. С впервые выявленным активным саркоидозом:
— при положительной динамике, инволюции процесса, положительном ответе на проводимую терапию, состоянии без динамических изменений и при наличии недостаточности органов и систем не более 1-й степени: первый год — посещение врача каждые 3 мес., второй — каждые 6 мес., далее 1 раз в год;
— при рефрактерности к лечению: посещение врача не реже 1 раза в 3 месяца.
2. С рецидивами и прогрессирующим течением заболевания:
— при рецидиве с положительным ответом на лечение (в течение не менее 3 месяцев) посещение врача 1 раз в 3 месяца в течение 2 лет, далее 1 раз в год;
— при прогрессирующем течении заболевания посещение врача не реже 1 раза в 3 месяца.
3. С неактивным саркоидозом: посещение врача 1 раз в год.
В соответствии с международным соглашением по саркоидозу больных с однажды выявленным саркоидозом рекомендуется наблюдать пожизненно.
Лечение саркоидоза
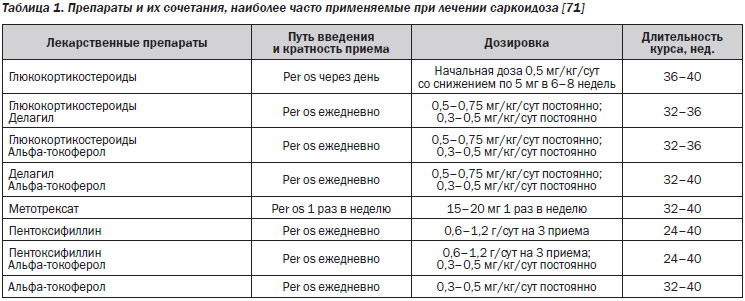
Основным методом лечения являются кортикостероиды, показанные при появлении симптомов со стороны печени или при обширном фиброзе печени. При развитии портальной гипертензии требуется также лечение варикозной болезни пищевода. Описаны удачные пересадки печени при саркоидозе, но необходимость в этом возникает крайне редко и не исключает рецидивов саркоидоза любой локализации. В табл. 1 приведены препараты и их сочетания, наиболее часто применяемые при лечении саркоидоза.
Жизнь с саркоидозом
Причина саркоидоза остается неизвестной, так что в настоящее время невозможно предотвратить или вылечить эту болезнь. Тем не менее врачами накоплен большой клинический опыт в управлении этой болезнью. Следует отметить, что большинство людей с саркоидозом ведут нормальную жизнь.
Если у пациента есть саркоидоз, он может помочь себе сам, следуя разумным рекомендациям по охране здоровья. Пациент не должен курить. Ему также следует избегать контакта с некоторыми веществами, такими как пыль и химические вещества, которые могут нанести вред легким.
Несмотря на то, что тяжелый саркоидоз может уменьшить шансы забеременеть, особенно для пожилых женщин, многие молодые женщины с саркоидозом родили здоровых детей во время лечения. Если пациенты планируют завести ребенка, они должны обсудить этот вопрос со своим врачом. Медицинские осмотры на протяжении всей беременности и сразу после этого особенно важны для пациентов с саркоидозом. В некоторых случаях постельный режим необходимо соблюдать в течение последних трех месяцев беременности. Помимо семьи и близки друзей рекомендуется общение с группами самопомощи, чтобы помочь пациентам справиться с саркоидозом. Поддерживая связь с ними, они могут поделиться личными чувствами и переживаниями. Как правило, пациенты обладают достоверной информацией о последних научных достижениях по саркоидозу, знают, где работают лучшие специалисты в этой области и как улучшить свою самооценку.
Больным саркоидозом рекомендуются следующие меры для улучшения образа жизни, позволяющие организму бороться с заболеванием:
— бросить курить, если больной курит;
— избегать попадания пыли, химических веществ, дыма и токсичных газов;
— соблюдать здоровую сбалансированную диету;
— пить много воды;
— много двигаться, выполнять физические нагрузки и спать;
— меньше бывать на солнце и не употреблять витамин D;
— найти группу поддержки по саркоидозу.
Прогноз и качество жизни
Если обратиться к форумам больных саркоидозом в Интернете, то изменение образа жизни, рациональное питание, пересмотр психологических жизненных ценностей нередко способствуют спонтанным ремиссиям. Направление больного при выявлении к фтизиатру и онкологу может усугублять этот стресс. Специально проведенные за рубежом исследования показали, что среди нелеченых больных саркоидозом встречаются тревожность с депрессией, агрессивность, что больным саркоидозом необходима психотерапия даже тогда, когда не требуется медикаментозное лечение [72]. Аналогичные выводы сделаны и в более новом исследовании, согласно которому среди больных, страдавших саркоидозом, пациенты с симптомами и женщины подвержены риску развития депрессии, им изначально рекомендована помощь психолога [73]. Многолетнее исследование качества жизни (КЖ) больных саркоидозом, проведенное в России и за рубежом с использованием средств телемедицины, показало, что КЖ больных саркоидозом снижено по всем параметрам жизнедеятельности и по большинству показателей ниже, чем в группах больных с заболеваниями, сходными с саркоидозом по клинической симптоматике (бронхиальная астма, ХОБЛ, рак легкого, легочный туберкулез, неспецифические артрозы, хронические дерматозы). На КЖ больных саркоидозом влияет социальный статус больного: факторами, снижающими КЖ больных по шкале психологического здоровья, являются женский пол и отсутствие семьи по шкале общего КЖ и шкале социальных взаимоотношений [75].
Хроническая усталость при саркоидозе, порой приобретающая крайние формы, лишает больного трудоспособности [76], но не констатируется медицинскими экспертами (лечащими врачами или представителями ВТЭК), устанавливающими работоспособность пациентов по объективным характеристикам. Жалобы больного не находят понимания врача, больной в глазах медика предстает симулянтом, что способствует усилению депрессии. Голландские клиницисты выделяют 4 типа усталости при саркоидозе: утренняя усталость, когда пациент после пробуждения не может подняться с постели; интермиттирующая усталость в течение дня, вынуждающая пациента приучать себя к прерывистому темпу своей активности (чередовать периоды активности и отдыха); вечерняя слабость, когда пациент просыпается утром с адекватной для жизни энергией, но чувствует себя «выжатым» уже к началу вечера; постсаркоидозный синдром хронической усталости, характеризующийся постоянной миалгией, чувством усталости, слабости и депрессией. Отсутствие каких-либо объективных проявлений сбивает с толку пациента и врача, нужен тщательный расспрос, чтобы уловить связь между этим синдромом и саркоидозом [76].
Для больных саркоидозом специальные медицинские образовательные программы пока не разработаны, хотя для самоконтроля за стрессом, восстановления чувства собственного достоинства и поиска альтернативных источников удовлетворения качества жизни таких больных многие исследователи предлагают варианты подобной помощи. В университете Ричмонда (США) предложена теория мастерства (the theory of mastery), которая помогает стать устойчивее к собственному состоянию и факторам окружающей среды. В основу положена работа медицинских сестер, которые помогают больным стимулировать собственный рост по 4 ступеням (уверенность, изменение, признание и рост) и тем самым достичь лучшего КЖ [77]. Кроме того, в ряде стран больные сами объединяются в организации по признаку их заболевания. В частности, в Голландии активно функционирует Голландское саркоидозное общество (DSS) [89], объединяющее больных и их родственников с целью поддержки людей, заболевших саркоидозом, обеспечения их первичной информацией об этом заболевании [79].
1. Iwai K., Tachibana T., Hosoda Y. et al. Sarcoidosis autopsies in Japan: Frequency and trend in the last 28 years // Sarcoidosis. 1988; 5: 60-5.
2. Longcope W.T., Freiman D.G. A study of sarcoidosis: Based on a combined investigation of 160 cases including 30 autopsies from The Johns Hopkins Hospital and Massachusetts General Hospital // Medicine. 1952; 31: 1-132.
3. Ricker W., Clark M. Sarcoidosis: A clinicopathologic review of three hundred cases, including twenty-two autopsies // J. Clin. Pathol. 1949; 19: 725-49.
4. Hercules H.C., Bethlem N.M. Value of liver biopsy in sarcoidosis // Arch. Pathol. Lab. Med. 1984; 108: 831-4.
5. Irani S.K., Dobbins W.O. Hepatic granulomas: Review of 73 patients from one hospital and survey of the literature // J. Clin. Gastroenterol. 1979; 1: 131-43.
6. Iwai K., Oka H. Sarcoidosis: Report of ten autopsy cases in Japan // Am. Rev. Respir. Dis. 1964; 90: 612-22.
7. Siegel C.I., Honda M., Salik J. et al. Dysphagia due to granulomatous myositis of the cricopharyngeus muscle: Physiological and cineradiographic studies prior to and following successful surgical therapy // Trans. Assoc. Am. Physicians. 1961; 74: 342-52.
8. Boyum R., Yeung K.J., Kaplan K.J. et al. Pediatric gastrointestinal sarcoidosis presenting with protein-losing enteropathy // J. Ped. Gastroenterol. Nutr. 2007; 44: 152-6.
9. Levine M.S., Ekberg O., Rubesin S.E. et al. Gastrointestinal sarcoidosis: Radiographic findings // Am. J. Roentgenol. 1989; 153: 293-5.
10. Wiesner P.J., Kleinman M.S., Condemi J.J. et al. Sarcoidosis of the esophagus // Am. J. Digest. Dis. 1971; 16: 943-51.
11. Hardy W.E., Tulgan H., Haidak G. et al. Sarcoidosis: A case presenting with dysphagia and dysphonia // Ann. Intern. Med. 1967; 66: 353-7.
12. Cappell M.S. Endoscopic, radiographic, and manometric findings in dysphagia associated with sarcoid due to extrinsic esophageal compression from subcarinal lymphadenopathy // Am. J. Gastroenterol. 1995; 90: 489-92.
13. Polachek A.A., Matre W.J. Gastrointestinal sarcoidosis: Report of a case involving the esophagus // Am. J. Dig. Dis. 1964; 9: 429-33.
14. Cook D.M., Dines D.E., Dycus D.S. Sarcoidosis: Report of a case presenting as dysphagia // Chest. 1970; 57: 84-6.
15. Palmer E.D. Note on silent sarcoidosis of the gastric mucosa // J. Lab. Clin. Med. 1958; 52: 231-4.
16. Low V.H., Heyneman L.E. Gastric ulceration due to sarcoidosis // Am. J. Roentgenol. 1999; 172: 251-2.
17. Ona F.V. Gastric sarcoid: Unusual cause of upper gastrointestinal hemorrhage // Am. J. Gastroenterol. 1981; 75: 286-8.
18. Chinitz M.A., Brandt L.J., Frank M.S. et al. Symptomatic sarcoidosis of the stomach // Dig. Dis. Sci. 1985; 30: 682-8.
19. Kaneki T., Koizumi T., Yamamoto H. et al. Gastric sarcoidosis — а single polypoid appearance in the involvement // Hepatogastroenterology. 2001; 48: 1209-10.
20. Korsager S. Sarcoidosis of the stomach. A case report // Scand. J. Respir. Dis. 1979; 60: 24-8.
21. DeAngelis C., Caula G., Rizzetto M. et al. EUS in gastric sarcoidosis // Gastrointestinal Endoscopy. 1999; 49: 639-41.
22. Miller L.K., Rochester D., Miller J.W. Extensive abdominal lymphadenopathy in sarcoidosis // Am. J. Gastroenterol. 1981; 75: 367-9.
23. Noel J.M., Katona I.M., Pineiro-Carrero V.M. Sarcoidosis resulting in duodenal obstruction in an adolescent // J. Ped. Gastroenterol. Nutr. 1997; 24: 594-8.
24. Stampfl D.A., Grimm I.S., Barbot D.J. et al. Sarcoidosis causing duodenal obstruction. Case report and review of gastrointestinal manifestations // Dig. Dis. Sci. 1990; 35: 526-32.
25. Okamura S., Iesaki K., Muramatsu S. Gastric-aspirate angiotensin-converting enzyme in gastrosarcoidosis // Lancet. 1991; 338: 121.
26. Tinker M.A., Viswanathan B., Laufer H. et al. Acute appendicitis and pernicious anemia as complications of gastrointestinal sarcoidosis // Am. J. Gastroenterol. 1984; 79: 868-72.
27. Romero-Gomez M., Suarez-Garcia E., Otero M.A. et al. Sarcoidosis, sclerosing cholangitis, and chronic atrophic autoimmune gastritis: A case of infiltrative sclerosing cholangitis // J. Clin. Gastroenterol. 1998; 27: 162-5.
28. Rudzki C., Ishak K.G., Zimmerman H.J. Chronic intrahepatic cholestasis of sarcoidosis // Am. J. Med. 1975; 59: 373-87.
29. Devaney K., Goodman Z.D., Epstein M.S. et al. Hepatic sarcoidosis. Clinicopathologic features in 100 patients // Am. J. Surg. Pathol. 1993; 17: 1272-80.
30. Alam I., Levenson S.D., Ferrell L.D. et al. Diffuse intrahepatic biliary strictures in sarcoidosis resembling sclerosing cholangitis. Case report and review of the literature // Dig. Dis. Sci. 1997; 42: 1295-301.
31. Murphy J.R., Sjogren M.H., Kikendall J.W. et al. Small bileduct abnormalities in sarcoidosis // J. Clin. Gastroenterol. 1990; 12: 555-61.
32. Bloom R., Sybert A., Mascatello V.J. Granulomatous biliary tract obstruction due to sarcoidosis // Am. Rev. Res. Dis. 1978; 117: 783-7.
33. Rezeig M.A., Fashir B.M. Biliary tract obstruction due to sarcoidosis: A case report // Am. J. Gastroenterol. 1996; 92: 527-8.
34. Maddrey W.C., Johns C.J., Boitnott J.K. et al. Sarcoidosis and chronic hepatic disease: A clinical and pathologic study of 20 patients // Medicine. 1970; 49: 375-95.
35. Rosenberg J.C. Portal hypertension complicating hepatic sarcoidosis // Surgery. 1971; 69: 294-9.
36. Nelson R.S., Sears M.E. Massive sarcoidosis of the liver. Report of 2 cases // Am. J. Dig. Dis. 1968; 13: 95-106.
37. Russi E.W., Bansky G., Pfaltz M. et al. Budd-Chiari syndrome in sarcoidosis // Am. J. Gastroenterol. 1986; 81: 71-5.
38. Raziel А. et al. Sarcoidosis and giant midesophageal diverticulum // Dis. Esophag. 2000; 13(4): 317-319.
39. Lukens F.J., Machicao V.I., Woodward T.A. et al. Esophageal sarcoidosis: an unusual diagnosis // J. Clin. Gastroenterol. 2002; 34: 54-6.
40. Gastric sarcoidosis mimicking irritable bowel syndrome-Cause not association? http://www.wjgnet.com/1007-9327/12/4754.asp.
41. Gastrointestinal and Hepatic Manifestations of Sarcoidosis Ellen C., Ebert et al. // Am. J. Gastroenterol. 2008; 103: 3184-3192.
42. Symptomatic Pancreatic Sarcoidosis. Case Report and Review of Literature M. Shukla, M.F. Hassan, V. Toor, J. Kaur, C. Solomon, H. Cohen // J. Pancreas (Online). 2007; 8(6): 770-774.
43. Extrapulmonary sarcoidosis of liver and pancreas: A case report and review of literature. http://www.wjgnet.com/1007-9327/13/2504.asp.
44. Djrolo F., Gervaise N., Vaillant L. et al. Post-partum recurrent sarcoidosis associated with type I diabetes mellitus // Diabetes Metab. 2003; 29: 82-85.
45. Sanchez-Lozada R. Acute pancreatitis, diabetes, and sacoidosis. Case report and review of the literature // PubMed. 2004 May — Jun; 140(3): 343-5.
46. MacRury S.M., McQuaker G., Morton R. et al. Sarcoidosis: Association with small bowel disease and folate deficiency // J. Clin. Pathol. 1992; 45: 823-5.
47. Sprague R., Harper P., McClain S. et al. Disseminated gastrointestinal sarcoidosis. Case report and review of the literature // Gastroenterology. 1984; 87: 421-5.
48. Douglas J.G., Gillon J., Logan R.F. et al. Sarcoidosis and coeliac disease: An association? // Lancet. 1984; 2: 13-5.
49. Papadopoulos K.I., Sjoberg K., Lindgren S. et al. Evidence of gastrointestinal immune reactivity in patients with sarcoidosis // J. Int. Med. 1999; 245: 525-31.
50. McCormick P.A., Feighery C., Dolan C. et al. Altered gastrointestinal immune response in sarcoidosis // Gut. 1988; 29: 1628-31.
51. Deconda D., Tudi S.R., Patel V. et al. Asymptomatic colonic sarcoid polyps // Am. J. Gastroenterol. 2006; 101: S337-A843.
52. Zech J.R., Kroger E., Bonnin A.J. et al. Sarcoidosis: Unusual cause of a rectal mass // South. Med. J. 1993; 86: 1054-5.
53. Sarcoidosis V. Nannegari, E. Irions et al. A rare case of colonic http://www.amc.edu/academic/GME/programs/Gastroenterology/documents/colonic_sarcoid_-_nannegari.pdf
54. Branson J.H., Park J.H. Sarcoidosis — Hepatic involvement: Presentation of a case with fatal liver involvement, including autopsy findings and review of the evidence for sarcoid involvement of the liver as found in the literature // Ann. Intern. Med. 1954; 40: 111-45.
55. Baughman R.P., Teirstein A.S., Judson M.A. et al. Case Control Etiologic Study of Sarcoidosis (ACCESS) research group. Clinical characteristics of patients in a case control study of sarcoidosis // Am. J. Resp. Crit. Care Med. 2001; 164: 1885-9.
56. Kitamura M., Ishizaki T. Sarcoidosis of the liver and spleen in Japan. http://www.ncbi.nlm.nih.gov/pubmed/8046847.
57. http://www.radiomed.ru/publications/priezientatsiia-ogk-kt-diaghnostika-i-diffierientsial-naia-diaghnostika-sarkoidoza.
58. Ectors N.L., Dixon M.F., Geboes K.J. et al. Granulomatous gastritis: A morphological and diagnostic approach // Histopathology. 1993; 23: 55-61.
59. Shapiro J.L., Goldblum J.R., Petras R.E. A clinicopathologic study of 42 patients with granulomatous gastritis // Am. J. Surg. Pathol. 1996; 20: 462-70.
60. Dumot J.A., Adal K., Petras R.E. et al. Sarcoidosis presenting as granulomatous colitis // Am. J. Gastroenterol. 1998; 93: 1949-51.
61. Brunner J., Sergi C., Muller T. et al. Juvenile sarcoidosis presenting as Crohn’s disease // Eur. J. Pediatr. 2006; 165: 398-401.
62. Bulger K., O’Riordan M., Purdy S. et al. Gastrointestinal sarcoidosis resembling Crohn’s disease // Am. J. Gastroenterol. 1988; 83: 1415-7.
63. Mitchell I.C., Turk J.L. Observations on the Kveim reaction using an animal model of granulomatous bowel disease // Pub. Med. Gut. 1991 Feb; 32(2): 159-62.
64. Smiejan J.M. et al. Sarcoid-like lymphocytosis ofthe lower respiratory tract in patients with active Crohn’s disease // Annals of Internal Medicine. 1986; 104: 17.
65. Hilzenrat N., Spanier A., Lamoureux E. et al. Colonic obstruction secondary to sarcoidosis: Nonsurgical diagnosis and management // Gastroenterology. 1995; 108: 1556-9.
66. Fellermann K., Stahl M., Dahlhoff K. et al. Crohn’s disease and sarcoidosis: Systemic granulomatosis? // Eur. J. Gastroenterol. Hepatol. 1997; 9: 1121-4.
67. Fries W., Grassi S.A., Leone L. et al. Association between inflammatory bowel disease and sarcoidosis. Report of two cases and review of the literature // Scand. J. Gastroenterol. 1995; 30: 1221-3.
68. Theodoropoulos G., Archimandritis A., Davaris P. et al: Ulcerative colitis and sarcoidosis: A curious association-report of a case // Dis. Colon. Rectum. 1981; 24: 308-10.
69. Van Steenbergen W., Fevery J., Vandenbrande P. et al. Ul-cerative colitis, primary sclerosing cholangitis, bile duct carcinoma, and generalized sarcoidosis // J. Clin. Gastroenterol. 1987; 9: 574-9.
70. Hurley T.H., Bartholomeusz C.L. The Kveim test in sarcoidosis // Med. J. Aust. 1968 Nov 23; 2(21): 947-949.
71. Саркоидоз. Учебно-методическое пособие / Под ред. А.Г. Чучалина. — Казань, 2010.
72. Escande M., Gardes J.P., Gayral L.F. Reactions and psychic disorders in Besnier-Boeck-Schaumann disease: Clinical and psychological approach; application of a scale of aggressive behavior to the mental profile // Ann. Med. Psychol. (Paris). 1980; Vol. 138, № 7: 813-828.
73. Guneylioglu D., Ozseker F., Baran A. et al. Sarcoidosis and depression // Europ. Resp. J. 2002; Vol. 20(Suppl. 38): Ref. P2758: P. 435s.
74. Гурылева М.Э., Визель Е.А., Казаков И.М. и др. Саркоидоз глазами пациента: результаты опросов больных // Пробл. туб. 2003; № 6: 10-13.
75. Drent M. et al. Fatigue associated with obstructive sleep apnea in a patient with sarcoidosis // Respiration. 2000; Vol. 67, № 3: 337-340.
76. James D.G. Complications of sarcoidosis: Chronic fatigue syndrome // Sarcoidosis. 1993; Vol. 10, № 1: 1-3.
77. White K.R. The transition from victim to victor: application of the theory of mastery // J. Psychosoc. Nurs Ment. Health Serv. 1995; Vol. 33, № 8: 41-44.
78. De Vries J. et al. Quality of life in sarcoidosis: a comparison between members of a patient organisation and a random sample // Sarcoidosis Vasc. Diffuse Lung Dis. 1998; Vol. 15, № 2: 183-188.
79. Саркоидоз: от гипотезы к практике / Под ред. А.А. Визеля. — Казань: Издательство «ФЭН», Академия наук РТ, 2004.