Газета «Новости медицины и фармации» Неврология (339) 2010 (тематический номер)
Вернуться к номеру
Гемореология и гемостаз у больных пожилого возраста с дисциркуляторной энцефалопатией
Авторы: М.Ю. Максимова, В.Г. Ионова, М.В. Костырева, А.А. Шабалина, Е.Н. Сыскина, Научный центр неврологии РАМН, г. Москва, Кафедра нервных болезней с/ф МГМСУ, г. Москва
Версия для печати
Атеросклероз и артериальная гипертония являются основой тяжелой возрастной патологии сосудистой системы головного мозга. При этом не только структурные изменения сосудов, но и функциональные изменения ангиогемических взаимодействий между клетками крови и сосудистой стенкой, сказываясь на кровоснабжении головного мозга, оказывают существенное влияние на проявление церебральной дисциркуляции при старении [1–3].
Среди факторов, осложняющих течение дисциркуляторной энцефалопатии (ДЭ) у лиц пожилого возраста, важная роль принадлежит гемореологическим и гемостатическим нарушениям и дисфункции эндотелия [2, 4, 5]. Возрастные изменения системы кровоснабжения головного мозга в условиях артериальной гипертонии и атеросклероза сопровождаются снижением ее адаптационных возможностей, что приводит к напряжению и перенапряжению регуляторных механизмов системы гемостаза [2–4].
Для оценки функционального состояния разных систем при старении наибольшие возможности открывает использование проб с нагрузками. Напряжение системы, вызываемое применением функциональных проб, позволяет выявить ее возрастную недостаточность. Аналогичный подход был использован нами при изучении возрастных сдвигов гемостатических процессов.
Цель работы — проанализировать характер изменений гемореологических и гемостатических детерминант с учетом атромбогенного резерва сосудистой стенки при дисциркуляторной энцефалопатии у больных пожилого возраста.
Материалы и методы
Обследованы 58 больных с дисциркуляторной энцефалопатией в возрасте 68,5 ± 5,6 года. У большинства больных впервые повышение АД было отмечено на пятом и шестом десятилетии жизни. Уровень систолического давления (САД) (средний по результатам измерений) у них находился в рамках I–II степени АГ в соответствии с критериями ВОЗ (1999 г.) — 140–179 мм рт.ст. Уровень диастолического АД (ДАД) также не превышал верхнего предела II степени АГ, т.е. был не выше 109 мм рт.ст. На глазном дне наблюдалась типичная картина гипертонической ангиопатии. При ЭхоКГ отмечались умеренные изменения в виде гипертрофии левого желудочка. Установленные при ультразвуковой допплерографии и дуплексном сканировании данные о проходимости магистральных артерий головы позволяют объяснить связь имеющихся у больных неврологических симптомов с поражением в первую очередь внутримозговых сосудов.
У пожилых больных с дисциркуляторной энцефалопатией нами были выделены следующие синдромы: подкорковый (44 %), псевдобульбарный (24 %) и вестибуло-мозжечковый (32 %). В 45 % наблюдений симптоматика была смешанной. Кроме того, у всех больных определялись разной степени выраженности нарушения интеллектуально-мнестических функций. При рентгеновской компьютерной томографии были выявлены небольшие инфаркты, расположенные в зоне васкуляризации глубоких ветвей основных артерий мозга (базальные ядра, внутренняя капсула, белое вещество мозга), а также снижение плотности перивентрикулярного белого вещества, расширение желудочков и субарахноидальных пространств.
Исследовались следующие гемореологические и гемостатические показатели: вязкость крови (ВК), гематокрит (Ht), фибриноген (ФГ), агрегация эритроцитов (АЭ), АДФ-индуцированная агрегация тромбоцитов (АДФ-АТ), концентрация растворимых комплексов фибрин-мономера (РКФМ). Проводилось исследование системы антикоагулянтов крови: активности протеина С (ПС), антитромбина III (AT III). Активность фибринолитической системы крови анализировали на основании определения времени лизиса эуглоблинового сгустка (ВЛЭС), фибринолитической активности эуглобулиновой фракции (ФАЭФ), содержания антигена тканевого активатора плазминогена (tpA), ингибитора активатора плазминогена (РАГ-1), Д-димера, продуктов деградации фибрина. Для оценки атромбогенной активности сосудистой стенки была проведена манжеточная проба (МП), создающая кратковременную ишемию плеча. Реакцией на эти пробы у здоровых людей является дополнительное образование AT III, ПС, tpA, что приводит к снижению агрегации тромбоцитов крови и характеризует реактивность антитромботической и фибринолитической активности крови [2].
Контрольную группу составили 20 практически здоровых лиц в возрасте 47,0 ± 3,6 года.
Результаты и обсуждение
У больных пожилого возраста с дисциркуляторной энцефалопатией в условиях стабилизации АД показатели Ht и АДФ-АТ существенно не отличались от данных, полученных при обследовании здоровых лиц. Установлено увеличение ВК — 5,6 ± 0,4 отн. ед. (р < 0,001) на фоне повышенных значений агрегационной активности эритроцитов — 18,6 ± 4,3 % (р < 0,001). Как известно, повышение вязкости крови при изменениях функциональных свойств эритроцитов может приводить к повышению сдвиговых напряжений потока крови и росту сосудистого сопротивления [3, 5, 10].
При анализе характера изменений показателей свертывающей, противосвертывающей систем и фибринолиза в нашем исследовании установлено, что активность AT III, ПС, содержание ФГ, Д-димера, ФАЭФ, РКФМ, ингибитора активатора плазминогена (PAI-1) статистически значимо не отличались от нормальных величин.
Функциональные пробы, выполненные у больных пожилого возраста с дисциркуляторной энцефалопатией, позволили выявить недостаточность антиагрегационной активности эндотелия, что проявлялось парадоксальным проагрегантным ответом тромбоцитов при проведении МП (табл. 1), в то время как физиологической реакцией на функциональные (нагрузочные) пробы должно быть снижение исходной активности тромбоцитов.

Оценка антикоагулянтного резерва сосудистого эндотелия также выявила, в отличие от здоровых лиц, снижение уровня AT III, ПС в ответ на МП (табл. 2).
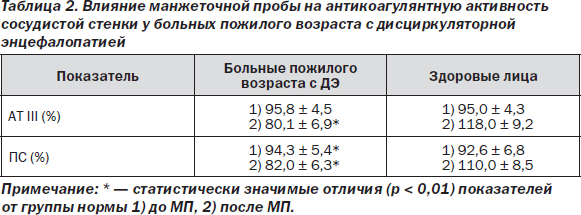
При рассмотрении фибринолитического потенциала эндотелия у пожилых больных с дисциркуляторной энцефалопатией выявлялась адекватная по направленности и выраженности реакция увеличения ФАЭФ наряду с ростом концентрации tpA в ответ на МП, что свидетельствовало о сохранности этого звена атромбогенности (табл. 3).
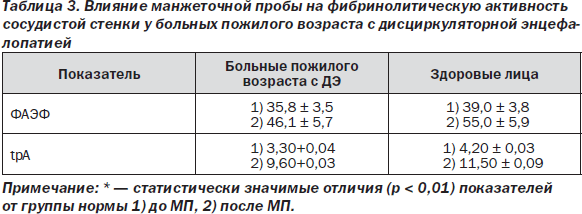
Таким образом, у больных пожилого возраста с дисциркуляторной энцефалопатией определенная сбалансированность системы гемостаза в условиях снижения антиагрегационного и антикоагуляционного резерва сосудистой стенки обеспечивается сохранностью эндотелиальных мобилизационных резервов фибринолиза, что является основой адекватной церебральной гемоперфузии и жизнедеятельности пожилого человека в целом.
Выводы
1. У больных пожилого возраста с дисциркуляторной энцефалопатией имеет место повышение основных гемореологических детерминант — ВК и АЭ.
2. У больных пожилого возраста с дисциркуляторной энцефалопатией выявлено снижение атромбогенной активности сосудистой стенки. Дефицит антикоагулянтных свойств сосудистой стенки связан со снижением активности AT III и ПС, продуцируемых ею в ответ на МП.
3. У больных пожилого возраста с дисциркуляторной энцефалопатией антиагрегационная и антикоагулянтная недостаточность сосудистой стенки компенсируется высокой реактивностью ее фибринолитического потенциала.
1. Верещагин Н.В., Моргунов В.А., Гулевская Т.С. Патология головного мозга при атеросклерозе и артериальной гипертонии. — М.: Медицина, 1997.
2. Ильинская О.П. Старение эндотелия сосудов человека и атеросклероз // Клиническая геронтология. — 2002. — № 6. — С. 51-54.
3. Сторожаков Г.И., Верещагина Г.С., Малышева Н.В. Эндотелиальная дисфункция при артериальной гипертонии у пациентов пожилого возраста // Клиническая геронтология. — 2003. — № 1. — С. 23-28.
4. Суслина З.А., Танашян М.М. Антитромботическая терапия в ангионеврологии. — М.: Медицинская книга, 2004.
5. Takada A., Urano Т., Takada Y. Stress and hemostasis. — Recent progress in blood coagulation and fibrinolysis // International Congress series 1129. — Exepta Medica, 1997. — P. 213-221.
