Газета «Новости медицины и фармации» 11-12(331-332) 2010
Вернуться к номеру
Контрацепція
Авторы: Донна Шауп і Деніел Р. Мішель-мол. Університет Південної Каліфорнії, Лос-Анджелес (штат Каліфорнія)
Версия для печати
Продовження. Початок у № 10 (326)
Хоч усі нові міні-пілі зі зменшеною дозою активних речовин позитивно впливають на вугри й жирну шкіру, декотрі прогестини мають андрогенний ефект. Спостерігаються такі андрогенні побічні явища, пов''язані з прогестинним компонентом препарату, як збільшення апетиту й маси тіла, вугри, жирна шкіра [41], негативний вплив на ліпідний обмін, діабетогенний ефект, сверблячка, депресія, зміни настрою, підвищена збудливість, виснаження й втома [36]. Нові прогестини, а також комбіновані препарати з малою дозою прогестину дають змогу мінімізувати ці андрогенні ефекти.
Обидва компоненти пероральних контрацептивів — естрогени й прогестини — можуть спричинити появу таких проблем, як підвищений кров''яний тиск, головний біль, болючість молочних залоз. Якщо в період після припинення прийому препарату не виникає менструальноподібна кровотеча або спостерігається аменорея, це зумовлюється домінуванням у його складі прогестинів і може бути усунено з переходом на прийом контрацептивів зі збільшеним умістом естрогенів.
А. Вплив на печінкові білки: глобулін, що зв''язує статеві гормони, і зміни здатності крові зсідатися. Основний вплив андрогенних прогестинів на печінку полягає в дозозалежному пригніченні синтезу глобуліну, що зв''язує статеві гормони (ГЗСГ). Оскільки естрогени підвищують концентрацію ГЗСГ, вимірювання її являє собою надійний спосіб визначення відносного балансу між естрогенами й андрогенами, що входять до складу препарату (рис. 5).
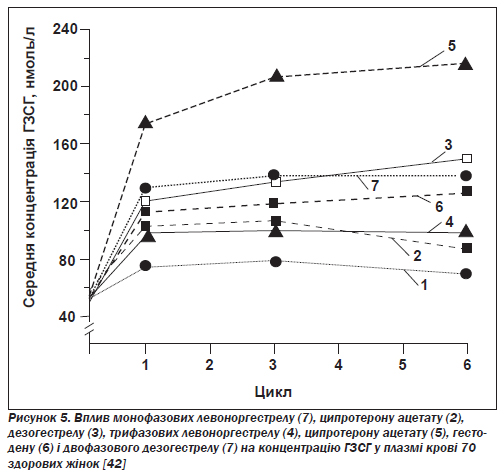
Найбільше підвищення концентрації ГЗСГ спостерігалося під час вживання комбінованих пігулок із дезогестрелом, гестоденом, ципротерону ацетатом [42], норгестиматом; це дає підстави вважати, що ці препарати найефективніші для лікування жінок із симптомами гіперандрогенізму, такими як вугри, гірсутизм або ожиріння андроїдного типу.
Синтетичні естрогени в пероральних контрацептивах, потрапляючи в організм через ротову порожнину, викликають дозозалежне посилення внутрішньопечінкового синтезу білків. Збільшення кількості цих білків, що спричиняє підвищення коагуляційної активності (фактори V, VIII, X системи зсідання крові й фібриноген), підраховують за змінами в концентрації факторів, що посилюють антитромботичну активність [43] (рис. 6).

Найсерйозніші ускладнення, яких зазнають користувачки пероральних контрацептивів, пов''язані з хворобами, що перебігають з розладами кровообігу, зумовленими змінами зсідання крові. Серцево-судинні хвороби найчастіше виникають під час приймання таких препаратів у тих жінок, які курять, мають надмірну масу тіла, страждають на діабет, гіпертонію або старші від 50 років. За даними епідеміологічних досліджень, частота випадків як артеріального, так і венозного тромбозу безпосередньо пов''язана з дозою естрогену (табл. 4) [45а].
Ризик виникнення серйозних серцево-судинних захворювань при користуванні новими пігулками з малою дозою невисокий. Частота госпіталізацій із приводу серйозних серцево-судинних захворювань, що пов''язані з уживанням комбінованих пероральних контрацептивів зі зменшеною дозою (або яких не було уникнуто, незважаючи на прийом цих препаратів), характеризується такими показниками: один інфаркт міокарда, три інсульти й 11 випадків тромбозу або емболії вен на 100 тис. користувачок цих засобів [46].
Базовий показник частоти випадків тромбозу/емболії вен серед невагітних жінок репродуктивного віку, які не вживають пероральних контрацептивів, становить 0,8 на 10 тис. жінко-років. Аналогічний показник серед користувачок пероральних контрацептивів, що містять 20–50 мкг етинілестрадіолу, за даними широкомасштабного обсерваційного дослідження, дорівнює трьом. Це майже в чотири рази вище від базового показника, однак удвічі нижче показника 6 на 10 тис. жінко-років, пов''язаного з вагітністю [47]. Жінки зі спадковими розладами зсідання крові (наприклад, із недостатністю білків С та S, фактора Ляйдена, антитромбіну III чи з резистентністю до активованого білка С) належать до групи високого ризику. Одне з досліджень показало, що загальний ризик розвитку тромбозу в користувачок пероральних контрацептивів збільшився від базового показника 6 до 30 на 10 тис. жінко-років [48]. Жінок з родинним або особистим анамнезом, обтяженим випадками тромбозу, рекомендується піддавати скринінговому обстеженню на виявлення цих дефіцитарних розладів зсідання крові.
Чотири обсерваційних дослідження показали, що ризик тромбозу/емболії вен у користувачок пероральних контрацептивів третього покоління зріс порівняно з аналогічним показником, пов''язаним із вживанням препаратів другого покоління. Хоча ці висновки викликали стурбованість, подані результати стосовно тривалості користування були суперечливі; до того ж при вживанні пероральних контрацептивів третього покоління порівняно з другим спостерігалося значно нижче відношення шансів (ВШ) щодо інфаркту міокарда. Після того як дані транснаціонального дослідження повторно проаналізували з урахуванням тривалості вживання пероральних контрацептивів кожного типу, виявилося, що ризик тромбозу/емболії вен для жінок, які вперше приймали препарати третього покоління, залежить від тривалості приймання попередніх контрацептивів і що він практично ідентичний для пігулок другого і третього покоління (табл. 5).
Б. Вуглеводний обмін. У жінок, які вживають сучасні пероральні контра цептиви зі зменшеною дозою активних речовин, не виявлено клінічно значущих змін вуглеводного обміну, хоча давніші пігулки з великою дозою справляли значний вплив на концентрацію глюкози й інсуліну. Дані щодо впливу естрогенного компонента суперечливі, однак найімовірніше, що він діє синергічно з прогестином, погіршуючи толерантність до глюкози [49]. Загалом чим вищі доза й активність прогестину, тим більшою мірою порушуються процеси метаболізму глюкози. Завдяки тому, що препарати з низькою дозою не справляють істотного впливу на концентрацію глюкози, інсуліну та глюкагону, ними можуть без особливого ризику користуватися жінки з анамнезом гестаційного діабету [50] і багато хто з інсулінозалежних хворих на діабет. Дослідження з вивчення стану здоров''я медичних сестер показало, що хоча діабет типу 2 розвився в понад 2000 жінок, ризик серед користувачок сучасних пероральних контрацептивів не зріс (RR = 0,86, 95% ІН 0,46–1,61) [51].
В. Ліпіди й довготерміновий ризик атеросклерозу. Естрогени, що входять до складу пероральних контрацептивів, підвищують концентрацію ліпопротеїдів високої щільності, загального холестерину й тригліцеридів, знижуючи концентрацію ліпопротеїдів низької щільності. Прогестинний компонент, навпаки, сприяє зниженню концентрації ліпопротеїдів високої щільності, загального холестерину й тригліцеридів, підвищуючи концентрацію ліпопротеїдів низької щільності. Більш ранні препарати, у складі яких домінував прогестин, мали загалом негативний вплив на ліпідний обмін, тоді як сучасні засоби з низькою дозою цього компонента, за наявними даними, не спричиняють значних змін концентрацій ліпопротеїдів високої і низької щільності та загального холестерину (хоча концентрація тригліцеридів підвищується). Препарати з високим відношенням кількості естрогену до кількості прогестину (тобто такі, що містять не більше ніж 0,5 мг норетиндрону або нових прогестинів) підвищують концентрацію ліпопротеїдів високої щільності та тригліцеридів, знижуючи концентрацію ліпопротеїдів низької щільності (рис. 7) [52, 53, 53а].
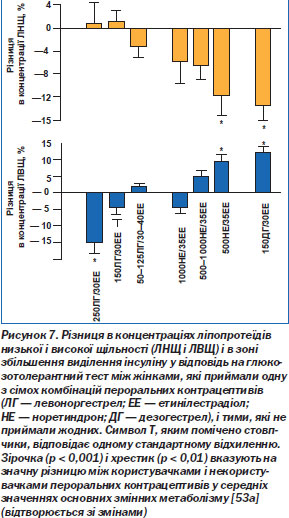
Незважаючи на певні зміни концентрації ліпідів, у жінок, які в минулому користувалися пероральними контрацептивами старого чи нового типу, не спостерігається підвищення ризику розвитку атеросклерозу [54, 55]. Нагромаджується дедалі більше даних, які, по суті, свідчать про те, що пероральні контрацептиви мають довготерміновий захисний ефект щодо захворювань судин [56], хоча існує короткотерміновий ризик виникнення тромбозу, пов''язаний із поточним вживанням пероральних контрацептивів. Результати ангіографічного обстеження молодих жінок, у яких було діагностовано інфаркт міокарда, підтверджують, що в тих з них, які в поточному періоді вживають пероральні контрацептиви, інфаркт частіше зумовлюється тромбозом, а не атеросклерозом: коронарний атеросклероз було виявлено в 79 % пацієнток, що не користуються цими препаратами, і тільки в 36 % жінок, котрі приймають їх [57]. Ці дані підтримують наявність швидше довготермінового захисного впливу, ніж підвищеного ризику.
Г. Вплив на виникнення новоутворень
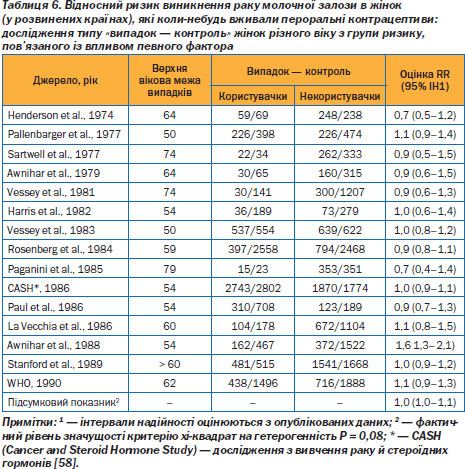
Ризик раку молочної залози. Оскільки естрогени стимулюють ріст тканини молочної залози, виникає занепокоєність стосовно ймовірності того, що пероральні контрацептиви можуть або викликати рак цього органа в користувачок, або активізувати розвиток злоякісного процесу. Всебічний науковий аналіз даних усіх опублікованих епідеміологічних досліджень, проведений у 1991 році, показав, що підсумковий показник відносного ризику в жінок, які вживають ці препарати, становить 1,0 (95% ІН 1,0–1,1) (табл. 6) [58].
Відносний ризик раку молочної залози в користувачок пер оральних контрацептивів із родинним анамнезом цього захворювання і без нього вивчався у вісьмох дослідженнях типу «випадок — контроль» і одному когортному. Жодне з них не виявило значущої різниці в жодній з цих категорій [36].
У 1996 році міжнародна група повторно проаналізувала весь масив епідеміологічних даних глобального масштабу стосовно пероральних контрацептивів і раку молочної залози [59]. Аналіз виконувався на матеріалах 54 досліджень, проведених у 25 країнах із охопленням понад 53 тис. хворих на рак молочної залози і понад 100 тис. контрольних пацієнток. У жінок, які вживали пероральні контрацептиви, спостерігався трохи підвищений ризик розвитку цієї форми раку (RR = 1,24, 95% ІН 1,15–1,33) [59], який неухильно зменшувався після припинення прийому препаратів і через десять років після цього не перевищував 1,01 (95% ІН 0,96–1,05). Цікаво, що порівняно з іншими жінками, в яких було діагностовано рак молочної залози, у користувачок пероральних контрацептивів він виявлявся на більш ранній стадії клінічного розвитку. Ризик наявності раку, що поширився за межі молочної залози, порівняно з пухлиною, локалізованою в її межах, у жінок, які в поточному періоді вживають ці препарати, значно нижчий (RR = 0,88, 95% ІН 0,81–0,95), ніж у тих, котрі ними не користуються.
Загалом більшість даних стосовно пероральних контрацептивів має заспокійливий характер. Імовірно, що протизаплідні стероїди активізують ріст вже наявної злоякісної пухлини й одночасно підвищують шанси на її ранню діагностику, таким чином уникаючи звичайної ситуації, коли проходить багато років, поки рак молочної залози виявляється клінічно. На підставі результатів досліджень рекомендується застосовувати пер оральні контрацептиви з найменшою дозою активних речовин.
Рак шийки матки. Епідеміологічні дані щодо ризику виникнення інвазивного раку шийки матки в користувачок пероральних контрацептивів суперечливі. Результати деяких досліджень можуть пояснюватись впливом факторів, що втручаються, таких як кількість сексуальних партнерів, вік на момент першого статевого контакту, інфікування вірусом папіломи людини, використання бар''єрних контрацептивів і сперміцидів, тютюнокуріння, частота цитологічних досліджень. Шлесельман у своєму огляді за матеріалами 14 досліджень, що охоплювали понад 3800 жінок з інвазивним раком шийки матки, доходить висновку про значне підвищення ризику зі збільшенням тривалості вживання пероральних контрацептивів (рис. 8) [60].
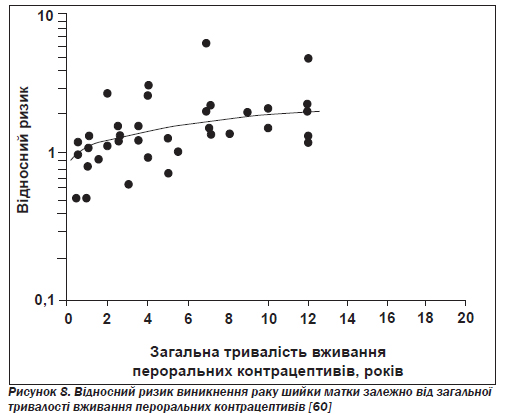
У публікаціях за даними інших досліджень повідомляється, що внаслідок довготермінового вживання ризик підвищується в 1,5–2,5 раза [61, 62]. На відміну від цих даних деякі добре контрольовані дослідження не виявили змін щодо ризику виникнення внутрішньоепітеліальної неоплазії шийки матки, пов''язаних із використанням пероральних контра цептивів [61, 63]. У статті за результатами популяційного дослідження типу «випадок — контроль» стверджувалося, що пероральні контрацептиви й тютюнокуріння впливають на здатність вірусу папіломи людини викликати інвазивний рак шийки матки [64]. Автори припускають, що вживання пероральних контрацептивів може відігравати значну роль в етіології інвазивних сквамозноклітинних пухлин шийки матки тільки тоді, коли ці препарати вживаються в критичний період розвитку жіночого репродуктивного тракту, тобто у віці до 17 років.
Рак ендометрію. Тринадцять із п''ятнадцятьох досліджень (типу «випадок — контроль» і когортних) показали, що пероральні контрацептиви захищають від раку ендометрію — третього за поширеністю різновиду раку серед жінок у США [65]. Жінки, які вживали такі препарати хоча б один рік, мали на 50 % менший ризик розвитку раку ендометрію у віці від 40 до 55 років порівняно з тими жінками, котрі ними не користувалися. Виявлено значущу тенденцію зменшення ризику зі збільшенням тривалості використання комбінованих контрацептивів (рис. 9) [60].
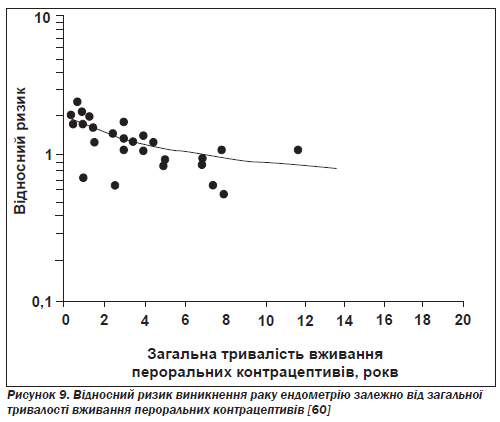
Найвищий захисний ефект спостерігався в жінок, які не народжували, причому він забезпечувався при використанні комбінованих препаратів як з великою, так і з малою дозою прогестину [66].
Рак яєчника. Як відзначено у вісімнадцятьох із двадцятьох публікацій за матеріалами відповідних досліджень, серед користувачок пероральних контрацептивів зменшується ризик виникнення раку яєчника, особливо його найпоширенішого різновиду — епітеліального раку яєчника (рис. 10) [67].
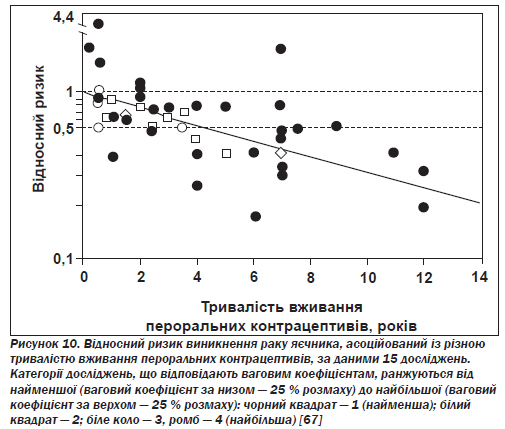
Підсумковий (отриманий на базі сукупних даних) показник відносного ризику розвитку раку яєчника серед жінок, які коли-небудь вживали ці препарати, становить 0,64, тобто зниження дорівнює 36 %. Пероральні контрацептиви знижують ризик виникнення чотирьох основних гістологічних типів епітеліального раку яєчника (серозного, мукозного, ендометріоїдного й паренхіматозноклітинного), а також як інвазивного раку яєчника, так і форм із низьким потенціалом злоякісного росту. Ступінь зниження ризику безпосередньо пов''язаний з тривалістю вживання препаратів і коливається від 40 % після чотирьох років до 53 % після восьми і до 60 % після дванадцяти років. Захисний ефект починає проявлятися в межах десятьох років від початку вживання пероральних контрацептивів і зберігається принаймні протягом 20 років після припинення прийому. При використанні монофазових препаратів з низькою дозою активних речовин та інших контрацептивів з вищою дозою спостерігається приблизно однаковий захисний ефект [68]. Як і в разі раку ендометрію, такий ефект виявляється лише в жінок, які народжували не більше ніж від одного до чотирьох разів, — тобто в тих, які належать до групи найвищого ризику щодо цього типу раку.
Гепатоаденома і рак печінки. У рідкісних випадках спостерігається розвиток доброякісної гепатоцелюлярної аденоми, пов''язаний із довготривалим вживанням пероральних контрацептивів із великою дозою активних речовин (особливо це стосується препаратів, що містять местранол). У публікації за матеріалами двох досліджень, проведених у Великобританії, повідомлялося про підвищений ризик раку печінки серед користувачок пероральних контра цептивів, однак значущість цих результатів знижується через невелику чисельність охоплених пацієнток і значну кількість сторонніх факторів, що втручаються [69]. Широкомасштабне багатоцентрове епідеміологічне дослідження, координоване ВООЗ, не виявило зростання ризику виникнення раку печінки навіть зі збільшенням тривалості вживання таких препаратів [70].
Аденома гіпофіза. Пероральні контрацептиви маскують симптоми пролактиноми, а саме аменорею й галакторею. Коли приймання препаратів переривається, ці симптоми проявляються, що наводить на думку про наявність причинного зв''язку. Однак дані трьох досліджень свідчать про те, що захворюваність на аденому гіпофіза серед користувачок протизаплідних пігулок не вища від спостережуваної серед контрольних пацієнток, дібраних за принципом парності [71].
Злоякісна меланома. Кілька епідеміологічних досліджень з вивчення зв''язку між вживанням пероральних контрацептивів і розвитком злоякісної меланоми дали неоднозначні результати. Автори публікації за матеріалами дослідження щодо пер оральних контрацептивів, здійсненого Королівським коледжем лікарів загальної практики (Великобританія), і дослідження, проведеного в Оксфорді Асоціацією планування родини (з охопленням понад 450 тис. жінко-років спостереження), дійшли висновку, що вживання пероральних контрацептивів, найімовірніше, не асоціюється зі зростанням ризику виникнення меланоми [72].
5. Протипоказання щодо використання пероральних контрацептивів
Призначати пероральні контра цептиви більшості жінок репродуктивного віку цілком безпечно. До абсолютних протипоказань належить анамнез тромбоемболії, атеросклерозу, інсульту чи будь-якого системного захворювання, пов''язаного з ураженням судин (вовчак, діабет із ретинопатією, нефропатія та тощо). У перелік протипоказань входять також куріння у віці понад 35 років, неконтрольована гіпертонія, вагітність, макроаденома гіпофіза, мігреневий головний біль із локалізованими ознаками, гостра хвороба печінки, рак молочної залози або ендометрію. Не слід призначати пер оральні контрацептиви й жінкам з функціональними серцевими захворюваннями, оскільки в таких випадках затримка рідини в організмі може призвести до серцевої недостатності. Відносним протипоказанням є підвищений кров''яний тиск у літніх або повних жінок.
Не є протипоказаннями асимптоматичне пролабування стулок мітрального клапана серця, вік за 40 років, перенесена в минулому хвороба печінки, випадки раку молочної залози в родинному анамнезі, контрольований діабет, пролактинсекретуюча мікроаденома гіпофіза. Користування пероральними контра цептивами слід припинити, якщо на тлі їх вживання в жінки виникає сильний головний біль, непритомність, тимчасова втрата зору чи мови, парестезії.
6. Взаємодія з іншими препаратами
Деякі лікарські засоби, такі як барбітурати, сульфаніламіди, циклофосфан і рифампіцин, перешкоджають дії пероральних контрацептивів, стимулюючи ферменти печінки, що перетворюють відповідні стероїди на більш полярні й менш біологічно активні метаболіти. У жінок, які приймають ці ліки, може спостерігатися більша частота невдач у запобіганні вагітності. Клінічні дані щодо показників невдач під час лікування певними антибіотиками (зокрема, пеніциліном, ампіциліном і тетрацикліном), сульфаніламідами, анальгетиками й барбітуратами (наприклад, фенітоїном) суперечливі.
7. Користь для здоров''я, не пов''язана з контрацепцією
На додаток до того, що пероральні контрацептиви являють собою один з найефективніших засобів конт рацепції, вони ще й справляють позитивну дію на здоров''я жінки в багатьох його аспектах.
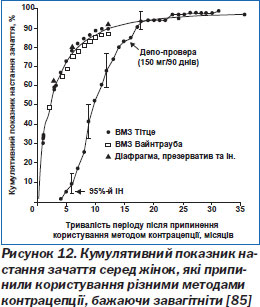
А. Вплив на репродуктивну функцію. Пероральні контрацептиви мають довготривалий сприятливий вплив на фертильність, зменшуючи ризик сальпінгіту, позаматкової вагітності, формування кісти яєчника. Однак вони також дають короткотривалий негативний ефект, пов''язаний із періодом затримки (більшим чи меншим) відновлення овуляції після припинення їх прийому: протягом двох років після цього фертильність залишається нижчою порівняно зі спостережуваною після припинення користування бар''єрними засобами контрацепції (рис. 11) [73, 74].
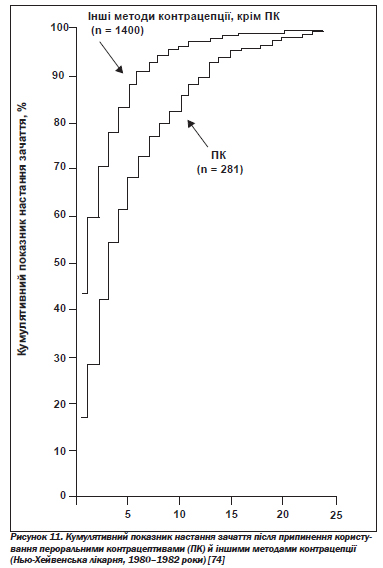
Естроген справляє проліферативну дію на тканини молочної залози, що містять естрогенні рецептори. Припускають, що прогестини пригнічують синтез цих рецепторів у залозі, таким чином справляючи на неї антиестрогенну дію. Кілька досліджень показали, що пероральні контрацептиви знижують частоту виникнення доброякісних пухлин молочної залози, причому цей ефект безпосередньо пов''язаний із кількістю прогестину. За даними досліджень, серед жінок, які в поточному періоді вживають пероральні контра цептиви, спостерігається 85% зменшення частоти випадків фіброаденоми й 50% — хронічного полікістозу й пухлин молочної залози (не перевірених біопсією) порівняно з тими жінками, котрі не використовують цих препаратів [75].
В. Користь від пригнічення овуляції. Такі розлади, як дисменорея, передменструальне напруження, рідше виникають в ановуляційних циклах. Серед тих користувачок, які раніше страждали від дисменореї, тільки приблизно 30 % повідомляють про відсутність покращення після того, як вони почали приймати пероральні контрацептиви [76]. Комбіновані пероральні контрацептиви зі зменшеною дозою активних речовин фактично усувають у більшості жінок циклічні симптоми передменструального синдрому [77]. Пригнічення овуляції зменшує ймовірність розвитку функціональних кіст (табл. 7) [78];
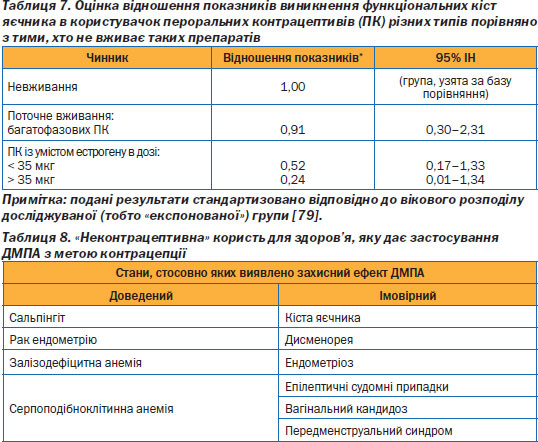
на тлі прийому пероральних контрацептивів частота виникнення таких кіст знижується на 80–90 % [75]. Багатофазові препарати також мають подібний захисний ефект, хоча й менш виражений. Інші розлади, пов''язані з постійною овуляцією, рак яєчника також значно рідше трапляються в користувачок пероральних контрацептивів.
Г. Інші переваги. Кілька досліджень, проведених в Європі, показали, що ризик розвитку ревматоїдного артриту в користувачок пероральних контрацептивів удвічі менше, ніж у контрольній групі [79], хоча інші розвідки не виявили такого захисного ефекту [80]. Ще одна перевага — захисний ефект щодо сальпінгітів: ризик зменшується на 50 %, що може пояснюватися скороченням тривалості менструальної кровотечі або згущенням цервікального слизу, який перешкоджає проникненню збудників інфекції у верхні статеві шляхи. У жінок, які вживають пероральні контрацептиви в поточному періоді, більше ніж на 90 % знижується ризик позаматкової вагітності [41]. За даними кількох досліджень, ці препарати уповільнюють процес зниження щільності кісток у перименопаузі [81] (особливо в жінок із олігоменореєю), зменшують ризик виникнення фіброміом [82] і поліпшують контроль над кровотечею [83].
Ґ. Ін''єкційні протизаплідні засоби тривалої дії
Оскільки більшість ін''єкційних стероїдних препаратів пролонгованої дії містять тільки прогестин без естрогену, ендометрій не підтримується й маткова кровотеча виникає нерегулярно, з непрогнозованими інтервалами. Упроваджено три типи ін''єкційних стероїдів: депо-препарати медроксипрогестерону ацетату (ДМПА); енантат норетиндрону; кілька комбінованих препаратів (з умістом прогестину й естрогену), що вводять один раз на місяць. Ін''єкційні протизаплідні засоби — популярний метод контрацепції в усьому світі, хоч у США офіціально затверджено для використання тільки ДМПА.
1. Депо-препарати медроксипрогестерону ацетату
ДМПА являє собою 17-ацетоксипрогестерон, тобто це єдиний із прогестинів, використовуваних для цілей контрацепції, який не є похідним від 19-нортестостерону. Ацетоксипрогестинам, структурно пов''язаним з прогестероном, не властива андрогенна активність. Медроксипрогестерону ацетат широко використовувався в складі пер оральних контрацептивів доти, доки це не було заборонено в США після експериментів, які показали, що він підвищує ризик раку молочної залози в собак породи бігль (коротконога гонча). Згодом виявилося, що через певні особливості метаболізму в організмі цих тварин 17-ацетоксипрогестини перетворюються на естроген, стимулюючи гіперплазію молочних залоз. В організмі людини ДМПА не зазнає подібних перетворень. У 1992 році, після того як відповідні епідеміологічні дослідження довели, що ДМПА не підвищує ризик раку молочної залози в жінок, Управління США з санітарного нагляду за якістю харчових продуктів і ліків дозволило використовувати цей препарат як протизаплідний засіб.
У широкомасштабному випробуванні, проведеному ВООЗ, частота випадків вагітності на першому році вживання ДМПА становила лише 0,1 %, а кумулятивний показник за два роки не перевищував 0,4 %.
Основний механізм дії медроксипрогестерону ацетату полягає в пригніченні овуляції; на додаток до цього під його впливом слизова оболонка матки тоншає, що перешкоджає імплантації ембріона. Крім того, ДМПА викликає згущення й підвищення в''язкості цервікального слизу, таким чином зводячи до мінімуму імовірність досягнення сперматозоїдами фаллопієвих труб.
А. Фармакокінетика. У великому колі кровообігу ДМПА виявляється через 30 хвилин після ін''єкції; протягом 24 годин його концентрація в крові неухильно підвищується до ефективного рівня (більше 0,5 нг/мл). Потім упродовж трьох місяців вона підтримується на постійному рівні 1,0–1,5 нг/мл, а на п''ятому місяці знижується приблизно до 0,2 нг/мл. Нерідко препарат можна виявити в крові протягом сімох, іноді навіть дев''ятьох місяців. Концентрація естрадіолу протягом перших чотирьох місяців залишається нижчою від 100 пг/мл. Фолікулярна активність відновлюється на 2–3 місяці раніше, ніж лютеїнова. У декотрих користувачок ДМПА овуляція може не відновлюватися протягом сімох-дев''ятьох місяців, поки концентрація медроксипрогестерону ацетату не зменшиться до рівня нижче 0,01 нг/мл.
Б. Пригнічення овуляції. Мішель зі співавт. у своїй публікації повідомляють, що протягом перших двох місяців після ін''єкції, хоча пік екскреції ЛГ і ФСГ у середині циклу гальмується, секреція цих гормонів усе ще відбувається в пульсуючому ритмі [84]. Упродовж цього проміжку часу в жінок, які використовували ДМПА протягом чотирьох-п''яти років, концентрація естрадіолу коливається від 5 до 100 пг/мл (у середньому — 42 пг/мл), але жодна з них не скаржилася на симптоми, пов''язані з гіпоестрогенним станом.
В. Відновлення фертильності. Ос кіль ки для виведення ДМПА з системи кровообігу потрібен певний час, відновлення овуляції може затриматися навіть на рік з моменту останньої ін''єкції. Після цієї затримки повертається нормальна здатність до зачаття (рис. 12) [85].
Тривалість інтервалу між припиненням вживання препарату й відновленням фертильності не залежить від кількості ін''єкцій, але збільшується з підвищенням маси тіла жінок — найімовірніше, через те, що медроксипрогестерону ацетат абсорбується жировими тканинами, звідки він виводиться повільніше.
Г. Зміни ендометрію. Біопсія ендометрію, зразки тканини для якої відбиралися з інтервалом в 1,5; 3; 6; 9 і 12 місяців після першої ін''єкції ДМПА в групі жінок, які отримували цей препарат один раз у три місяці, показала, що протягом шістьох тижнів приблизно в половині зразків тканина була проліферативною. Після другої ін''єкції проліферативними були менше ніж 10 % біопсій. Більшість зразків визначалися як неактивний тип ендометрію, а після року прийому ДМПА приблизно 40 % характеризувались як атрофічні.
Ґ. Побічні явища
Клінічні прояви. Найголовніший побічний ефект ДМПА — цілковите порушення менструального циклу. Упродовж трьох місяців після першої ін''єкції приблизно в 30 % жінок спостерігалася аменорея, а в інших 30 % — нерегулярні кровотечі й кров''янисті виділення в міжменструальному періоді, які тривали понад 11 днів на місяць. Кровотеча звичайно була незначною й не викликала анемії. Наприкінці другого року користування ДМПА аменорея розвинулася приблизно в 70 % жінок [86]. Після припинення прийому ДМПА через шість місяців регулярні цикли відновилися майже в половини жінок, а до закінчення року з моменту останньої ін''єкції — у трьох чвертей.
За даними п''ятьох одномоментних поперечних досліджень, у жінок, які вживали ДМПА, маса тіла була більша, ніж у тих, що не користувалися гормональними контрацептивами [36]. Кілька лонгітудинальних (поздовжніх) досліджень показали, що користувачки ДМПА набирають від 1,5 до 4 кг маси тіла на рік [87]; цей показник вищий від типового показника збільшення ваги, що становить близько 1 кг на рік.
В інструкції, що додається до препарату, серед побічних явищ ДМПА перелічуються також депресія й зміни настрою. Однак за даними кількох досліджень частота випадків цих розладів не досягає й 5 %. Для з''ясування питання щодо наявності причинного зв''язку між користуванням ДМПА й розвитком депресії не провадилося жодних клінічних випробувань із застосуванням групи порівняння. Головний біль, за багатьма повідомленнями, є найчастішим ускладненням медичного характеру й найпоширенішою причиною припинення вживання ДМПА, однак знов-таки не було жодного компаративного дослідження, яке б засвідчило, що ці препарати підвищують частоту виникнення або ступінь тяжкості головного болю напруження чи мігреневого болю.
Вплив на метаболізм. Оскільки ДМПА не активізує вироблення глобулінів печінки, на тлі його вживання не спостерігається змін у факторах системи згортання крові чи в концентрації ангіотензиногенів. Ці препарати також не пов''язують із підвищенням кров''яного тиску або з випадками тромбоемболії. У результаті дослідження, проведеного ВООЗ, було відзначено, що після двох років ін''єкцій показники кров''яного тиску в користувачок ДМПА не змінилися [88].
Середні значення концентрації тригліцеридів і загального холестерину під час використання ДМПА не змінюються (або спостерігаються лише незначні зміни). У всіх сімох дослідженнях, в яких визначали концентрацію ліпопротеїдів високої щільності, цей показник був нижчий у тих жінок, котрі користувалися ДМПА. Три з п''ятьох досліджень, у ході яких вимірювалася концентрація ліпопротеїдів низької щільності, показали її підвищення в користувачок ДМПА [36]. Жодне з досліджень не виявило збільшення частоти випадків серцево-судинних хвороб серед жінок, які протягом тривалого часу вживали ДМПА (у поточному періоді або в минулому), а також немає даних, які б підтверджували, що ДМПА пришвидшує розвиток атеросклерозу.
Остеопороз. В одномоментному поперечному дослідженні, де було застосовано метод сканування кісток DEXA, у 30 жінок, які протягом тривалого часу користувались ДМПА, виявилося зниження щільності кісток у поперековому відділі хребта, а також стегнових кісток порівняно з 30 жінками, які не користувалися цими препаратами [89]. Катамнестичне спостереження показало, що після припинення прийому ДМПА щільність кісток повертається до норми [89]. Ці дані дають підставу припускати, що зниження щільності кісток під час користування ДМПА можна звести до мінімуму (або уникнути цього зовсім) за умови достатнього вживання кальцію. Інші довготривалі дослідження не виявили зменшення щільності кісток у користувачок ДМПА, і досі жодне дослідження не продемонструвало зростання ризику переломів кісток у жінок, які користувалися чи користуються ним [36].
Ризик виникнення раку. Протягом багатьох років відповідні органи не давали дозволу на використання ДМПА для цілей контрацепції в США, оскільки існували побоювання щодо можливого підвищення ризику раку шийки матки, молочної залози й ендометрію. Результати двох широкомасштабних досліджень типу «випадок — контроль» показали, що серед користувачок ДМПА не спостерігається підвищення відносного ризику раку молочної залози [90, 91]. У жінок, що вживали ці препарати понад п''ять або понад чотирнадцять років тому, такий ризик теж не зріс (відповідно RR = 1,0, 95% ІН 0,7–1,5 і RR = 0,89, 95% ІН 0,63–1,3). Однак серед жінок до 35 років, які почали користуватися ДМПА в останні п''ять років, було помічено значне зростання ризику раку молочної залози (RR = 2,0, 95% ІН 1,5–2,8), порівнянне зі спостережуваним серед користувачок пероральних контрацептивів. Загалом ДМПА, судячи з наявних даних, не впливає на частоту випадків розвитку раку молочної залози.
Дослідження типу «випадок — контроль», проведене ВООЗ, виявило серед користувачок ДМПА значно знижений ризик виникнення раку ендометрію (RR = 0,21, 95% ІН 0,06–0,79), причому цей ефект зберігається щонайменше протягом восьми років після припинення вживання препаратів [92].
Ризик розвитку раку яєчника серед користувачок ДМПА, згідно з результатами дослідження ВООЗ типу «випадок — контроль», практично не змінюється (RR = 1,1, 95% ІН 0,6–1,8) [93]. Ці дані не демонструють захисного ефекту, подібного до виявленого серед користувачок пероральних контрацептивів, хоча препарати обох типів пригнічують овуляцію. Відсутність захисного ефекту, спостережувана при використанні ДМПА, може пояснюватись тим, що в країнах, де здійснювалося дослідження, ці контрацептиви застосовували тільки до жінок, які неодноразово народжували (а отже, належать до групи з низьким ризиком розвитку епітеліального раку яєчника).
Значного зростання ризику розвитку інвазивного раку шийки матки, за даними кількох широкомасштабних досліджень типу «випадок — контроль», не спостерігається (RR = 1,1, 95% ІН 1,0–1,3) — ні при короткочасному, ні при тривалому використанні ДМПА. Згідно з результатами дослідження ВООЗ, загальний ризик розвитку раку in situ в користувачок ДМПА трохи підвищується (RR = 1,4, 95% ІН 1,2–1,7), однак такої тенденції не виявлено в одній з охоплених країн — Коста-Риці (RR = 1,0, 95% ІН 0,6–1,8) [94], а також у Новій Зеландії (за даними двох досліджень, проведених у цій країні) [95, 96].
Д. Користь для здоров''я, не пов''язана з контрацепцією. Існують переконливі епідеміологічні дані, які свідчать про те, що користування ДМПА зменшує ризик розвитку залізодефіцитної анемії, ЗТО та раку ендометрію й позитивно впливає на стан жінок із серпоподібноклітинною анемією (табл. 8).
Є підстави припускати, що ці препарати також знижують частоту судомних припадків у жінок, хворих на епілепсію, і частоту виникнення первинної дисменореї, функціональних кіст яєчника, болю під час овуляції. Крім того, вони пом''якшують симптоми ендометріозу, а згідно з результатами двох невеликих досліджень сприяють зниженню захворюваності на вагінальний кандидоз [36].
2. Норетиндрону енантат (Нет-Ен)
Норетиндрону енантат — ін''єкційний прогестинний препарат, дозволений для використання як протизаплідний засіб у понад 40 країнах, до яких, однак, не належать США. Через менш тривалу дію рекомендовано вводити Нет-Ен (200 мг у маслянистій суспензії) кожні 60 днів принаймні в перші шість місяців використання, а відтак — не рідше ніж один раз у 12 тижнів.
3. Прогестино-естрогенний ін''єкцій ний препарат (для щомісячного введення)
З огляду на те що в користувачок засобів, що містять тільки прогестин, часто виникали проблеми, пов''язані з кровотечею, було розроблено кілька комбінованих ін''єкційних препаратів складного ефіру прогестину-естрадіолу. Вони призначені для введення один раз на місяць і часто асоціюються з регулярними кровотечами в період припинення дії активних речовин. Нині найпопулярніші чотири варіанти складу таких препаратів. Контрацептив, який застосовують у Китаї, містить 250 мг 17α-гідроксипрогестерону капронату і 5 мг естрадіолу валерату, а використовуваний у Мексиці та в інших країнах Латинської Америки — 150 мг дигідроксипрогестерону ацетофеніду і 10 мг естрадіолу енантату. Всесвітньою організацією охорони здоров''я розроблено дві нові формули, що їх застосовують у програмах планування сім''ї кількох країн. Комбінований препарат, що містить 25 мг медроксипрогестерону ацетату з естрадіолу ципіонатом, надходить на ринок під назвою циклофем (або циклопровера), а засіб, до складу якого входять 50 мг норетиндрону енантату й 5 мг естрадіолу валерату, — під назвою месигина. Ці препарати дають змогу контролювати кровотечу краще, ніж ті, що містять тільки прогестин. Майже в 85 % випадків цикли регулярні, а частота аменореї низька. За результатами п''ятьох клінічних випробувань, при вживанні циклофему й месігини частота випадків вагітності не перевищує відповідно 0,4 і 0,2 % за 12 місяців [97].
Д. Підшкірні імплантати
Підшкірні імплантати — капсули з полідиметилсилоксану (силастик, або силіконова гума), що містять левоноргестрел, — були розроблені Радою з проблем народонаселення США й дозволені до впровадження в Сполучених Штатах у 1990 році. Сьогодні 5,5 млн жінок використовують норплант, дозволений відповідними органами державного регулювання 60 країн. Доза стероїдів, що виділяються в організм, прямо пропорційна площі поверхні капсули, а тривалість дії залежить від кількості стероїдів у капсулах. Кожна з шістьох циліндричних капсул (довжина 3,4 см, зовнішній діаметр 2,4 мм), що імплантуються в жирову підшкірну клітковину, містить 36 мг кристалічного левоноргестрелу.
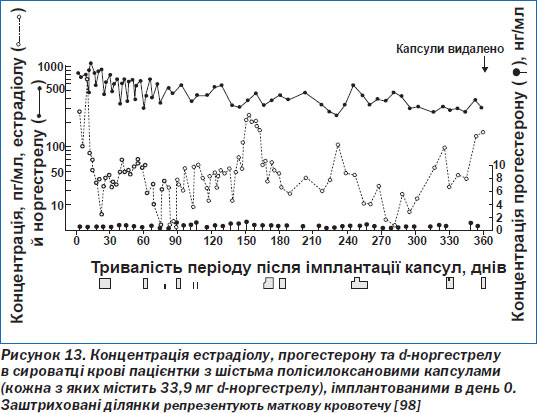
Після імплантації капсул концентрація левоноргестрелу в сироватці крові швидко зростає, досягаючи рівня 1000–2000 пг/мл за 24 години. Після закінчення першого місяця вона залишається відносно постійною протягом року (рис. 13) [98].
Через п''ять років середня концентрація левоноргестрелу в сироватці крові становить 170–350 пг/мл (у повніших жінок цей показник нижче, ніж у худих). Щоденний показник виділення левоноргестрелу становить у середньому 50 пг/мл протягом першого року й спадає до 30 пг/мл через вісім років.
1. Механізм дії
Визначити частоту овуляційних циклів у користувачок норпланту дуже важко. Згідно з даними одного дослідження, в якому показником концентрації прогестерону в сироватці крові понад 3 нг/мл скористались як ознакою наявності овуляції, приблизно в третині випадків цикли, можливо, були овуляційні. Однак концентрація прогестерону в користувачок виявилася значно нижчою порівняно зі спостережуваною в контрольних учасниць, що свідчить про високу частоту наявності дефіциту гормону жовтого тіла та/або ановуляційних лютеїнізованих фолікулів. Результати щоденного ультразвукового сканування яєчників у користувачок норпланту, в котрих спостерігалися регулярні цикли й підвищена концентрація прогестерону в лютеїновій фазі, показали, що тільки в одній третині циклів картина, отримана за допомогою ультразвукового сканування, збігалася з типовою для овуляції [99]. Оскільки лише половина циклів асоціювалися в користувачок з нормальними менструаціями, отримані дані дають підставу вважати, що в цих жінок овуляційними були менше ніж 20 % циклів і що в багатьох з них знижено вироблення прогестерону.
Продовження далі