Газета «Новости медицины и фармации» 9(325) 2010
Вернуться к номеру
Интраназальный спрей флютиказона фуроат в лечении аллергических ринитов
Авторы: Pedro Giavina-Bianchi, Rosana Agondi, Rafael Stelmach, Alberto Cukier, Jorge Kalil. University of Sao Paulo, Sao Paulo, Brazil
Версия для печати
Аллергический ринит
Аллергический ринит (АР) является воспалительным заболеванием слизистой оболочки полости носа, которое вызвано IgE-зависимым иммунным ответом. Клинически АР проявляется четырьмя основными симптомами: ринореей, чиханием, зудом и заложенностью носа (Международная рабочая группа по лечению ринитов, 1994; Bousquet и соавт., 2001).
У пациентов с АР могут также наблюдаться слабость, нарушения сна, затруднение выполнения социальных функций, депрессия, тревога, нарушение внимания, в результате чего снижается работоспособность и продуктивность на работе и в школе. Влияние АР на качество жизни пациента становится еще более выраженным при наличии таких сопутствующих заболеваний, как синусит, экссудативный средний отит, аллергический конъюнктивит, бронхиальная астма, поражение зубов. В целом для АР характерна высокая заболеваемость со значительной социальной и экономической (прямые и непрямые издержки) нагрузкой (Международная рабочая группа по лечению ринитов, 1994; Yawn и соавт., 1999; Crystal-Peters и соавт., 2000; Leynaert и соавт., 2000а; Bousquet и соавт., 2001; O''Connell, 2004; Schoenwetter и соавт., 2004).
Распространенность АР в общей популяции составляет 30 % и продолжает расти, особенно в западных странах (Организационный комитет Международного исследования астмы и аллергии у детей, фаза I (ISAAC Phase I), 1998; Upton и соавт., 2000; Bousquet и соавт., 2001). АР относится к наиболее частым хроническим заболеваниям у детей и должен рассматриваться в качестве одной из наибольших проблем общественного здоровья.
Аллергический ринит и его влияние на астму
Руководство ARIA (Аллергический ринит и его влияние на астму), вышедшее в свет в 2001 г., привнесло некоторые концептуальные изменения в представления о рините, включая модификацию его классификации и акцент на взаимосвязи патологии верхних и нижних дыхательных путей (Bousquet и соавт., 2001).
В зависимости от сроков возникновения заболевания и типа аллергена АР может быть разделен на круглогодичный и сезонный (сенная лихорадка).
У пациентов с сезонным АР обострение симптомов развивается главным образом во время сезона пыления. Позднее в зависимости от длительности симптомов и частоты обострений АР был разделен на интермиттирующий и персистирующий. Дополнительно в рамках этой же классификации АР делят на легкий, умеренный и тяжелый. При этом тяжесть заболевания определяется на основании краткой оценки нарушений в выполнении повседневных навыков, а не по выраженности назальных симптомов (Bousquet и соавт., 2001).
Сегодня ринит и бронхиальную астму рассматривают как проявления хронического аллергического респираторного синдрома. Накоплены эпидемиологические, иммунопатологические и клинические данные, которые подтверждают интегрированный взгляд на эти заболевания и закладывают основу для понимания их взаимодействия (Leynaert и соавт., 2000b; Bousquet и соавт., 2001; Linneberg и соавт., 2002; Togias, 2003). Почти у всех пациентов с бронхиальной астмой имеет место ринит, а наличие тяжелого ринита у таких пациентов ассоциируется с неблагоприятными исходами астмы. АР является фактором риска развития астмы. Интересно, что лечение АР оказывает положительное влияние на течение астмы: уменьшается необходимость в обращении за неотложной медицинской помощью, частота госпитализаций, снижается реактивность бронхов (Crystal-Peters и соавт., 2002; Taramarcaz, 2003).
Лечение ринита
Лечение ринита включает избегание контактов с аллергеном, фармако- и иммунотерапию. Интраназальные кортикостероиды (ИКС) рекомендуют в качестве терапии первой линии у пациентов с умеренным и тяжелым АР, особенно если основным симптомом при этом является заложенность носа (Международная рабочая группа по лечению ринитов, 1994; Bousquet и соавт., 2001; van Cauwenberge и соавт., 2005; Antonicelli и соавт., 2007). ИКС устраняют заложенность носа с большей клинической и экономической эффективностью, чем антигистаминные средства без седативного действия, обычно прописываемые в этом случае (Craig и соавт., 1998; Schoenwetter и соавт., 2004; Price и соавт., 2006). Пероральные антигистаминные средства могут использоваться вместе с ИКС при более тяжелом течении обострений ринита, а также у пациентов с глазными и кожными симптомами, которые могут присутствовать, поскольку те или иные атопические заболевания являются компонентами одного системного синдрома.
Основными преимуществами использования ИКС являются высокая концентрация препарата, быстрое начало действия, доставка прямо к месту действия, что исключает или минимизирует системные эффекты. ИКС взаимодействуют с внутриклеточными глюкокортикоидными рецепторами и проявляют противовоспалительную активность путем торможения продукции цитокинов, хемокинов, ферментов и молекул клеточной адгезии.
Рецепторная активность является фармакодинамическим параметром и отражает связывающую способность ИКС, которая выражается их аффинностью к рецепторам по сравнению с дексаметазоном. Местную активность глюкокортикоидов часто сравнивают с помощью пробы Маккензи, в которой оценивается побледнение кожи как мера вызываемой вазоконстрикции (McKenzie, 1962). Позже был предложен метод для сравнения биологических эффектов местных глюкокортикоидов на основе оценки их тормозного влияния на продукцию Т-лимфоцитзависимых цитокинов (English и соавт., 1994; Umland и соавт., 1997).
К фармакокинетическим параметрам, заслуживающим внимания, относятся наличие пролекарственной формы, накопление в органах, начало действия, липофильность, биодоступность, системный клиренс, связывание с белками, объем распределения, система доставки и время пребывания в полости носа.
В систематическом обзоре Cochrane сравнили эффективность и безопасность флютиказона пропионата с беклометазона дипропионатом и будесонидом при лечении хронической астмы. У пациентов, получавших флютиказона пропионат, была отмечена несколько лучшая функция легких, однако увеличивалась осиплость и, по-видимому, имел место риск развития ангины (Adams и соавт., 2007).
Важно подчеркнуть, что решение о назначении ИКС, особенно детям, должно приниматься на основе клинического опыта врача, индивидуальных особенностей пациентов и их предпочтений (Al Sayyad
и соавт., 2007).
Флютиказона фуроат
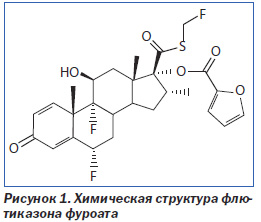 Флютиказона фуроат является новым местным, интраназальным трифторированным глюкокортикоидом с повышенной аффинностью к глюкокортикоидным рецепторам, который проявляет выраженное противовоспалительное действие и оказывает незначительную системную нагрузку. Флютиказона фуроат — синтетический фторированный глюкокортикоид с химическим названием (6α,11β,16α,17α)-6,9-дифтор-17-{[(фтор-метил)тио]карбонил}-11-гидрокси-16-метил-3-оксоандроста-1,4-диен-17-ил 2-фуранкарбоксилат (рис. 1). Данный препарат (GW685698X; VeramystТМ;
Флютиказона фуроат является новым местным, интраназальным трифторированным глюкокортикоидом с повышенной аффинностью к глюкокортикоидным рецепторам, который проявляет выраженное противовоспалительное действие и оказывает незначительную системную нагрузку. Флютиказона фуроат — синтетический фторированный глюкокортикоид с химическим названием (6α,11β,16α,17α)-6,9-дифтор-17-{[(фтор-метил)тио]карбонил}-11-гидрокси-16-метил-3-оксоандроста-1,4-диен-17-ил 2-фуранкарбоксилат (рис. 1). Данный препарат (GW685698X; VeramystТМ;
Авамис™) выпускают в виде назального спрея, содержащего водную суспензию тонкодисперсного флютиказона фуроата для местного применения. Доставка препарата в полость носа и дозирование осуществляется с помощью специального распылителя. При каждом нажатии выделяется 27,5 мкг флютиказона фуроата в 50 мкл суспензии, которая также содержит 0,015% (весовой процент) бензалкония хлорид, обезвоженную декстрозу, динатрия эдетат, микрокристаллическую целлюлозу, полисорбат 80 и очищенную воду.
Флютиказона фуроат был разработан для лечения АР у детей начиная с 2 лет и взрослых. Спрей имеет уникальный дизайн, поскольку кнопка для его распыления находится сбоку корпуса. Флютиказона фуроат вводится один раз в день, рекомендуемая начальная доза составляет 55 мкг у детей и 110 мкг у подростков и взрослых (Управление по контролю за продуктами и лекарствами США (FDA), 2007; GlaxoSmithKline, 2007; McCormack и Scott, 2007; RxList, 2007).
Фармакодинамический профиль
Флютиказона фуроат имеет высокую аффинность к глюкокортикоидным рецепторам, с низкой равновесной константой диссоциации (kd = 0,3 нмоль/л) и большей относительной рецепторной аффинностью (2989) по сравнению с мометазона фуроатом (2244), флютиказона пропионатом (1775), беклометазона-17-монопропионатом (1345), действующим началом циклесонида (1212) и будесонидом (855) (Biggadike и соавт., 2007).
В ряде исследований in vitro было показано, что флютиказона фуроат сильнее угнетает синтез и действие фактора некроза опухоли по сравнению с другими глюкокортикоидами. Он также более эффективно предохраняет культуру человеческих эпителиальных клеток легких от различных повреждений. Экспериментальные исследования свидетельствуют о том, что флютиказона фуроат проявляет более быструю и более выраженную противовоспалительную активность по сравнению с флютиказона пропионатом (Salter и соавт., 2006, 2007).
Флютиказона фуроат продемонстрировал более высокую избирательность к глюкокортикоидным рецепторам in vitro и не оказывал влияния на гипоталамо-гипофизарно-надпочечниковую систему у детей и взрослых во время проведения клинических исследований (Pastel и соавт., 2007; Salter и соавт., 2007; Tripathy и соавт., 2007). Лабораторные тесты, которые оценивают базальную и динамическую функцию гипоталамо-гипофизарно-надпочечниковой системы, часто используют для оценки системных эффектов ИКС.
Фармакокинетический профиль
После одно- и многократного интраназального введения флютиказона фуроата его концентрация в плазме крови у большинства пациентов находится ниже нижней границы количественного определения (Allen и соавт., 2007; Hughes и соавт., 2007; Martin, 2007). Только в одном исследовании было обнаружено, что при введении пациентам 110 мкг флютиказона фуроата в 2 % образцов плазмы крови наблюдались количественно определяемые концентрации препарата (Martin, 2007).
Системная биодоступность определяется суммой двух факторов: количеством препарата, которое абсорбируется через слизистую оболочку носовой полости, и количеством препарата, которое проглатывается. Это является основным путем попадания препарата в системный кровоток, что делает предсистемную элиминацию в печени после абсорбции препарата в желудочно-кишечном тракте особенно важной.
После интраназального введения здоровым взрослым волонтерам 10 доз флютиказона фуроата по 880 мкг с интервалом в 8 ч средняя абсолютная биодоступность составила 0,5 %. Пероральная биодоступность после однократного приема внутрь 2 мг препарата составила 1,26 %. Период полувыведения после однократного внутривенного введения препарата составил 15,1 ч (FDA, 2007; Allen и соавт., 2007).
In vitro 99,4 % флютиказона фуроата связывалось с белками плазмы. В другом исследовании было показано, что после абсорбции препарат подвергается интенсивной предсистемной элиминации (Salter и соавт., 2006; Allen и соавт., 2007). Связывание с белками имеет существенное значение, поскольку только свободная фракция препарата способна взаимодействовать с рецепторами. До тех пор, пока глюкокортикоид связан с белком, он не способен связываться с рецептором. Клиренс флютиказона фуроата осуществляется в основном в печени путем гидролиза с участием изофермента (CYP)3A4 цитохрома Р450, который превращает препарат в метаболит 17[бета]-карбоксиловой кислоты (М10), проявляющий низкую аффинность к глюкокортикоидным рецепторам. Препарат выделяется главным образом с калом, и лишь небольшое его количество выделяется с мочой (Hughes и соавт., 2005; FDA, 2007).
Флютиказона фуроат является синтетическим липофильным глюкокортикоидом (Biggadike и соавт., 2006). Известно, что высоколипофильные средства более быстро и более интенсивно захватываются слизистой оболочкой носовой полости, дольше удерживаются внутри тканей носа и обладают повышенной способностью достигать глюкокортикоидных рецепторов.
Общеизвестно, что многие пациенты используют ИКС только при необходимости и прекращают принимать препараты после уменьшения выраженности симптомов. В пользу данного подхода свидетельствуют и результаты последних исследований, в которых было показано, что эпизодическое использование ИКС приводит к развитию умеренного эффекта у большинства пациентов (Juniper и соавт., 1993). Из сказанного следует, что скорость начала действия является важной характеристикой для данной группы препаратов. В одном из клинических исследований круглогодичного АР статистически достоверная разница между флютиказона фуроатом и плацебо после введения первой дозы впервые была отмечена спустя 24 ч по данным фиксированной оценки общего балла назальных симптомов и спустя 2 дня по данным интервальной оценки общего балла назальных симптомов (Vasar и соавт., 2007).
Лекарственная форма и система доставки
Лекарственная форма и система доставки могут влиять на эффективность, переносимость и безопасность препарата, удерживание и накопление препарата в тканях носа, предпочтение пациентов и их приверженность к лечению (Hebner и соавт., 2005; Meltzer, 2007). Оптимизация лекарственной формы является одним из путей улучшения лечения ринита.
Влияние на сенсорный аппарат является важным фактором, определяющим предпочтение и приверженность пациентов к лечению ИКС. Пациенты оценивают ряд сенсорных параметров во время лечения ИКС: вкус, остающийся впоследствии привкус, запах, выделения из носа, стекание препарата в горло, раздражение, позывы на чихание (Mahadevia и соавт., 2004; Meltzer и соавт., 2005; Meltzer, 2007); при этом ощущение влажности и мягкости обычно оценивается позитивно.
Устройство доставки водного спрея флютиказона фуроата представляет собой легкий в использовании флакон с распылителем, который сконструирован так, что минимизируется риск повреждения тканей носа. Одним из элементов его конструкции является новый пусковой механизм, который уменьшает вариабельность доставляемой дозы (FDA, 2007; Berger и соавт., 2007). Устройство доставляет малый объем препарата, что уменьшает вероятность его стекания в горло или вытекания из носа. Оно пригодно для использования у маленьких детей и у лиц пожилого возраста.
Клинические исследования
Терапевтическая эффективность флютиказона фуроата при АР была подтверждена двойными слепыми плацебо-контролируемыми клиническими исследованиями (табл. 1).
В исследовании с несколькими дозами флютиказона фуроата, назначаемого подросткам и взрослым с сезонной аллергией на пыльцу мексиканского можжевельника, было установлено, что оптимальное соотношение между выгодами и рисками при приеме препарата наблюдается при использовании дозы 110 мкг. Достоверное снижение утренних (до приема препарата) значений при проведении фиксированной оценки общего балла носовых симптомов (iTNSS) свидетельствует по крайней мере о 24-часовой длительности эффекта (Martin и соавт., 2007).
Флютиказона фуроат был также эффективнее плацебо в отношении уменьшения выраженности глазных симптомов у взрослых и подростков с сезонным или круглогодичным АР (Stuebner, 2006; Fokkens и соавт., 2007a; Hampel и соавт., 2007; Kaiser и соавт., 2007; Ratner и соавт., 2007; Vasar et al., 2007). Механизм, благодаря которому препарат уменьшает проявления аллергического конъюнктивита, до конца не ясен. Возможно, это связано с уменьшением воспаления в полости носа, что приводит к уменьшению выброса провоспалительных медиаторов и, следовательно, меньшей активации клеток воспаления в соседних тканях; с улучшением дренажа из глаза в носослезный канал; или с модуляцией носоглазного нервного рефлекса. Непохоже, чтобы наблюдаемые эффекты были результатом системного действия флютиказона фуроата, поскольку он имеет низкую абсолютную биодоступность.
У пациентов, отмечающих выраженные глазные симптомы, в комплексе с ИКС могут быть использованы антигистаминные средства. Однако в метаанализе исследований, сравнивающих ИКС и антигистаминные средства, было обнаружено, что ИКС уменьшают глазные симптомы так же эффективно, как и пероральные антигистаминные средства (Weiner и соавт., 1998).
Безопасность и переносимость
Хорошо известно, что при длительном лечении системными глюкокортикоидами развиваются тяжелые побочные эффекты. ИКС, принимаемые в рекомендуемых дозах, как правило, не приводят к развитию стойких, клинически значимых или необратимых осложнений. Тем не менее многие врачи и пациенты все еще опасаются потенциальных побочных эффектов ИКС, что приводит к снижению приверженности к лечению данной группой средств — одна из наибольших проблем сегодняшней врачебной практики. Если врачи смогут эффективно донести до пациентов информацию о реальном соотношении между выгодами и рисками при использовании ИКС, то исходы от лечения пациентов могут быть улучшены (Rao и Apter, 2005).
При объединении результатов разных клинических исследований было обнаружено, что частота развития осложнений при интраназальном введении флютиказона фуроата подобна таковой при использовании плацебо. То же самое касалось и частоты преждевременного прекращения терапии. Наиболее частыми побочными эффектами (частота > 1 % у подростков/взрослых или > 3 % у детей, при этом частота больше, чем при приеме плацебо) были: головная боль, носовые кровотечения, назофарингит, пирексия, глоточно-гортанная боль, изъязвление слизистой носа, кашель, боль в спине (FDA, 2007).
Длительное назначение (12 месяцев) флютиказона фуроата взрослым и подросткам также хорошо переносилось, без развития каких-либо необычных или неожиданных осложнений. Среди пациентов, получавших флютиказона фуроат, по сравнению с плацебо-группой только носовые кровотечения наблюдались более часто и были выраженными (FDA, 2007; Rosenblut и соавт., 2007).
В течение всего времени лечения не было зафиксировано побочных эффектов, которые бы указывали на клинически значимые системные эффекты глюкокортикоидов.
В ряде исследований были получены данные о том, что лечение ИКС у детей может замедлять темпы роста, особенно во время первого года лечения. Однако также было выяснено, что обычные дозы ИКС не вызывают клинически значимой задержки роста у подавляющего большинства пациентов (Brand, 2001; Gulliver и Eid, 2005). Данная группа лекарственных средств может влиять на темпы роста только при попадании в системный кровоток. Как было отмечено выше, для флютиказона фуроата характерна низкая системная биодоступность. Кроме того, он не оказывал влияния на скорость роста ног у детей, оцененную с помощью кнемометрии (Gradman и соавт., 2007).
Необходимо соблюдать осторожность при совместном введении флютиказона фуроата с ингибиторами CYP3A4, такими как кетоконазол и ритонавир, поскольку увеличение поступления глюкокортикоида в системный кровоток может увеличивать риск развития системных побочных эффектов (FDA).
При введении ИКС в рекомендуемых дозах риск развития системных побочных эффектов достаточно низок.
При использовании более высоких доз врач должен оценить все возможные выгоды и риски. В целом для уменьшения риска развития системных побочных эффектов необходимо использовать самую низкую из эффективных доз ИКС.
Выводы
В настоящее время не вызывает сомнения важность ИКС для лечения АР. Они обладают доказанной эффективностью и рекомендуются в качестве терапии первой линии пациентам с персистирующими ринитами умеренной и выраженной степени тяжести.
Объем знаний об ИКС значительно вырос за последние 10 лет. Были выяснены механизм действия, фармакологические свойства и клиническая значимость этих препаратов при лечении аллергических заболеваний дыхательного тракта. Несмотря на то, что существующие ИКС обладают достаточной активностью, внедрение новых препаратов данного класса с улучшенным соотношением эффективности и безопасности по-прежнему продолжает приветствоваться.
Флютиказона фуроат в виде интраназального спрея является новым местным глюкокортикоидом с повышенной аффинностью к глюкокортикоидным рецепторам и уникальной конструкцией устройства для доставки препарата (кнопка для распыления спрея находится сбоку корпуса). Данный препарат эффективно устраняет назальные симптомы аллергического ринита. Кроме того, он способствует устранению глазных симптомов и улучшает качество жизни. Низкая биодоступность флютиказона фуроата при приеме внутрь и высокая способность к связыванию с белками плазмы крови минимизируют его системные побочные эффекты. Пролонгированное время удерживания флютиказона фуроата в полости носа способствует еще большему росту его эффективности, что позволяет использовать его 1 раз в день у взрослых, подростков и детей.
Флютиказона фуроат проявляет высокую местную активность, обладает низким потенциалом в отношении развития системных побочных эффектов и потому является оптимальным препаратом для лечения АР. Для флютиказона фуроата, как и любого нового препарата, необходимо проведение длительных исследований безопасности и эффективности, в ходе которых также может быть выявлено модифицирующее влияние препарата на течение АР.
Перевод к.м.н. А.В. Савустьяненко

