Газета «Новости медицины и фармации» 7(320) 2010
Вернуться к номеру
Хроническая болезнь почек
Авторы: Д.Д. Иванов, д.м.н., профессор, НМАПО им. П.Л. Шупика
Версия для печати
 Понятие хронической болезни почек
Понятие хронической болезни почек
С 2002 года по инициативе NKF-KDOQI™ в современной нефрологии используется понятие хронической болезни почек (ХБП, CKD — chronic renal disease) и классификация стадий ХБП. В 2003 году термин предложен также для использования в детской нефрологии. В 2005 году на 2-м съезде нефрологов Украины утверждены термины «хроническая болезнь почек» для взрослых пациентов и «хроническое заболевание почек» (ХЗП) для детей. Эта терминология носит собирательный характер и сходна с такими понятиями, как, например, ишемическая болезнь сердца (ИБС) или хронические неспецифические заболевания легких (ХНЗЛ).
Целесообразность использования термина «ХБП» в качестве диагноза несколько отличается для общей практики и специалистов. Так, в разъяснении определения и классификации ХБП A.S. Levey с соавт. было отмечено, что врачам общей практики нецелесообразно включать название заболевания почек в диагноз ХБП. Врач общей практики, гипертензиолог, диабетолог чаще диагностируют ХБП без нозологической верификации, заменяя известное ранее понятие «нефропатия». Нефрологом, прежде всего, подразумевается, что ХБП, как правило, прогрессирует с развитием хронической почечной недостаточности (ХПН). Именно понимание прогрессирования почечного процесса, его необратимости легло в основу терминологического выделения «хроническая болезнь почек», а не «хроническое заболевание почек». Вместе с тем в детском возрасте возможно обратное развитие хронического повреждения почек и восстановление функции органа, в связи с чем в приказе МЗ Украины № 365 от 20.07.05 используется термин «ХЗП».
Наличие ХБП должно устанавливаться независимо от первичного диагноза, исходя из признаков повреждения почек и/или скорости клубочковой фильтрации (СКФ). При этом ХБП может сама рассматриваться как диагноз, например: ХБП, 3-я стадия, гипертоническая болезнь, 2-я стадия, ІІІ степень, дефицитная анемия, 1-я степень. Диагноз «ХБП» еще не квалифицирован согласно МКБ-Х, но уже входит в последнюю редакцию Американского классификатора болезней.
Пациент имеет ХБП, если присутствует любой из следующих критериев (Am. J. Kidney Dis. — 2002. — 39. — 2, suppl. 1. — S18; 2-й съезд нефрологов Украины, 2005):
1. Повреждение почек ≥ 3 месяцев, которое обнаружено по структурным или функциональным нарушениям почек со снижением СКФ или без него, и проявление 1 или более из следующих признаков:
— нарушения, обнаруженные при биопсии почки.
2. СКФ < 60 мл/мин/1,73 м2 на протяжении ≥ 3 месяцев с другими признаками повреждения почек, приведенными выше, или без них.
Считается, что в популяции 10–17 % людей страдают ХБП. При этом диагностирована болезнь лишь у 1 % населения. Ежегодный прирост диализной ХПН (ХБП 5-й ст.) составляет около 100 пациентов на 1 млн населения, находясь в пределах от 60 в странах с холодным климатом до 150 больных в южных государствах. Данные о распространенности ХБП представлены в исследовании NeoЕRICA (рис. 1.1).
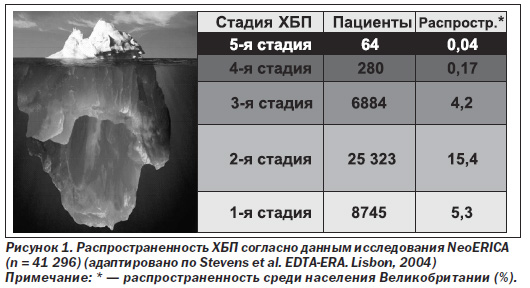
К сожалению, часто наблюдается гиподиагностика ХБП. Например, ХБП в США страдают около 20 миллионов жителей. Анализ, приведенный в исследовании NHANES III (National Health and Nutrition Examination Survey), свидетельствует о наличии у 11 % из 19,2 млн обследованных американцев хронической болезни почек, а именно: 3,3 % имели первую стадию ХБП (персистирующая микроальбуминурия со СКФ > 90 мл/мин); 3 % — вторую стадию ХБП (СКФ 60–89 мл/мин); 4,3 % — третью стадию (СКФ 30–59 мл/мин); 0,2 % — четвертую (СКФ 15–29 мл/мин) и 0,1 % — пятую (СКФ < 15 мл/мин).
ХБП может быть диагностирована без известной причины, так как для ее установления могут потребоваться специфические знания и/или проведение диагностических процедур, недоступных широкому кругу врачей.
Результаты анализа мочевого осадка, визуализационные исследования почки и некоторые клинические симптомы позволяют обнаружить разные варианты ХБП, в том числе гломерулярные, сосудистые, тубулоинтерстициальные и кистозные. При этом считается, что все реципиенты с почечным трансплантатом, независимо от СКФ, наличия или отсутствия маркеров поражения почек, имеют ХБП.
В большинстве случаев для выявления и контроля протеинурии следует использовать случайные разовые порции мочи. Как правило, для этих исследований нет необходимости в сборе мочи длительное время (ночные или суточные порции). Желаемой является первая утренняя порция, но возможно использование случайных порций, если утренняя порция не собрана. В большинстве случаев скрининг с помощью индикаторных тест-полосок является приемлемым для выявления протеинурии:
У пациентов с позитивными тестами с помощью индикаторных тест-полосок (1+ или больше) протеинурия должна быть подтверждена с помощью количественных методов (отношение белок/креатинин или альбумин/креатинин) на протяжении 3 месяцев.
У пациентов с наличием двух из трех или больше положительных количественных тестов в интервале 1–2 недели следует диагностировать персистирующую протеинурию и назначить им дополнительное обследование.
Таким образом, при подозрении на наличие ХБП руководство NKF-KDOQI™ рекомендует:
Авторы этих рекомендаций исходят из того, что наиболее часто ХБП сопровождается снижением СКФ и наличием микроальбуминурии. Результаты исследования NHANES III свидетельствуют, что у 20 % пациентов с диабетом и 43 % — с гипертензией при отсутствии протеинурии наблюдается СКФ менее 30 мл/мин. У 20 % пациентов с диабетом и 14,2 % — с гипертензией без диабета отмечалась СКФ менее 60 мл/мин, а количество таких пациентов росло с увеличением возраста. Результаты исследования свидетельствуют, что распространенность ХБП значительно выше, чем выявлено. При этом показанием для направления пациента к нефрологу является уровень креатинина 133–177 ммоль/л (или СКФ менее 60 мл/мин).
Неблагоприятные последствия ХБП часто могут быть предупреждены или отсрочены путем ранней диагностики и лечения. Первые стадии ХБП выявляются с помощью рутинных лабораторных исследований. Повреждение почки может быть установлено по показателям крови, мочи или по данным визуализационных исследований, а не с помощью биопсии почки. При этом персистирующая протеинурия и гипертензия служат важнейшими признаками повреждения почки. Обоснованием включения лиц с нормальной СКФ в группу ХБП является частая манифестация значительных повреждений почек еще до снижения этого ключевого показателя почечных функций, а также то, что эти пациенты имеют повышенный риск неблагоприятного исхода ХБП. Обоснованием включения лиц со СКФ < 60 мл/мин/1,73 м2 без любых других признаков повреждения почек является то, что снижение почечных функций ниже этого уровня отражает потерю почкой как минимум 50 % своих нормальных функций. Основания для определения СКФ меньше 60 мл/мин как необратимого снижения СКФ заключаются в следующем:
Перечень основных вариантов ХБП в зависимости от этиологического и патоморфологического факторов приведен в табл. 1.1.
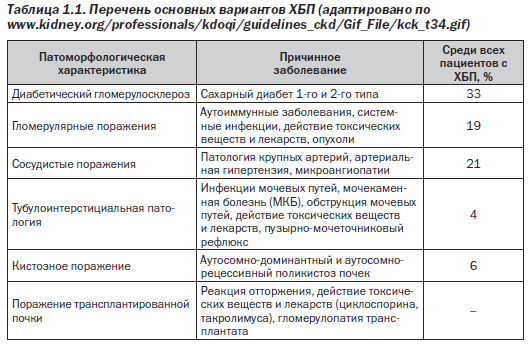
Как следует из данных табл. 1.1, самыми весомыми причинами развития ХБП (свыше 50 %) во взрослом возрасте являются диабет и гипертензия. Поэтому чаще всего именно они могут быть обнаружены терапевтом, семейным врачом, эндокринологом или кардиологом. При наличии микроальбуминурии и при подозрении на ХБП пациенты должны быть направлены к нефрологу для консультации и коррекции лечения. При уровне СКФ < 30 мл/мин/1,73 м2
пациенты обязательно должны консультироваться нефрологом/детским нефрологом. При возможности определения причинного фактора ХБП диагноз может быть сформулирован таким образом:
Современная терминология предполагает следующие определения наиболее часто встречаемых ХБП:
Конечный результат наиболее часто встречаемых ХБП — высокий риск кардиоваскулярной смерти.
Выявление причинного фактора ХБП позволяет назначить специфическую терапию и значительно отсрочить развитие хронической почечной недостаточности. Сам термин «ХБП» предусматривает, что заболевание прогрессирует с потерей функции почек, к сожалению, в большинстве случаев необратимо.
У детей определен свой перечень заболеваний, которые приводят к развитию ХБП:
Пример формулировки диагноза: геморрагический васкулит, смешанная форма. ХБП 1-й стадии: гломерулонефрит, изолированный мочевой синдром без нарушения функции почек.
В нефрологии выделяют 4 группы факторов риска, которые влияют на развитие и течение ХБП. Первая — это факторы, которые могут влиять на развитие ХБП, а именно: возраст пациента, отягощенный семейный анамнез по наличию ХБП, снижение размеров и объема почек, низкий вес при рождении или недоношенность (окончательное дозревание количества нефронов наблюдается на 38-й неделе внутриутробного развития), низкий материальный доход (социальный статус) и образовательный уровень. Вторая группа — факторы риска, которые инициируют ХБП. Они включают наличие сахарного диабета 1-го и 2-го типа, гипертензию, аутоиммунные заболевания, инфекции мочевых путей, мочекаменную болезнь, обструкцию мочевых путей, токсическое воздействие лекарств. Третья группа — факторы риска, которые приводят к прогрессированию ХБП, — представлена протеинурией или гипертензией высокой степени, неадекватным контролем гипергликемии, курением. Факторы риска конечной степени ХБП включают низкую диализную дозу, временный сосудистый доступ, анемию, низкий уровень альбумина, позднее начало почечнозаместительной терапии.
В детской нефрологии также выделяют 4 группы риск-факторов развития ХБП:
Следует отметить, что дозревание нормального количества нефронов наблюдается на 38-й неделе гестации при наличии нормальной массы плода. Поэтому все недоношенные или новорожденные с малым весом тела не имеют нормального количества нефронов. Это является риском развития ХБП, ранней гипертензии и более тяжелого течения приобретенных заболеваний почек.
Из книги Д.Д. Иванова «Лекции по нефрологии. — Донецк: Издатель Заславский А.Ю., 2010.
